Clear Sky Science · zh
CXCR5+ 单核细胞外迁损害放射诱导的抗肿瘤免疫反应
当癌症治疗与自身作对
放射治疗是癌症护理的基石,超过一半的患者会接受这种治疗。其目的是破坏肿瘤细胞并动员免疫系统完成清除任务。然而,许多肿瘤在看似成功的治疗后仍会复发。本研究揭示了一个令人意外的原因:放疗后某些免疫细胞被吸引进入肿瘤,最终非但没有协助消灭肿瘤,反而为其提供保护。 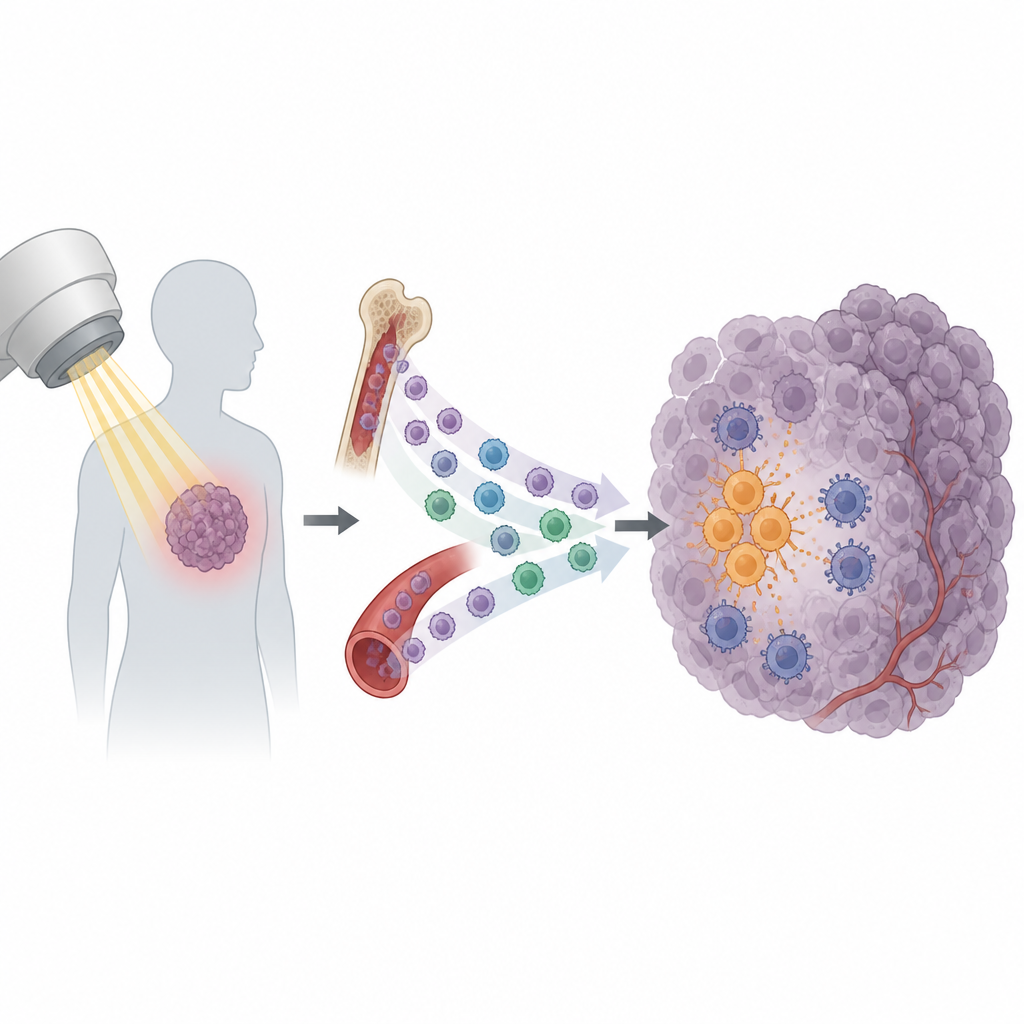
放射的双刃效应
放疗不仅仅是让癌细胞的 DNA 断裂。它还促使肿瘤释放一阵信号,招募免疫细胞。其中一些信号有助于激活杀伤性 T 细胞,使其识别并攻击肿瘤细胞。但也有相反作用的信号。研究者聚焦于一类循环免疫细胞——单核细胞。在若干小鼠肿瘤模型中,放疗后进入肿瘤的单核细胞数量急剧上升,而其他白细胞类型变化不大。这一模式提示,单核细胞可能是决定肿瘤对放疗敏感或耐受的重要角色。
引诱抑制性细胞的化学踪迹
进一步研究发现,接受放疗的肿瘤会产生更多名为 CXCL13 的化学信号。携带相应“接收器”分子 CXCR5 的单核细胞尤其倾向于在治疗后涌入肿瘤。即便在放疗之前,癌症已经在远处对这些细胞进行预置。肿瘤细胞向血液分泌生长因子 VEGF,激活单核细胞内一条名为 PI3K、Akt、mTOR 和 HIF-1α 的信号通路。这种内部传导改变提高了它们表面的 CXCR5 表达,有效地产生了一批循环中的 CXCR5 阳性单核细胞储备,随时准备沿着 CXCL13 的踪迹进入被照射的肿瘤。
被招募细胞如何使肿瘤杀手沉默
一旦进入肿瘤,CXCR5 阳性的单核细胞并没有表现出帮助防御的行为。相反,它们强烈抑制了 CD8 T 细胞的活性,而这些正是放疗后清除癌细胞所需要的细胞。在体外试验中,这些单核细胞减慢了 T 细胞的增殖并降低了其关键攻击分子的产生。这一效应在很大程度上依赖于 PD-L1——单核细胞表的一种免疫检查点蛋白,它与 T 细胞上的 PD-1 结合并发出抑制信号。缺失 CXCR5 的小鼠或缺失肿瘤 CXCL13 的模型在放疗后显示出更好的肿瘤控制和更活跃的 CD8 T 细胞。用抗体阻断 CXCL13 或 PD-L1 在多个模型中进一步提升了放疗效果,指向从单核细胞招募到 T 细胞抑制并导致治疗失败的一条明确链条。 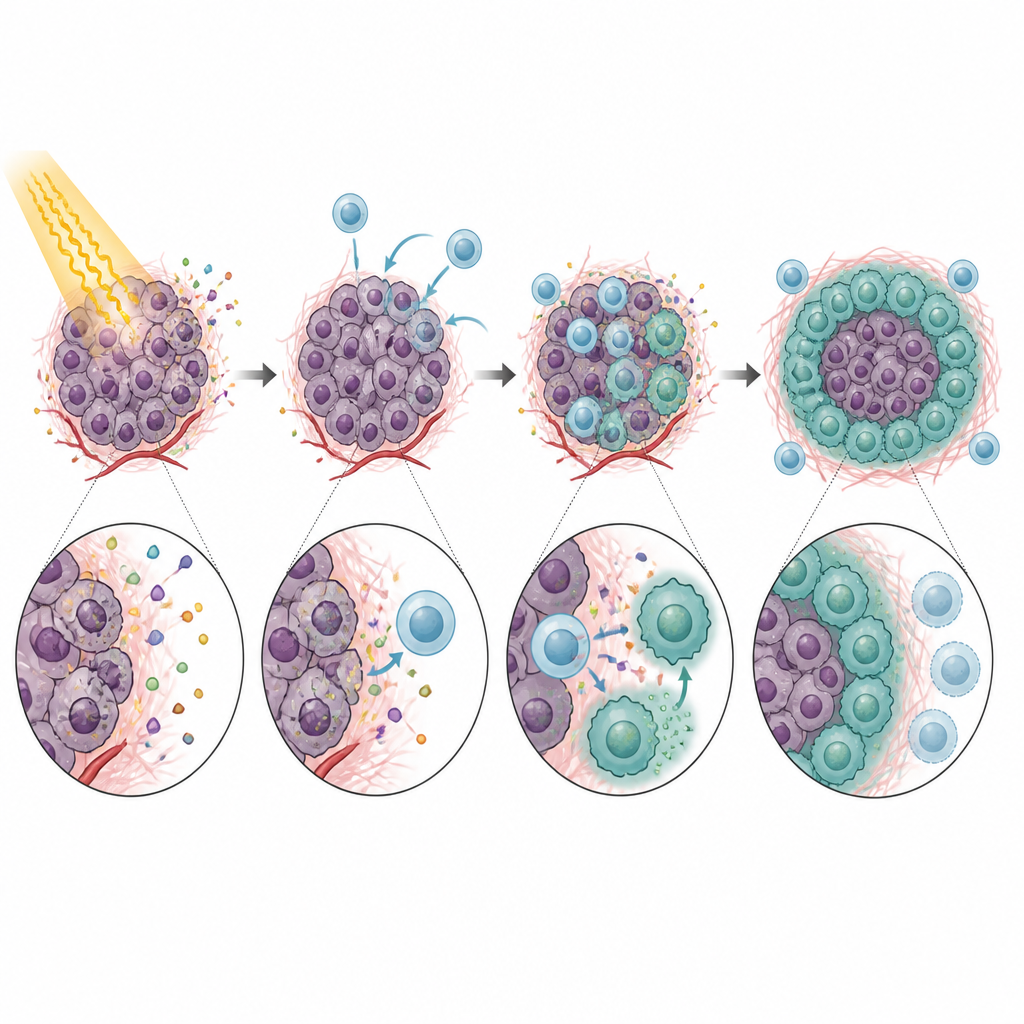
从可动的抑制者到固定的屏障细胞
故事并未止步于单核细胞。进入肿瘤后,许多 CXCR5 阳性单核细胞进一步分化为巨噬细胞,另一类免疫细胞。在放疗诱导的生长因子 GM-CSF 影响下,这些后代表现出 M2 样巨噬细胞的特征,M2 型通常被认为会抑制免疫反应并支持组织修复。这些 CXCR5 阳性巨噬细胞富含 PD-L1 及其他与免疫抑制相关的基因,对阻断 T 细胞活性尤其有效。降低 GM-CSF 水平或破坏 CXCL13–CXCR5 轴可减少这类 M2 样巨噬细胞的数量,并在小鼠中改善放疗反应。
来自患者样本的线索与可能的新策略
为测试在人类中是否存在类似过程,研究者分析了公开的癌症数据集和接受放疗的患者样本。接受放疗的肿瘤显示出更高的 CXCR5、CD14(人类单核细胞标志)和 PD-L1 表达水平。在血液样本中,疾病后来进展的患者在治疗后单核细胞数量上升,而肿瘤缩小或稳定的患者则没有这种上升。在直肠癌标本中,放疗后的肿瘤含有更多 CXCL13 以及 CXCR5 阳性的单核细胞和巨噬细胞。在细胞培养中,暴露于肿瘤液的人的单核细胞表现出与小鼠相似的行为,通过 VEGF 驱动的信号获得 CXCR5 并表达高水平 PD-L1。
将弱点转为优势
总体而言,这项工作表明放疗可能无意中召集并重塑一类免疫细胞,使其保护肿瘤免受原本旨在摧毁它们的治疗。通过在肿瘤中提高 CXCL13 水平及在单核细胞中通过 VEGF 驱动提高 CXCR5,放疗建立了一条输送抑制性单核细胞和巨噬细胞的通道,这些细胞随后通过 PD-L1 使杀伤性 T 细胞失活。在小鼠模型中,在多个环节干预这条通道——例如阻断 VEGF、CXCL13、GM-CSF 或 PD-L1——可使放疗更有效。对患者而言,这些发现提示将放疗与针对性的免疫药物合理组合,可能会将天平重新倾向于真正的抗肿瘤反应,从而改善癌症的长期控制。
引用: Lei, Y., Jia, R., Chen, C. et al. CXCR5+ monocyte emigration impairs the radiation-induced antitumor immune response. Nat Commun 17, 4258 (2026). https://doi.org/10.1038/s41467-026-70858-6
关键词: 放射治疗, 肿瘤免疫, 单核细胞, 免疫抑制, PD-L1