Clear Sky Science · es
La emigración de monocitos CXCR5+ perjudica la respuesta inmune antitumoral inducida por la radiación
Cuando el tratamiento contra el cáncer se vuelve contra sí mismo
La radioterapia es un pilar del tratamiento oncológico, empleada en más de la mitad de los pacientes. Su objetivo es dañar las células tumorales y movilizar al sistema inmune para rematar el trabajo. Sin embargo, muchos tumores reaparecen tras un curso de tratamiento aparentemente exitoso. Este estudio descubre una razón sorprendente: ciertos glóbulos inmunitarios son atraídos al tumor después de la radiación y terminan protegiendo al cáncer en lugar de ayudar a destruirlo. 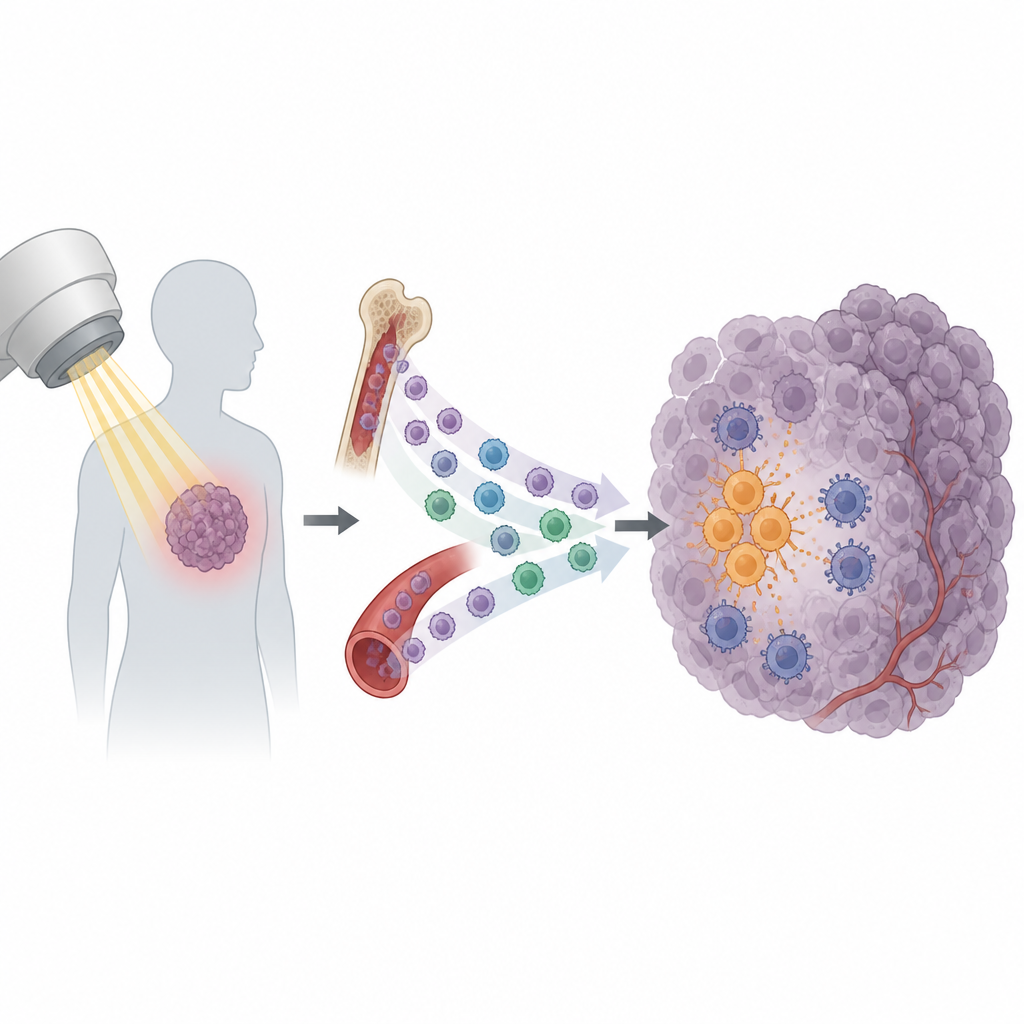
Un efecto de doble filo de la radiación
La radiación hace más que romper el ADN de las células cancerosas. También provoca que los tumores liberen una oleada de señales que reclutan células inmunitarias. Algunas de estas señales ayudan a activar a las células T citotóxicas, que pueden reconocer y atacar las células tumorales. Pero otras parecen producir el efecto contrario. Los investigadores se centraron en una subpoblación de células circulantes llamadas monocitos. En varios modelos murinos de tumor, la radiación provocó un aumento marcado de monocitos que entraban en el tumor, mientras que otros tipos de leucocitos cambiaron poco. Este patrón sugirió que los monocitos podrían ser actores importantes en que un tumor se vuelva sensible o resistente a la radiación.
Un rastro químico que atrae células supresoras
Indagando más, el equipo encontró que los tumores expuestos a radiación producían más de una señal química llamada CXCL13. Los monocitos que portan un receptor coincidente, CXCR5, fueron especialmente propensos a inundar el tumor tras el tratamiento. Antes de cualquier radiación, el cáncer ya había estado preparando a estas células a distancia. Las células tumorales secretaban el factor de crecimiento VEGF en el torrente sanguíneo, lo que activó una cadena de señales dentro de los monocitos conocida como vía PI3K, Akt, mTOR y HIF-1α. Este cambio interno aumentó CXCR5 en su superficie, creando efectivamente una reserva circulante de monocitos CXCR5-positivos listos para seguir el rastro de CXCL13 hacia los tumores irradiados.
Cómo las células reclutadas silencian a los asesinos tumorales
Una vez dentro del tumor, los monocitos CXCR5-positivos no actuaron como defensores útiles. En cambio, limitaban con fuerza la actividad de las células T CD8, las mismas células necesarias para que el sistema inmune elimine el cáncer tras la radiación. En pruebas de laboratorio, estos monocitos frenaron el crecimiento de las células T y redujeron su producción de moléculas clave de ataque. El efecto dependía en gran medida de PD-L1, una proteína de control en los monocitos que se acopla a PD-1 en las células T e indica que se detengan. Ratones carentes de CXCR5, o tumores carentes de CXCL13, mostraron mejor control tumoral tras la radiación y más células T CD8 activas. Bloquear CXCL13 o PD-L1 con anticuerpos mejoró aún más el impacto de la radiación en varios modelos, apuntando a una cadena clara desde el reclutamiento de monocitos hasta la supresión de células T y el fracaso del tratamiento. 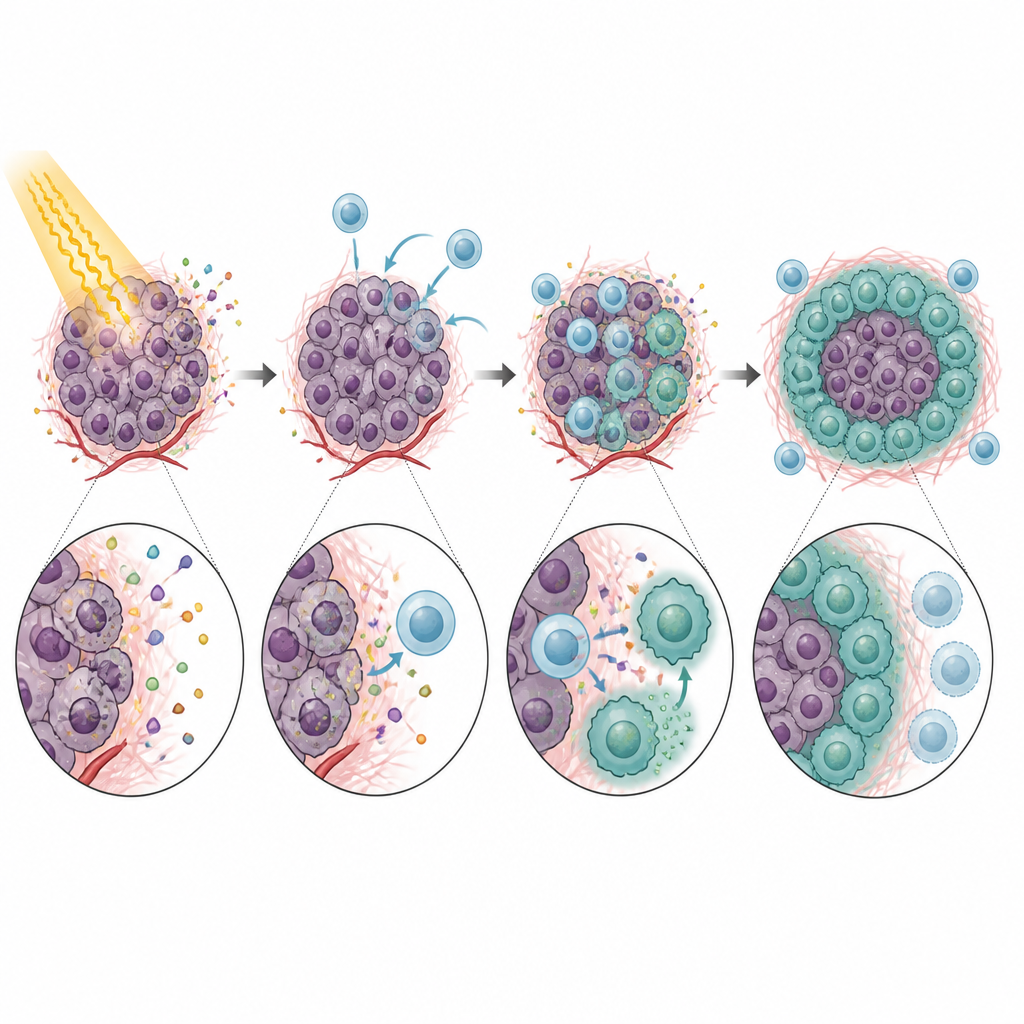
De supresores móviles a células escudo asentadas
La historia no terminó con los monocitos. Tras entrar en el tumor, muchos monocitos CXCR5-positivos maduraron a macrófagos, otro tipo de célula inmune. Bajo la influencia de un factor de crecimiento inducido por la radiación llamado GM-CSF, estos descendientes adquirieron rasgos de macrófagos tipo M2, conocidos por atenuar las respuestas inmunes y favorecer la reparación tisular. Estos macrófagos CXCR5-positivos eran ricos en PD-L1 y en otros genes vinculados a la supresión inmune, y eran particularmente eficaces para bloquear la actividad de las células T. Reducir los niveles de GM-CSF o interrumpir el eje CXCL13–CXCR5 disminuyó el número de estos macrófagos tipo M2 y mejoró las respuestas tumorales a la radiación en ratones.
Pistas en muestras de pacientes y posibles nuevas estrategias
Para comprobar si procesos similares ocurren en humanos, los investigadores examinaron bases de datos cancerígenas públicas y muestras de pacientes que recibían radioterapia. Los tumores de pacientes que se habían sometido a radiación mostraron niveles más altos de CXCR5, CD14 (un marcador de monocitos humanos) y PD-L1. En muestras de sangre, el número de monocitos aumentó tras el tratamiento en pacientes cuya enfermedad progresó posteriormente, pero no en aquellos cuyos tumores se redujeron o permanecieron estables. En muestras de cáncer de recto, los tumores tras la radioterapia contenían más CXCL13 y monocitos y macrófagos CXCR5-positivos. En cultivo celular, los monocitos humanos expuestos a fluidos tumorales se comportaron de forma similar a los de ratón, aumentando CXCR5 mediante señalización impulsada por VEGF y expresando altos niveles de PD-L1.
Convertir una debilidad en una ventaja
En conjunto, este trabajo muestra que la radiación puede, de forma no intencionada, atraer y reprogramar una población de células inmunes que protegen a los tumores del tratamiento que pretende destruirlos. Al aumentar CXCL13 en los tumores y el CXCR5 impulsado por VEGF en los monocitos, la radiación crea una vía que entrega monocitos y macrófagos supresores, que luego apagan a las células T citotóxicas mediante PD-L1. En modelos murinos, interrumpir esta vía en varios puntos, como bloqueando VEGF, CXCL13, GM-CSF o PD-L1, permitió que la radiación funcionara con mayor eficacia. Para los pacientes, estos hallazgos sugieren que combinar la radioterapia con fármacos inmunomoduladores seleccionados podría inclinar la balanza de nuevo hacia una verdadera respuesta antitumoral y mejorar el control a largo plazo del cáncer.
Cita: Lei, Y., Jia, R., Chen, C. et al. CXCR5+ monocyte emigration impairs the radiation-induced antitumor immune response. Nat Commun 17, 4258 (2026). https://doi.org/10.1038/s41467-026-70858-6
Palabras clave: radioterapia, inmunidad tumoral, monocitos, supresión inmune, PD-L1