Clear Sky Science · ar
هجرة الخلايا المونوسيتية CXCR5+ تضعف الاستجابة المناعية المضادة للورم الناتجة عن الإشعاع
عندما يقاتل علاج السرطان نفسه
يُعد العلاج الإشعاعي ركيزة أساسية من رعاية السرطان، ويُستخدم لأكثر من نصف المرضى. الهدف منه إحداث ضرر في خلايا الورم وتحفيز الجهاز المناعي لإكمال المهمة. ومع ذلك، تعود العديد من الأورام بعد دورة علاج تبدو ناجحة ظاهرياً. تكشف هذه الدراسة سبباً مفاجئاً: فبعض الخلايا المناعية تُسحب إلى الورم بعد الإشعاع وتنتهي بحماية السرطان بدلاً من المساعدة في تدميره. 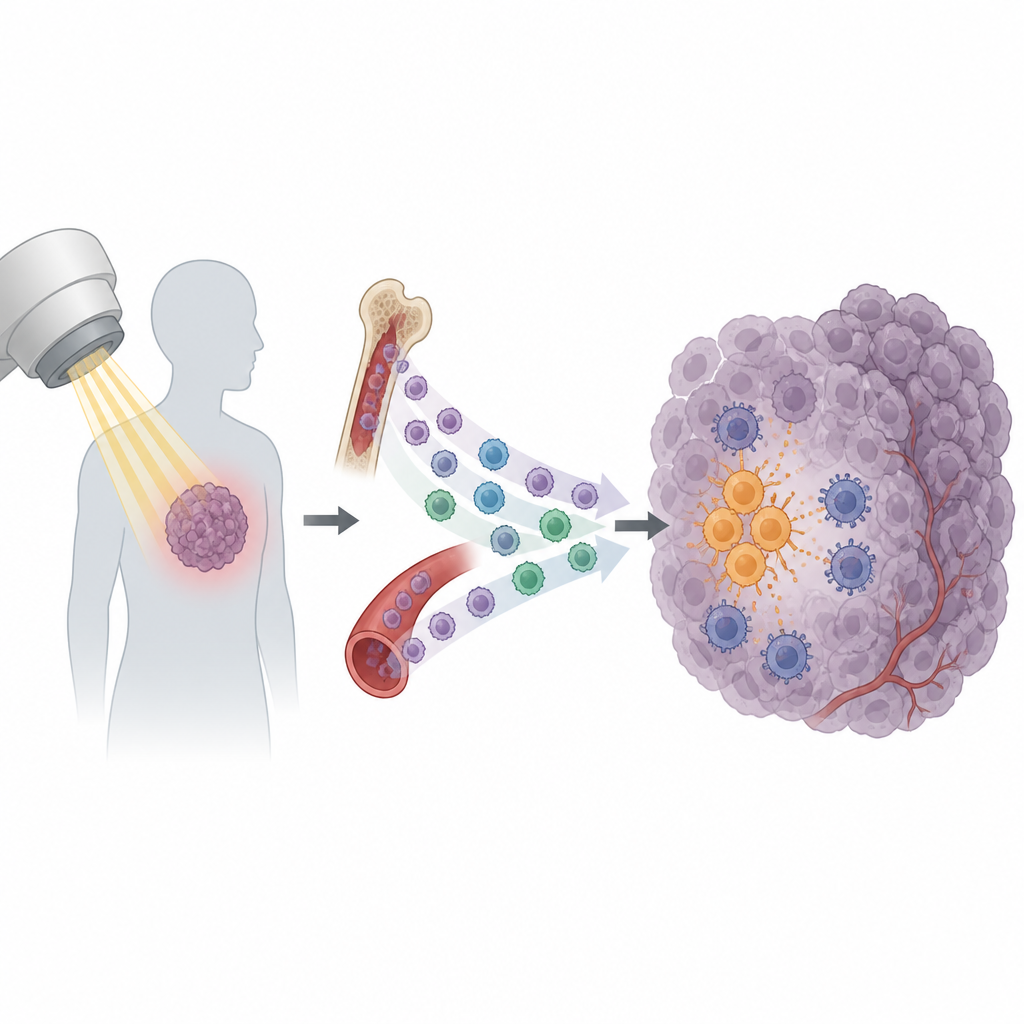
تأثير ذو حدين للإشعاع
لا يقتصر تأثير الإشعاع على كسر الحمض النووي في خلايا السرطان فحسب. بل يسبب أيضاً أن تُطلق الأورام دفعة من الإشارات التي تستدعي خلايا مناعية. بعض هذه الإشارات يساعد في تفعيل الخلايا التائية القاتلة، القادرة على تمييز ومهاجمة خلايا الورم. لكن يبدو أن إشارات أخرى لها تأثير معاكس. ركز الباحثون على مجموعة من الخلايا المناعية في الدم تُدعى المونوسيتات. في عدة نماذج ورمية للفئران، أدى الإشعاع إلى ارتفاع حاد في دخول المونوسيتات إلى الورم، بينما تغيرت أنواع أخرى من خلايا الدم البيضاء قليلاً. أشارت هذه النمطية إلى أن المونوسيتات قد تكون لاعبين مهمين في تحديد ما إذا كان الورم سيصبح حساساً أو مقاومًا للإشعاع.
أثر كيميائي يجذب الخلايا الكابحة
بالتعمق أكثر، وجد الفريق أن الأورام المعرضة للإشعاع أنتجت مزيداً من إشارة كيميائية تُدعى CXCL13. كانت المونوسيتات الحاملة لجزيء "المستقبل" المطابق، CXCR5، أكثر ميلاً للفيضان إلى داخل الورم بعد العلاج. قبل أي إشعاع، كان السرطان نفسه قد أعد هذه الخلايا عن بُعد. أفرزت الخلايا الورمية عامل نمو يُدعى VEGF إلى مجرى الدم، ما أدى إلى تشغيل سلسلة إشارات داخل المونوسيتات تُعرف بمسار PI3K وAkt وmTOR وHIF-1α. هذا التغيير الداخلي زاد من تعبير CXCR5 على سطحها، فأنشأ فعلياً مخزوناً دائرياً من المونوسيتات الموجبة لـ CXCR5 المستعدة لاتباع أثر CXCL13 نحو الأورام المعرضة للإشعاع.
كيف تُسكت الخلايا المجندة قناصي الورم
بمجرد دخولها إلى الورم، لم تتصرف المونوسيتات الموجبة لـ CXCR5 كمدافعين مفيدين. بل إنها كبتت بقوة نشاط الخلايا CD8 التائية، وهي الخلايا الضرورية للجهاز المناعي لتنقية السرطان بعد الإشعاع. في اختبارات المختبر، أبطأت هذه المونوسيتات نمو الخلايا التائية وخفضت إنتاجها لجزيئات هجوم رئيسية. اعتمد هذا التأثير إلى حد كبير على PD-L1، بروتين نقاط التفتيش على المونوسيتات الذي يرتبط بـ PD-1 على الخلايا التائية ويأمرها بالتراجع. أظهرت الفئران الخالية من CXCR5، أو الأورام الخالية من CXCL13، تحكماً أفضل في الورم بعد الإشعاع ونشاطاً أكبر للخلايا CD8 التائية. كما أن حجب CXCL13 أو PD-L1 بالأجسام المضادة حسّن تأثير الإشعاع في عدة نماذج، ما يشير إلى سلسلة واضحة من تجنيد المونوسيتات إلى قمع الخلايا التائية وفشل العلاج. 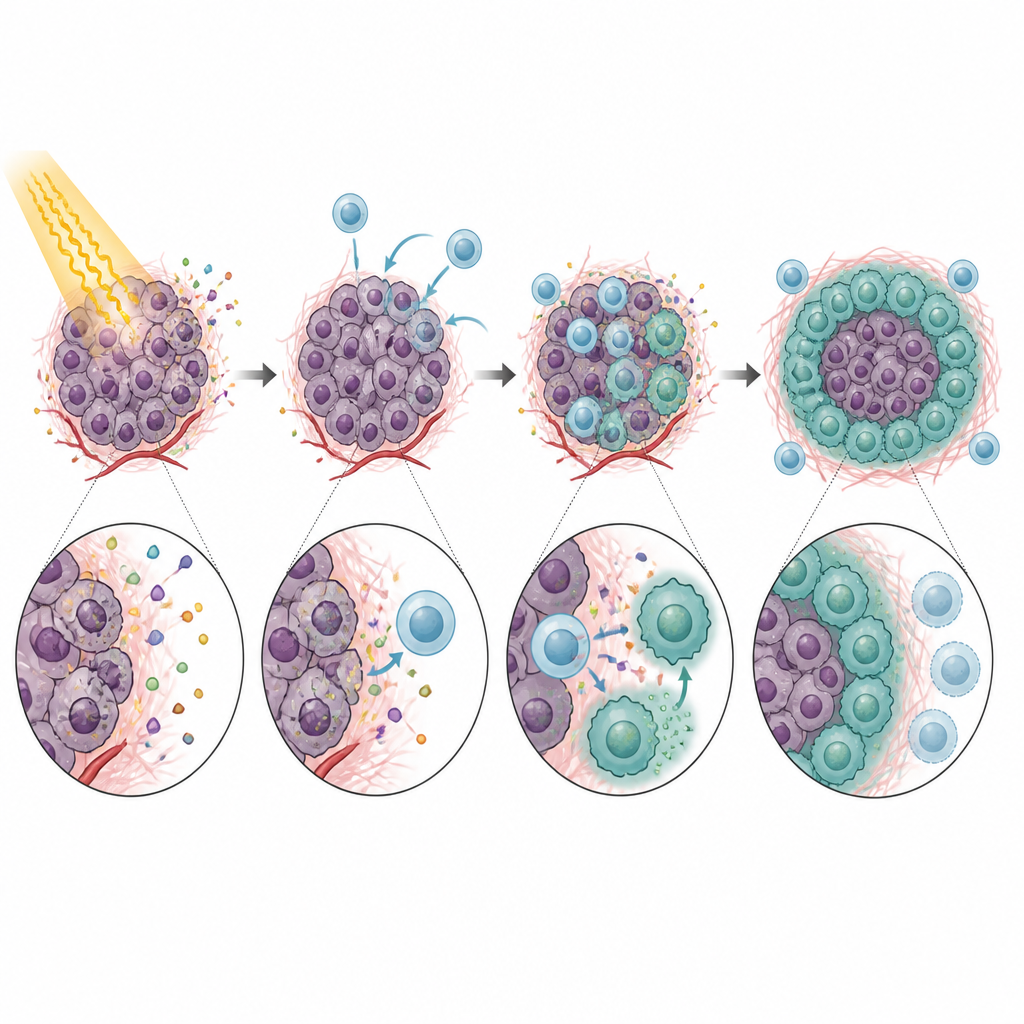
من الكابحات المتحركة إلى خلايا درع مستقرة
لم تنته القصة بالمونوسيتات. بعد دخولها الورم، تحوَّل العديد من المونوسيتات الموجبة لـ CXCR5 إلى البلاعم (الماكروفاج)، وهو نوع آخر من الخلايا المناعية. تحت تأثير عامل نمو ناتج عن الإشعاع يُدعى GM-CSF، اكتسبت هذه السلالات سمات البلاعم الشبيهة بـ M2، والمعروفة بتقليل الاستجابات المناعية ودعم إصلاح الأنسجة. كانت هذه البلاعم الموجبة لـ CXCR5 غنية بـ PD-L1 وجينات أخرى مرتبطة بالقمع المناعي، وكانت فعالة بشكل خاص في حجب نشاط الخلايا التائية. إن تقليل مستويات GM-CSF أو تعطيل محور CXCL13–CXCR5 خفّض عدد هذه البلاعم الشبيهة بـ M2 وحسّن استجابة الأورام للإشعاع في الفئران.
دلالات من عينات المرضى واستراتيجيات ممكنة جديدة
لاختبار ما إذا كانت عمليات مماثلة تحدث لدى البشر، فحص الباحثون مجموعات بياناتسرطانية متاحة علناً وعيّنات من مرضى تلقوا العلاج الإشعاعي. أظهرت الأورام لدى مرضى تعرضوا للإشعاع مستويات أعلى من CXCR5 وCD14 (وهو علامة على المونوسيت البشري) وPD-L1. في عينات الدم، ارتفعت أعداد المونوسيت بعد العلاج لدى المرضى الذين تقدمت حالتهم لاحقاً، ولم يحدث ذلك في المرضى الذين تقلصت أورامهم أو ظلت مستقرة. في عينات سرطان المستقيم، احتوت الأورام بعد العلاج الإشعاعي على مزيد من CXCL13 ومونوسيتات وبلاعم موجبة لـ CXCR5. في ثقافات خلوية، أظهرت المونوسيتات البشرية المعرضة لسوائل ورمية سلوكاً شبيهاً بما لوحظ في الفئران، إذ اكتسبت CXCR5 عبر إشارة مدفوعة بـ VEGF وعبّرت عن مستويات مرتفعة من PD-L1.
تحويل نقطة ضعف إلى ميزة
بشكل عام، تُظهر هذه الدراسة أن الإشعاع يمكن أن يستدعي عن غير قصد ويُعيد تشكيل مجموعة من الخلايا المناعية التي تحمي الأورام من العلاج المقصود بتدميرها. من خلال تعزيز CXCL13 في الأورام ورفع CXCR5 في المونوسيتات بواسطة VEGF، يخلق الإشعاع ممرًا يمد الأورام بمونوسيتات وبلاعم كابحة، والتي تطفئ الخلايا التائية القاتلة عبر PD-L1. في نماذج الفئران، سمح تعطيل هذا الممر عند نقاط متعددة—مثل حجب VEGF أو CXCL13 أو GM-CSF أو PD-L1—للإشعاع بأن يعمل بفعالية أكبر. تشير هذه النتائج إلى أنه يمكن لمزج العلاج الإشعاعي بأدوية مناعية مستهدفة بعناية أن يعيد التوازن لصالح استجابة مناعية حقيقية مضادة للورم ويحسن التحكم طويل الأمد بالسرطان لدى المرضى.
الاستشهاد: Lei, Y., Jia, R., Chen, C. et al. CXCR5+ monocyte emigration impairs the radiation-induced antitumor immune response. Nat Commun 17, 4258 (2026). https://doi.org/10.1038/s41467-026-70858-6
الكلمات المفتاحية: العلاج الإشعاعي, مناعة الورم, المونوسيتات, القمع المناعي, PD-L1