Clear Sky Science · pt
Emigração de monócitos CXCR5+ prejudica a resposta antitumoral induzida por radiação
Quando o tratamento do câncer luta contra si mesmo
A radioterapia é um pilar do tratamento do câncer, utilizada em mais da metade dos pacientes. Seu objetivo é danificar as células tumorais e mobilizar o sistema imune para concluir o trabalho. Ainda assim, muitos tumores voltam após um curso de tratamento aparentemente bem-sucedido. Este estudo revela um motivo surpreendente: certas células do sistema imune são atraídas para o tumor após a radiação e acabam protegendo o câncer em vez de ajudar a destruí-lo. 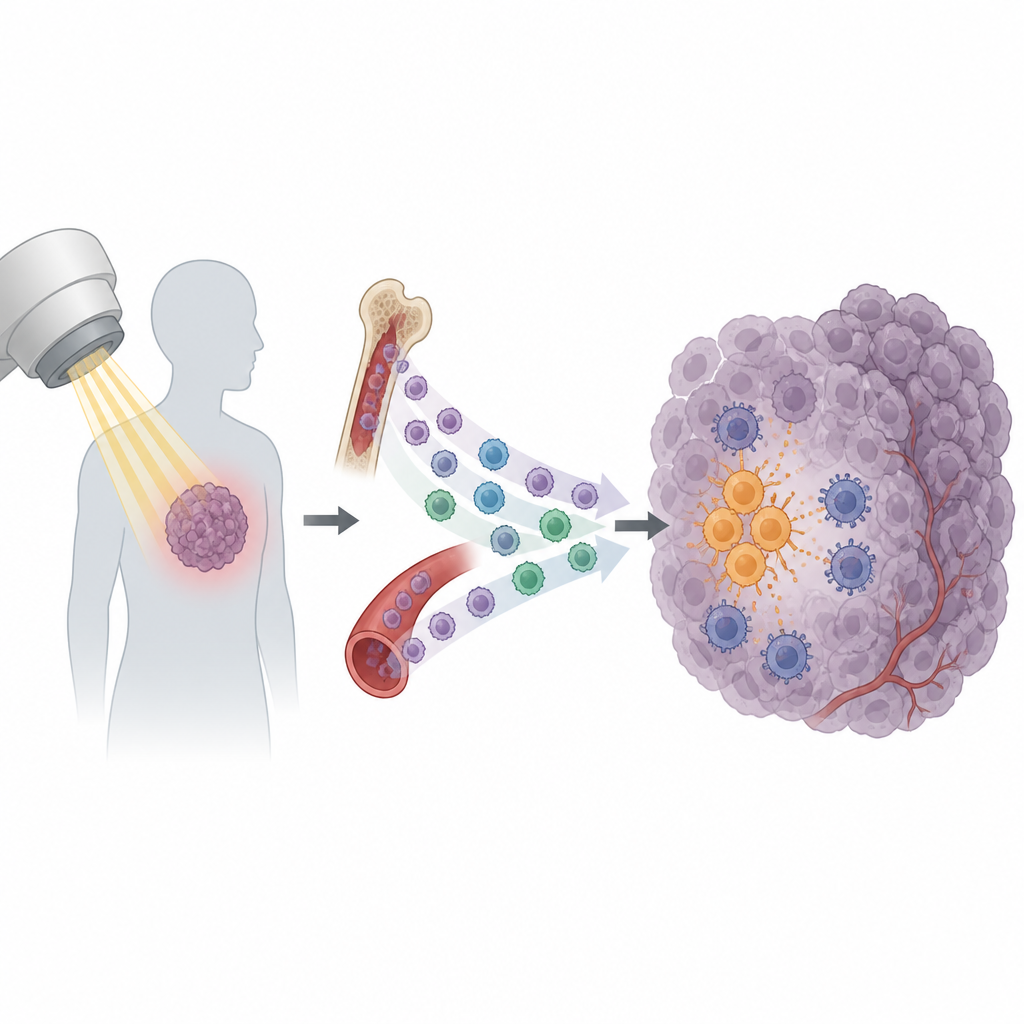
Um efeito de dois gumes da radiação
A radiação faz mais do que apenas quebrar o DNA das células cancerosas. Ela também faz com que os tumores liberem uma onda de sinais que recrutam células imunes. Alguns desses sinais ajudam a ativar células T citotóxicas, que podem reconhecer e atacar células tumorais. Mas outros parecem ter o efeito oposto. Os pesquisadores concentraram-se em um subconjunto de células imunes circulantes chamadas monócitos. Em vários modelos murinos de tumor, a radiação causou um aumento acentuado de monócitos entrando no tumor, enquanto outros tipos de leucócitos mudaram pouco. Esse padrão sugeriu que os monócitos podem ser protagonistas importantes na sensibilidade ou resistência do tumor à radiação.
Uma trilha química que atrai células supressoras
Aprofundando, a equipe descobriu que tumores expostos à radiação produziram mais do sinal químico chamado CXCL13. Monócitos que carregam um “receptor” correspondente, o CXCR5, foram especialmente propensos a invadir o tumor após o tratamento. Antes de qualquer radiação, o próprio câncer já vinha preparando essas células à distância. Células tumorais secretaram o fator de crescimento VEGF na corrente sanguínea, que ligou uma cascata de sinais dentro dos monócitos conhecida como via PI3K, Akt, mTOR e HIF-1α. Essa alteração na sinalização interna aumentou a expressão de CXCR5 em sua superfície, criando efetivamente uma reserva circulante de monócitos CXCR5-positivos pronta para seguir a trilha de CXCL13 até tumores irradiados.
Como as células recrutadas silenciam os assassinos tumorais
Uma vez dentro do tumor, os monócitos CXCR5-positivos não agiram como defensores úteis. Em vez disso, restringiram fortemente a atividade das células T CD8, justamente as células necessárias para que o sistema imune elimine o câncer após a radiação. Em testes laboratoriais, esses monócitos retardaram o crescimento das células T e reduziram a produção de moléculas de ataque essenciais. O efeito dependia em grande parte de PD-L1, uma proteína de ponto de controle nos monócitos que interage com PD-1 nas células T e as faz recuar. Camundongos sem CXCR5, ou tumores sem CXCL13, mostraram melhor controle tumoral após radiação e mais células T CD8 ativas. Bloquear CXCL13 ou PD-L1 com anticorpos melhorou ainda mais o impacto da radiação em diversos modelos, apontando para uma cadeia clara desde o recrutamento de monócitos até a supressão das células T e falha do tratamento. 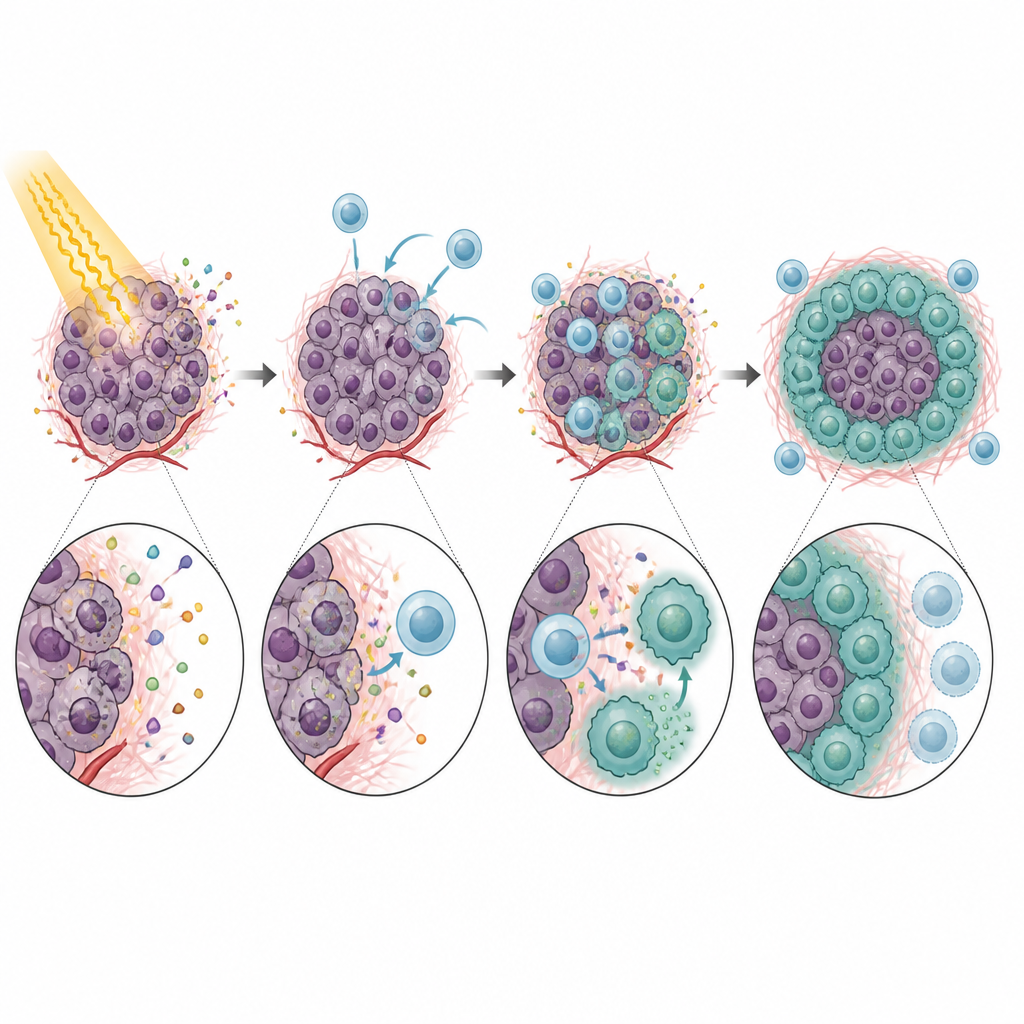
De supressores móveis a células de escudo estabelecidas
A história não terminou nos monócitos. Após entrar no tumor, muitos monócitos CXCR5-positivos amadureceram em macrófagos, outro tipo de célula imune. Sob influência de um fator de crescimento induzido pela radiação chamado GM-CSF, esses descendentes adquiriram características de macrófagos do tipo M2, conhecidos por atenuar respostas imunes e favorecer reparo tecidual. Esses macrófagos CXCR5-positivos eram ricos em PD-L1 e em outros genes ligados à supressão imune, sendo particularmente eficazes em bloquear a atividade das células T. Reduzir os níveis de GM-CSF ou interromper o eixo CXCL13–CXCR5 diminuiu o número desses macrófagos do tipo M2 e melhorou as respostas tumorais à radiação em camundongos.
Pistas de amostras de pacientes e possíveis novas estratégias
Para testar se processos semelhantes ocorrem em humanos, os pesquisadores examinaram conjuntos de dados públicos sobre câncer e amostras de pacientes submetidos à radioterapia. Tumores de pacientes que receberam radiação mostraram níveis mais altos de CXCR5, CD14 (um marcador humano de monócitos) e PD-L1. Em amostras de sangue, o número de monócitos aumentou após o tratamento em pacientes cujo quadro progrediu depois, mas não naqueles cujos tumores encolheram ou permaneceram estáveis. Em espécimes de câncer retal, tumores após radioterapia continham mais CXCL13 e monócitos e macrófagos positivos para CXCR5. Em cultura celular, monócitos humanos expostos a fluidos tumorais comportaram-se de maneira muito semelhante à observada em camundongos, ganhando CXCR5 por sinalização induzida por VEGF e expressando altos níveis de PD-L1.
Transformando uma vulnerabilidade em vantagem
No geral, este trabalho mostra que a radiação pode, involuntariamente, atrair e remodelar uma população de células imunes que protegem os tumores do próprio tratamento concebido para destruí-los. Ao aumentar CXCL13 nos tumores e a indução de CXCR5 por VEGF nos monócitos, a radiação cria um canal que fornece monócitos e macrófagos supressores, que então desligam as células T assassinas por meio de PD-L1. Em modelos murinos, interromper esse canal em vários pontos — como bloquear VEGF, CXCL13, GM-CSF ou PD-L1 — permitiu que a radiação atuasse de forma mais eficaz. Para pacientes, esses achados sugerem que combinar radioterapia com drogas imunológicas bem escolhidas pode reverter a balança em favor de uma resposta verdadeiramente antitumoral e melhorar o controle de longo prazo do câncer.
Citação: Lei, Y., Jia, R., Chen, C. et al. CXCR5+ monocyte emigration impairs the radiation-induced antitumor immune response. Nat Commun 17, 4258 (2026). https://doi.org/10.1038/s41467-026-70858-6
Palavras-chave: radioterapia, imunidade tumoral, monócitos, supressão imune, PD-L1