Clear Sky Science · he
הגרדיל של מונוציטים CXCR5+ מפחית את התגובה החיסונית לנשיאת הקרינה
כשטיפול בסרטן נלחם בעצמו
רדיותרפיה היא אבן יסוד בטיפול בסרטן ומשמשת ביותר ממחצית המטופלים. מטרת הטיפול היא לפגוע בתאי הגידול ולגייס את מערכת החיסון לסיים את המשימה. עם זאת, גידולים רבים חוזרים לאחר מהלך טיפול שנראה מוצלח. המחקר הזה חושף סיבה מפתיעה לכך: תאי חיסון מסוימים נמשכים אל הגידול אחרי הקרינה ובמקום לסייע להשמדתו, הם מגינים עליו. 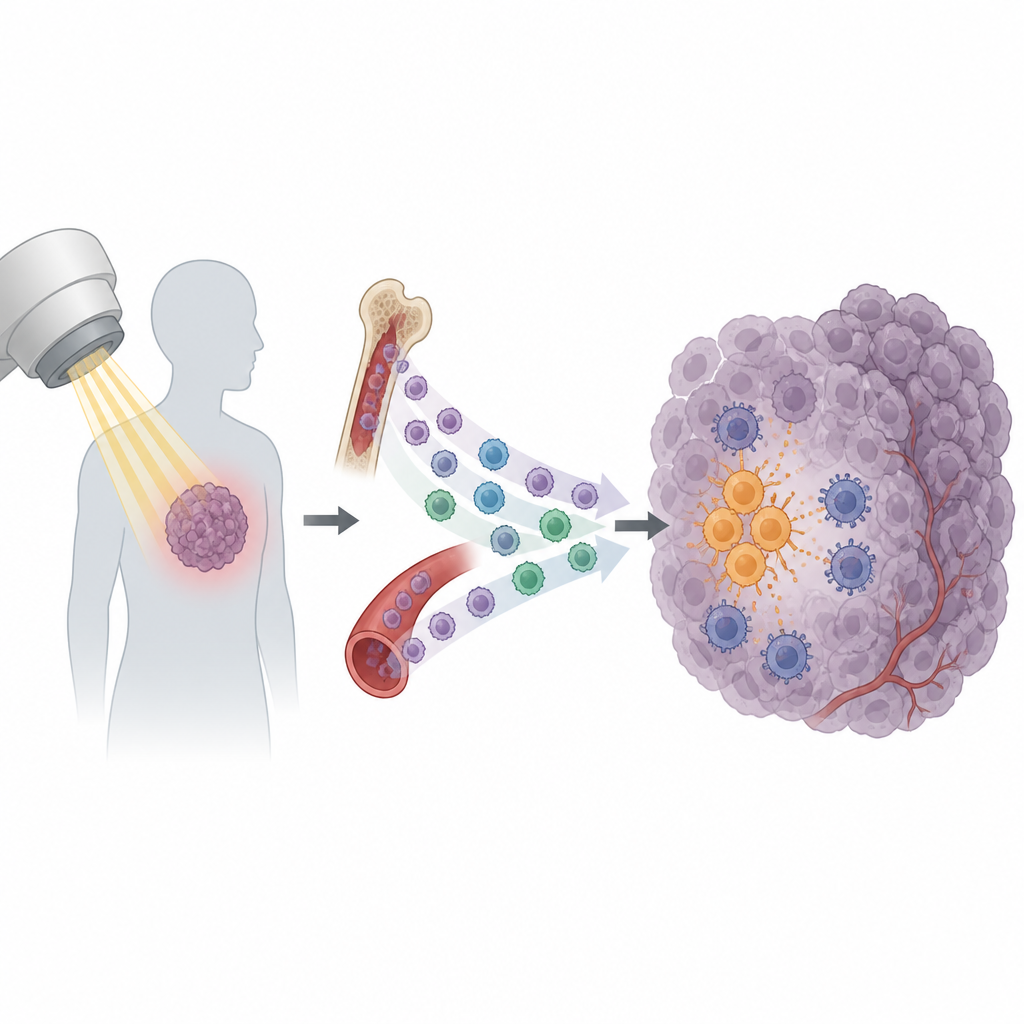
אפקט דו-חרבי של הקרינה
קרינה עושה יותר מפשוט לשבור DNA בתאי הסרטן. היא גם גורמת לגידול לשחרר גל של אותות שמזמינים תאי חיסון. חלק מהאותות הללו מסייעים להפעלת תאי T קוטלי-גידול, היכולים לזהות ולתקוף תאים סרטניים. אך אחרים נראים כמתנהגים באופן הפוך. החוקרים התמקדו בתת-קבוצה של תאים מעגלתיים שנקראים מונוציטים. בכמה מודלים עכבריים של גידול, הקרינה גרמה לעלייה חדה בחדירת מונוציטים אל הגידול, בעוד שסוגים אחרים של תאי דם לבנים השתנו במידה מועטה. דפוס זה רמז כי המונוציטים עשויים להיות שחקנים חשובים בקביעת רגישות או עמידות הגידול לקרינה.
שביל כימי שמפתה תאים מדכאים
בחינה מעמיקה יותר חשפה כי גידולים החשופים לקרינה מייצרים יותר מהאות הכימי CXCL13. מונוציטים הנושאים עליהם מולקולה מקבלת תואמת, CXCR5, היו בעלי סבירות גבוהה במיוחד להציף את הגידול אחרי הטיפול. עוד לפני שניתנה כל קרינה, הסרטן עצמו כבר הכין את התאים הללו מרחוק. תאי הגידול הפרישו למחזור הדם את גורם הצמיחה VEGF, שהפעיל שרשרת אותות בתוך המונוציטים הידועה כדרך PI3K–Akt–mTOR–HIF-1α. שינוי זה בתכנות הפנימי הגדיל את הביטוי של CXCR5 על פני השטח שלהם, ויצר למעשה מאגר מעגלי של מונוציטים חיוביים ל-CXCR5 מוכנים לעקוב אחרי שביל ה-CXCL13 אל הגידולים שהוקרו.
כיצד התאים המגויסים מעקרים את הקוטלים של הגידול
לאחר שהגיעו לתוך הגידול, מונוציטים חיוביים ל-CXCR5 לא פעלו כמגינים מועילים. במקום זאת, הם הגבילו בחוזקה את פעילות תאי CD8, אותם תאים הנדרשים כדי שמערכת החיסון תשמיד את הסרטן אחרי הקרינה. בניסויים במעבדה, מונוציטים אלה האטו את גדילת תאי ה-T והפחיתו את ייצור המולקולות ההתקפיות המרכזיות שלהם. האפקט תלוי במידה רבה ב-PD-L1, חלבון צ'ק-פוינט על המונוציטים שמתקשר עם PD-1 על תאי ה-T ומורה להם להשתתק. בעכברים חסרי CXCR5, או בגידולים חסרי CXCL13, נצפתה שליטה טובה יותר על הגידול אחרי הקרינה ופעילות מוגברת של תאי CD8. חסימת CXCL13 או PD-L1 בעזרת נוגדנים שיפרה עוד יותר את השפעת הקרינה בכמה מודלים, מה שמצביע על שרשרת ברורה ממגויסות המונוציטים לדיכוי תאי ה-T ולכישלון הטיפול. 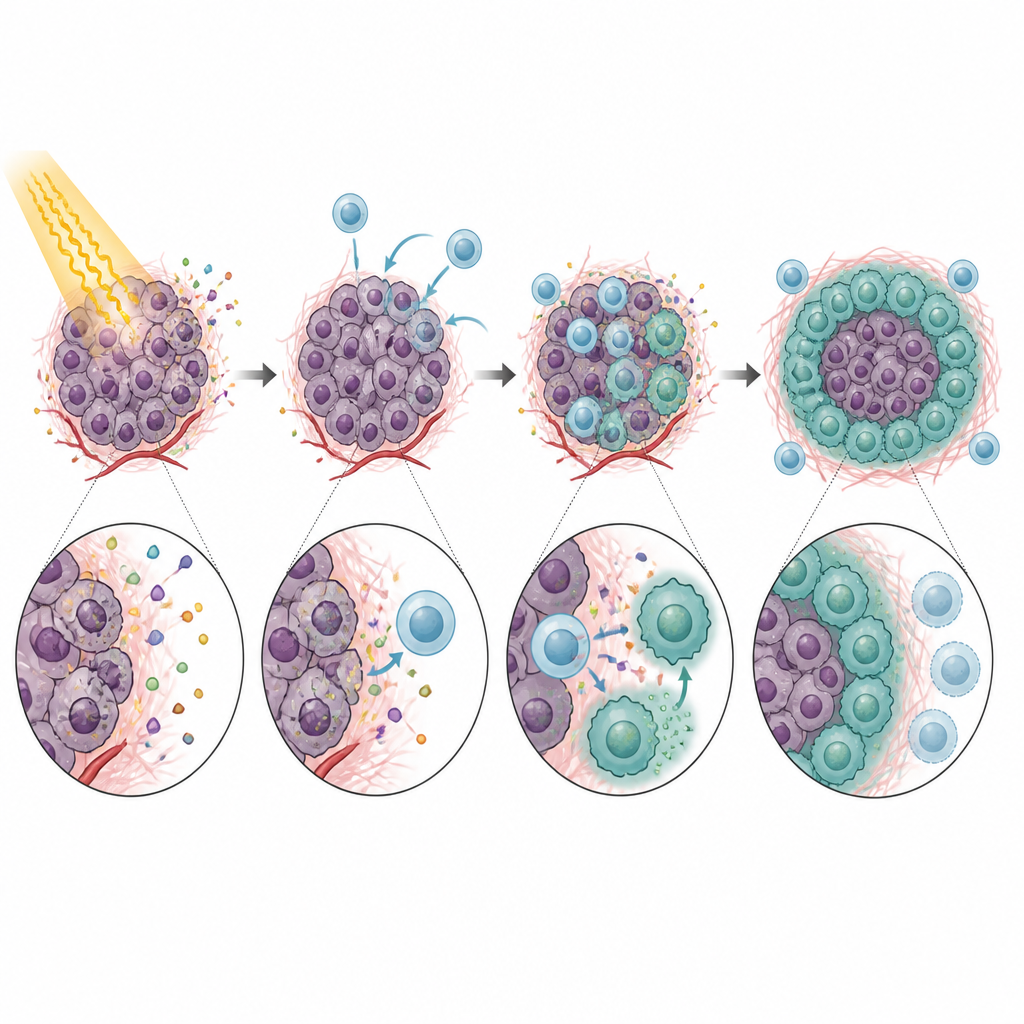
ממדכאים ניידים לתאי מגננה מושרשים
הסיפור לא הסתיים במונוציטים. לאחר כניסתם לגידול, רבים מהמונוציטים החיוביים ל-CXCR5 בגרו למקרופאגים, סוג נוסף של תאי חיסון. תחת השפעת גורם צמיחתי המיוצר בעקבות קרינה בשם GM-CSF, צאצאיהם לקחו על עצמם מאפיינים של מקרופאגים מדמויית M2, הידועים ביכולתם לדכא תגובות חיסוניות ולתמוך בתיקון רקמות. מקרופאגים חיוביים ל-CXCR5 אלו היו עשירים ב-PD-L1 ובגנים אחרים הקשורים לדיכוי חיסוני, והיו יעילים במיוחד בחסימת פעילות תאי ה-T. הקטנת רמות GM-CSF או שיבוש ציר CXCL13–CXCR5 הורידה את כמות המקרופאגים המדמות M2 ושיפרה את תגובת הגידול לקרינה בעכברים.
רמזים מדגימות מטופלים ואסטרטגיות אפשריות
כדי לבדוק האם תהליכים דומים מתרחשים בבני אדם, החוקרים בחנו מאגרי נתונים ציבוריים ודגימות ממטופלים המקבלים רדיותרפיה. בגידולים של מטופלים שעברו קרינה נמצאו רמות גבוהות יותר של CXCR5, CD14 (סמן מונוציטים אנושי) ו-PD-L1. בדגימות דם, מספר המונוציטים עלה אחרי הטיפול במטופלים שמחלתם התקדמה מאוחר יותר, אך לא אצל אלה שבהם הגידולים הצטמצמו או נשארו יציבים. בדגימות סרטן רקטלי, גידולים לאחר רדיותרפיה הכילו יותר CXCL13 ומונוציטים ומקרופאגים חיוביים ל-CXCR5. בתרבית תאים, מונוציטים אנושיים שנחשפו לנוזלי גידול התנהגו בדומה לאלה שבעכברים, והרוויחו ביטוי CXCR5 דרך איתות מונע VEGF והציגו רמות גבוהות של PD-L1.
להפוך חולשה ליתרון
בסך הכל, עבודה זו מראה כי הקרינה עלולה בשוגג לגייס ולעצב אוכלוסיית תאי חיסון שמגינה על הגידול מהטיפול שנועד להשמיד אותו. על ידי הגברה של CXCL13 בגידולים ושל ביטוי CXCR5 המונע על-ידי VEGF במונוציטים, הקרינה יוצרת צינור שמביא מונוציטים ומקרופאגים מדכאים, שמכבים בתורם את תאי הקטל באמצעות PD-L1. במודלים עכבריים, עצירת הצינור הזה בכמה נקודות — למשל על ידי חסימת VEGF, CXCL13, GM-CSF או PD-L1 — אפשרה לקרינה לפעול ביעילות רבה יותר. עבור מטופלים, ממצאים אלה מציעים כי צימוד רדיותרפיה עם תרופות חיסוניות ממוקדות שנבחרו בקפידה עשוי להטות את המאזניים חזרה לתגובה אנטי-גידולית אמיתית ולשפר את השליטה הארוכת-טווח בסרטן.
ציטוט: Lei, Y., Jia, R., Chen, C. et al. CXCR5+ monocyte emigration impairs the radiation-induced antitumor immune response. Nat Commun 17, 4258 (2026). https://doi.org/10.1038/s41467-026-70858-6
מילות מפתח: רדיותרפיה, חיסון נגד גידול, מונוציטים, דיכוי חיסוני, PD-L1