Clear Sky Science · tr
CXCR5+ monosit göçü, radyasyon kaynaklı antitumor bağışıklık yanıtını bozar
Tedavi Kanserle Savaşırken Kendi Kendine Karşı Çıkıyor
Radyasyon tedavisi, kanser bakımının temel taşlarından biridir ve hastaların yarısından fazlasında kullanılır. Amaç, tümör hücrelerine zarar verip bağışıklık sistemini işi bitirmeye teşvik etmektir. Yine de birçok tümör, görünürde başarılı bir tedavi sonrası geri döner. Bu çalışmada beklenmedik bir neden ortaya konuyor: belirli bağışıklık hücreleri radyasyon sonrası tümöre çekiliyor ve yok etmeye yardımcı olmak yerine kanseri koruyor. 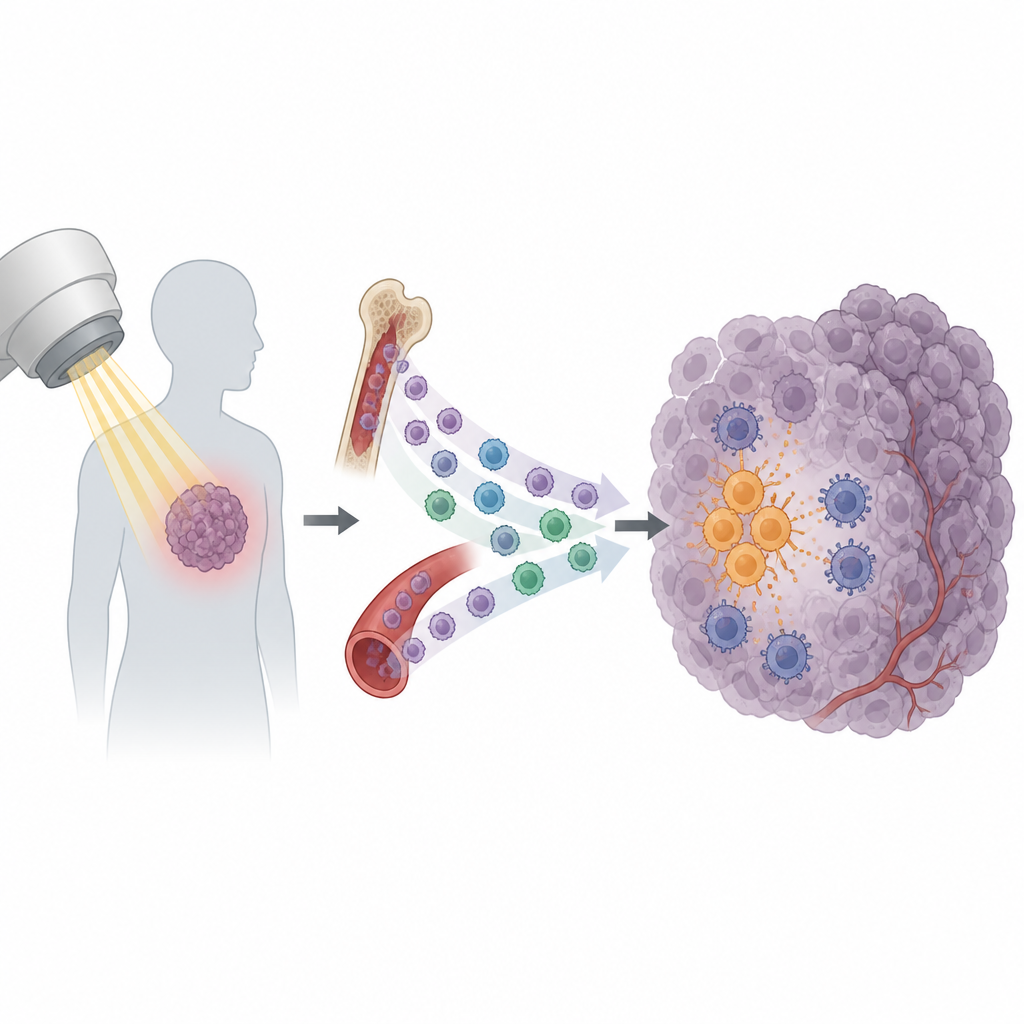
Radyasyonun İki Ucu Keskin Etkisi
Radyasyon sadece kanser hücrelerinin DNA’sını kırmaz. Aynı zamanda tümörlerin, bağışıklık hücrelerini çağıran bir dizi sinyal salmasına neden olur. Bu sinyallerden bazıları, tümör hücrelerini tanıyıp saldırabilecek sitotoksik T hücrelerini aktive etmeye yardım eder. Ancak diğerleri bunun tersine işlemiş görünür. Araştırmacılar, dolaşımdaki bağışıklık hücrelerinin bir alt grubu olan monositlere odaklandı. Birkaç fare tümör modelinde radyasyon, tümöre giren monosit sayısında keskin bir artışa yol açarken diğer beyaz kan hücresi tipleri pek değişmedi. Bu desen, monositlerin bir tümörün radyasyona duyarlı mı yoksa dirençli mi olacağı konusunda önemli oyuncular olabileceğini gösterdi.
Baskılayıcı Hücreleri Çeken Kimyasal Bir İz
Daha derine indiklerinde, araştırma ekibi radyasyona maruz kalan tümörlerin CXCL13 adında daha fazla kimyasal sinyal ürettiğini buldu. Eşleşen “alıcı” molekül CXCR5’i taşıyan monositler, tedavi sonrası özellikle tümöre akın etme eğilimindeydi. Herhangi bir radyasyon verilmeden önce bile, kanser bu hücreleri uzaktan hazırlamıştı. Tümör hücreleri VEGF büyüme faktörünü kana salgılıyor ve bu, monositler içinde PI3K, Akt, mTOR ve HIF-1α olarak bilinen bir sinyal zincirini etkinleştiriyordu. Bu içsel değişiklik, yüzeylerinde CXCR5 ifadesini artırarak CXCL13 izini takip etmeye hazır dolaşımdaki bir CXCR5-pozitif monosit rezervi oluşturdu.
İçeri Çekilen Hücreler Nasıl Tümör Katillerini Susturuyor
Tümör içine girdiklerinde, CXCR5-pozitif monositler yardımcı savunucular gibi davranmadı. Bunun yerine CD8 T hücrelerinin aktivitesini güçlü bir şekilde azalttılar; oysa bu hücreler radyasyon sonrası bağışıklığın kanseri temizlemesi için gereklidir. Laboratuvar testlerinde bu monositler T hücrelerinin çoğalmasını yavaşlattı ve kritik saldırı moleküllerinin üretimini azalttı. Etki büyük ölçüde monositlerin üzerindeki ve T hücrelerdeki PD-1 ile etkileşen bir kontrol noktası proteini olan PD-L1’e dayanıyordu. CXCR5’i olmayan fareler veya CXCL13’i olmayan tümörler, radyasyon sonrası daha iyi tümör kontrolü ve daha aktif CD8 T hücreleri gösterdi. CXCL13 veya PD-L1’i antikorlarla bloke etmek, birkaç modelde radyasyonun etkisini daha da artırdı ve monosit recrutmentinden T hücre baskılanmasına ve tedavi başarısızlığına kadar açık bir zinciri işaret etti. 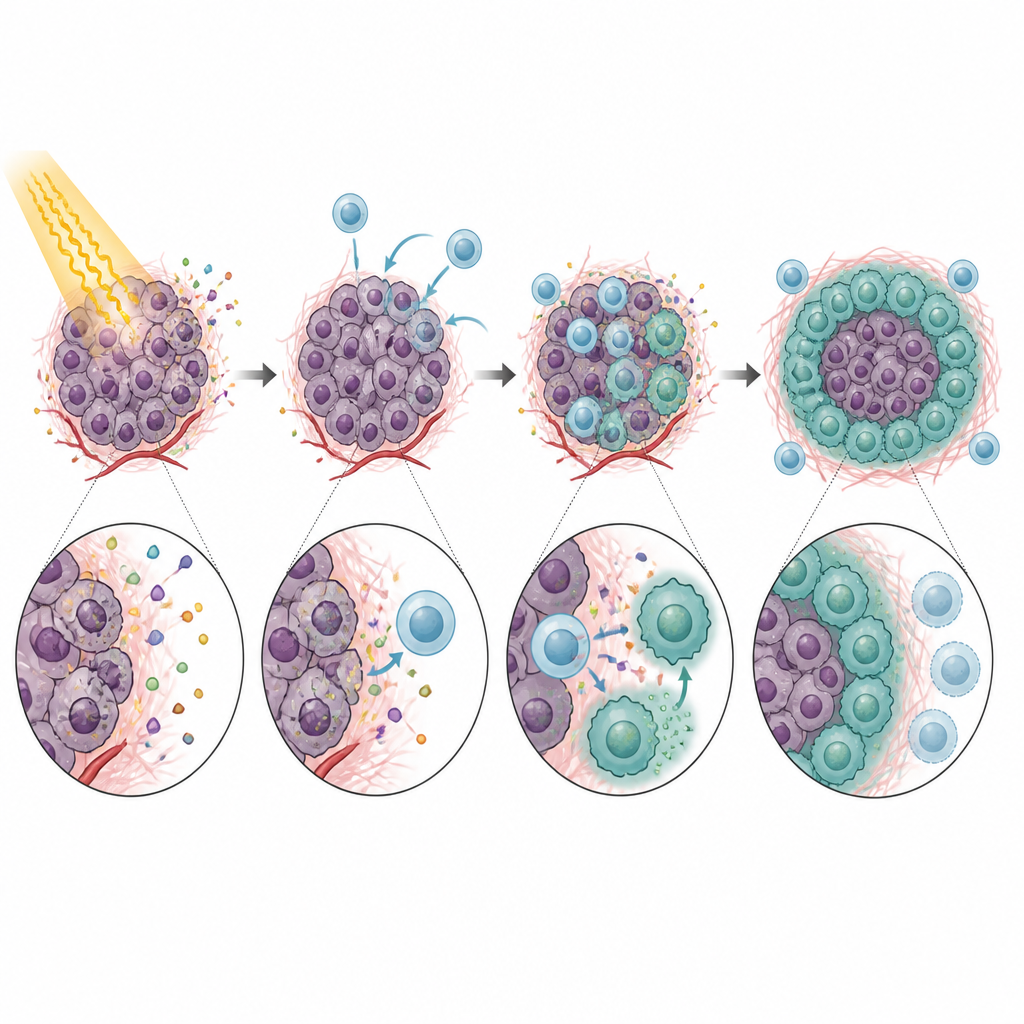
Hareketli Baskılayıcılardan Yerleşik Kalkan Hücrelere
Hikâye monositlerle bitmedi. Tümöre girdikten sonra birçok CXCR5-pozitif monosit, başka bir bağışıklık hücresi türü olan makrofajlara olgunlaştı. Radyasyonun tetiklediği bir büyüme faktörü olan GM-CSF etkisi altında, bu soylar M2-benzeri makrofaj özellikleri kazandı; bu tür makrofajlar bağışıklık yanıtlarını zayıflatmak ve doku onarımını desteklemekle bilinir. Bu CXCR5-pozitif makrofajlar PD-L1 ve bağışıklık baskılanmasıyla ilişkili diğer genler bakımından zengindi ve T hücresi aktivitelerini engellemede özellikle etkiliydiler. GM-CSF düzeylerini azaltmak veya CXCL13–CXCR5 eksenini bozmak, bu M2-benzeri makrofajların sayısını düşürdü ve farelerde radyasyona karşı tümör yanıtlarını iyileştirdi.
Hasta Örneklerinden İpuçları ve Olası Yeni Stratejiler
Aynı süreçlerin insanlarda da olup olmadığını test etmek için araştırmacılar halka açık kanser veri setlerini ve radyoterapi alan hastalardan alınan örnekleri inceledi. Radyasyon gören hastalardan alınan tümörlerde CXCR5, CD14 (insan monosit belirteci) ve PD-L1 seviyeleri daha yüksekti. Kan örneklerinde, hastalığı daha sonra ilerleyen hastalarda tedavi sonrası monosit sayıları artarken tümörü küçülen veya stabil kalanlarda bu artış görülmedi. Rektal kanser örneklerinde, radyoterapiden sonra tümörlerde daha fazla CXCL13 ve CXCR5-pozitif monosit ve makrofaj vardı. Hücre kültüründe, tümör sıvılarına maruz kalan insan monositleri farelerdekinin çok benzeri şekilde davrandı; VEGF kaynaklı sinyal yoluyla CXCR5 kazandılar ve yüksek PD-L1 ifade ettiler.
Zayıflığı Avantaja Çevirmek
Genel olarak bu çalışma, radyasyonun istemeden tümörü tedavi etmesi gereken işlemden koruyan bir bağışıklık hücresi popülasyonunu çağırıp yeniden şekillendirebildiğini gösteriyor. Tümörlerde CXCL13’i artırıp monositlerde VEGF kaynaklı CXCR5’i yükselterek, radyasyon baskılayıcı monosit ve makrofajları taşıyan bir hattı oluşturuyor; bunlar ardından PD-L1 yoluyla sitotoksik T hücrelerini kapatıyor. Fare modellerinde, VEGF, CXCL13, GM-CSF veya PD-L1’i bloke etmek gibi bu hattı birkaç noktadan kesmek, radyasyonun daha etkili çalışmasını sağladı. Hastalar için bu bulgular, radyoterapinin seçilmiş immün hedefli ilaçlarla eşleştirilmesinin antitumor yanıtı yeniden lehine çevirebileceğini ve kanserin uzun dönem kontrolünü iyileştirebileceğini düşündürüyor.
Atıf: Lei, Y., Jia, R., Chen, C. et al. CXCR5+ monocyte emigration impairs the radiation-induced antitumor immune response. Nat Commun 17, 4258 (2026). https://doi.org/10.1038/s41467-026-70858-6
Anahtar kelimeler: radyoterapi, tümör bağışıklığı, monositler, bağışıklık baskılanması, PD-L1