Clear Sky Science · ru
Эмиграция CXCR5+ моноцитов ослабляет радиационно-индуцированный антитуморный иммунный ответ
Когда лечение раком работает против самого себя
Лучевая терапия — один из краеугольных методов лечения рака, её применяют более чем у половины пациентов. Она направлена на повреждение клеток опухоли и мобилизацию иммунной системы для завершения уничтожения рака. Тем не менее многие опухоли рецидивируют после кажущегося успешным курса лечения. В этом исследовании выявлена неожиданная причина: после облучения в опухоль привлекаются определённые иммунные клетки, которые в итоге защищают рак, а не помогают его уничтожить. 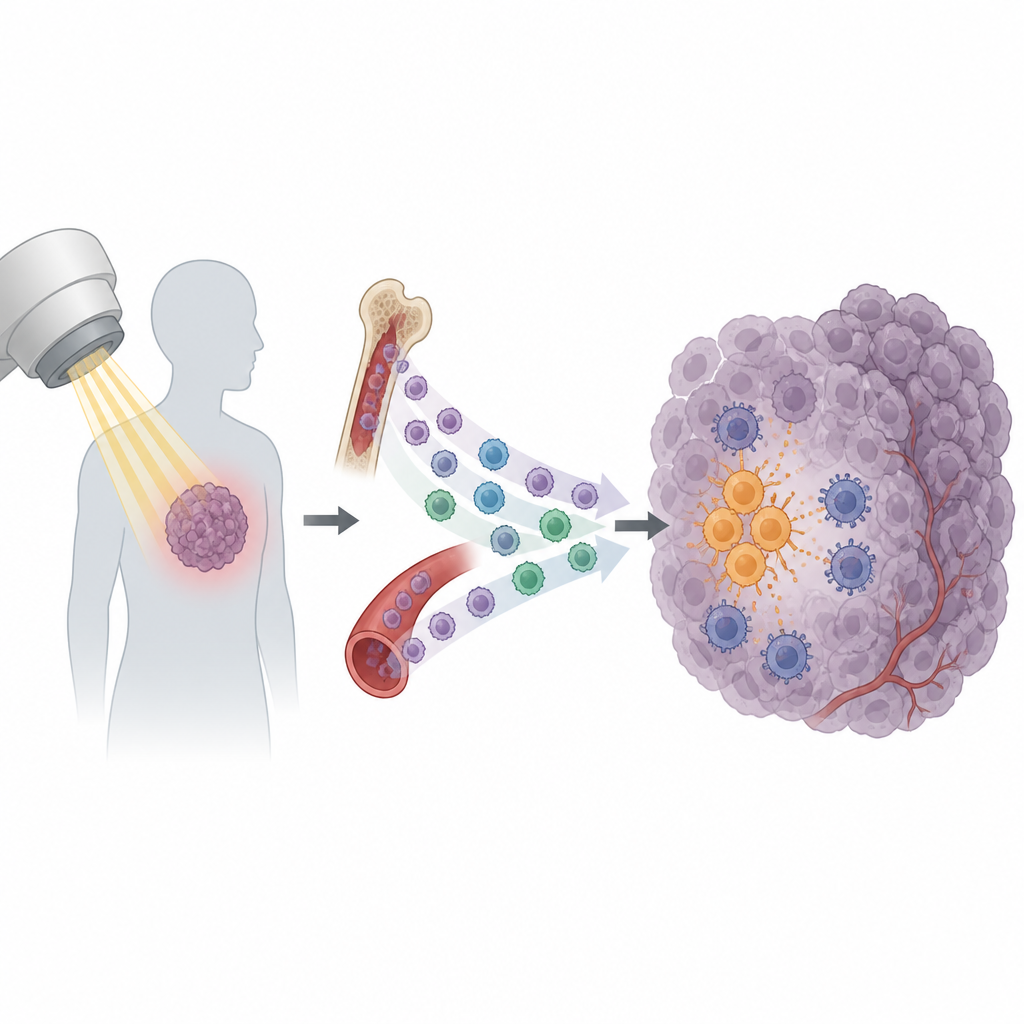
Двуострое действие облучения
Облучение делает не только одно — разрушает ДНК в раковых клетках. Оно также вызывает выброс сигналов со стороны опухоли, которые привлекают иммунные клетки. Некоторые из этих сигналов способствуют активации киллерных Т‑клеток, способных распознавать и атаковать опухоль. Но другие, напротив, имеют противоположный эффект. Исследователи сосредоточились на подмножестве циркулирующих иммунных клеток — моноцитах. В нескольких мышиных моделях опухолей облучение вызывало резкое увеличение притока моноцитов в опухоль, в то время как другие типы лейкоцитов изменялись мало. Такая картина указывала на возможную ключевую роль моноцитов в том, станет ли опухоль чувствительной или устойчивой к облучению.
Химическая дорожка, заманивающая супрессивные клетки
При более глубоком изучении команда обнаружила, что опухоли, подвергшиеся облучению, вырабатывали больше химического сигнала под названием CXCL13. Моноциты, несущие соответствующий «приёмник» CXCR5, особенно активно затекали в опухоль после лечения. Ещё до облучения сама опухоль уже подготовляла эти клетки на расстоянии. Опухолевые клетки секретировали фактор роста VEGF в кровоток, что запускало цепочку сигналов внутри моноцитов: PI3K, Akt, mTOR и HIF-1α. Эта внутренняя перестройка увеличивала экспрессию CXCR5 на поверхности моноцитов, фактически создавая циркулирующий резерв CXCR5‑положительных моноцитов, готовых следовать по тропе CXCL13 в облучённые опухоли.
Как привлечённые клетки заглушают киллеров опухоли
Попав в опухоль, CXCR5‑положительные моноциты не вели себя как помощники‑защитники. Напротив, они сильно тормозили активность CD8+ Т‑клеток — тех самых клеток, которые нужны иммунной системе для очищения опухоли после облучения. В лабораторных экспериментах эти моноциты замедляли пролиферацию Т‑клеток и снижали их продукцию ключевых атакующих молекул. Эффект во многом зависел от PD‑L1 — контрольного белка на моноцитах, который взаимодействует с PD‑1 на Т‑клетках и «приказывает» им притормозить. У мышей без CXCR5 или при отсутствии CXCL13 в опухолях наблюдался лучший контроль над опухолью после облучения и более активные CD8+ Т‑клетки. Блокирование CXCL13 или PD‑L1 антителами ещё более улучшало эффект радиации в нескольких моделях, что указывает на чёткую цепочку от рекрутинга моноцитов до подавления Т‑клеток и провала лечения. 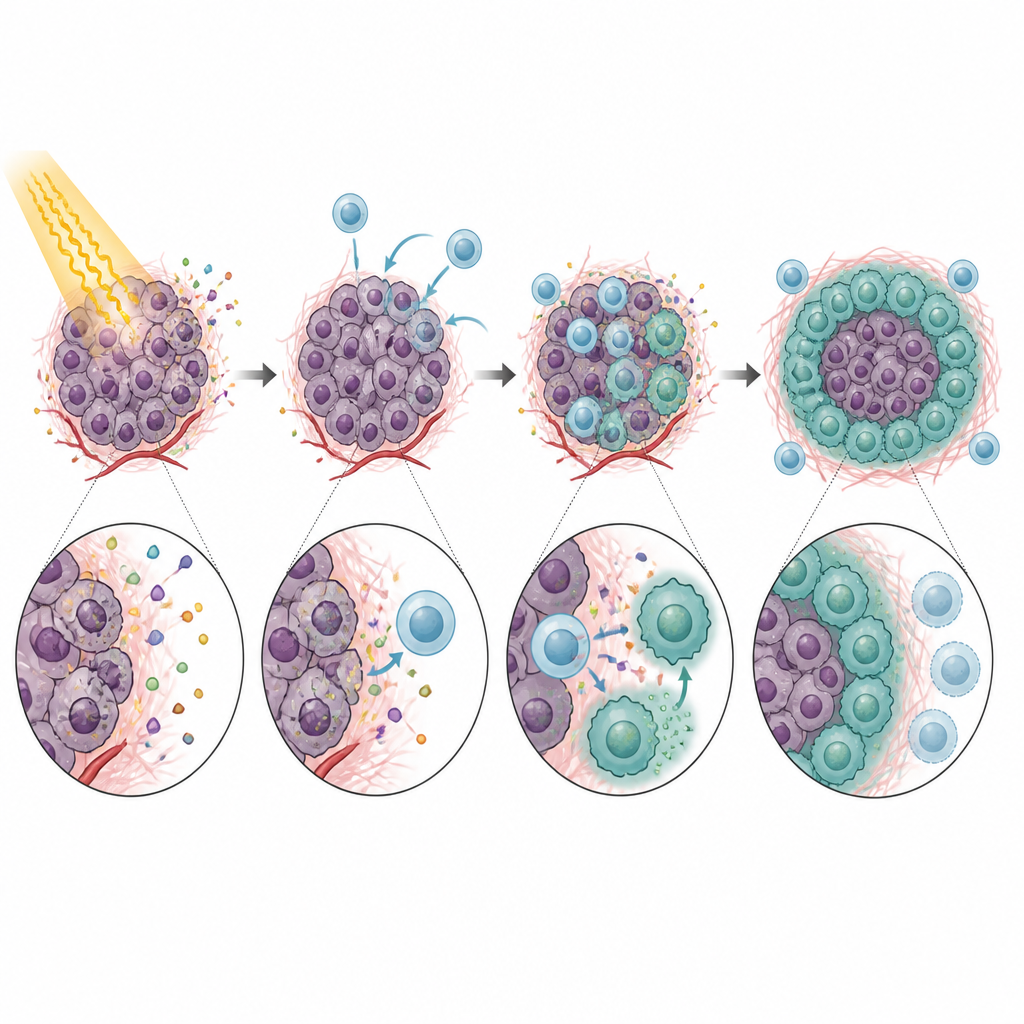
От подвижных супрессоров к осевшим защитным клеткам
История не ограничивалась моноцитами. Попав в опухоль, многие CXCR5‑положительные моноциты созревали в макрофаги — другой тип иммунных клеток. Под воздействием индуцируемого облучением фактора роста GM‑CSF их потомки приобретали признаки так называемых M2‑подобных макрофагов, известных своей способностью подавлять иммунные реакции и поддерживать заживление тканей. Эти CXCR5‑положительные макрофаги были богаты PD‑L1 и другими генами, связанными с иммунным подавлением, и особенно эффективно блокировали активность Т‑клеток. Снижение уровней GM‑CSF или нарушение оси CXCL13–CXCR5 уменьшало число таких M2‑подобных макрофагов и улучшало ответ опухолей на облучение у мышей.
Подсказки из образцов пациентов и возможные новые стратегии
Чтобы проверить, происходят ли похожие процессы у людей, исследователи проанализировали общедоступные онкологические датасеты и образцы пациентов, получавших радиотерапию. В опухолях пациентов после облучения отмечались повышенные уровни CXCR5, CD14 (маркер человеческих моноцитов) и PD‑L1. В образцах крови число моноцитов увеличивалось после лечения у пациентов, у которых затем болезнь прогрессировала, но не у тех, чьи опухоли уменьшались или оставались стабильными. В образцах ректального рака после радиотерапии в опухолях выявляли больше CXCL13 и CXCR5‑положительных моноцитов и макрофагов. В культурах человеческие моноциты, подвергшиеся воздействию опухолевых сред, вели себя похоже на мышиные: приобретали CXCR5 через VEGF‑опосредованную сигнализацию и высоко экспрессировали PD‑L1.
Преобразование слабости в преимущество
В целом работа показывает, что облучение может непреднамеренно привлекать и перекраивать популяцию иммунных клеток, которая защищает опухоли от самого лечения, предназначенного их уничтожить. За счёт повышения CXCL13 в опухолях и VEGF‑опосредованного увеличения CXCR5 в моноцитах облучение создаёт «конвейер», доставляющий супрессивные моноциты и макрофаги, которые затем выключают киллерные Т‑клетки через PD‑L1. В мышиных моделях прерывание этого конвейера на разных уровнях — например, блокирование VEGF, CXCL13, GM‑CSF или PD‑L1 — позволяло радиации действовать эффективнее. Для пациентов эти результаты подразумевают, что сочетание радиотерапии с целенаправленными иммунными препаратами может вернуть преимущество антитуморному ответу и улучшить длительный контроль над раком.
Цитирование: Lei, Y., Jia, R., Chen, C. et al. CXCR5+ monocyte emigration impairs the radiation-induced antitumor immune response. Nat Commun 17, 4258 (2026). https://doi.org/10.1038/s41467-026-70858-6
Ключевые слова: радиотерапия, опухолевый иммунитет, моноциты, иммунное подавление, PD-L1