Clear Sky Science · it
La migrazione dei monociti CXCR5+ compromette la risposta antitumorale indotta dalle radiazioni
Quando il trattamento contro il cancro si ritorce contro se stesso
La radioterapia è una pietra miliare nella cura del cancro, impiegata in più della metà dei pazienti. È pensata per danneggiare le cellule tumorali e mobilitare il sistema immunitario per completare il lavoro. Eppure molti tumori ricrescono dopo un ciclo di trattamento apparentemente riuscito. Questo studio svela una ragione sorprendente: dopo la radioterapia, alcuni tipi di cellule immunitarie vengono richiamati nel tumore e finiscono per proteggerlo invece di aiutarne la distruzione. 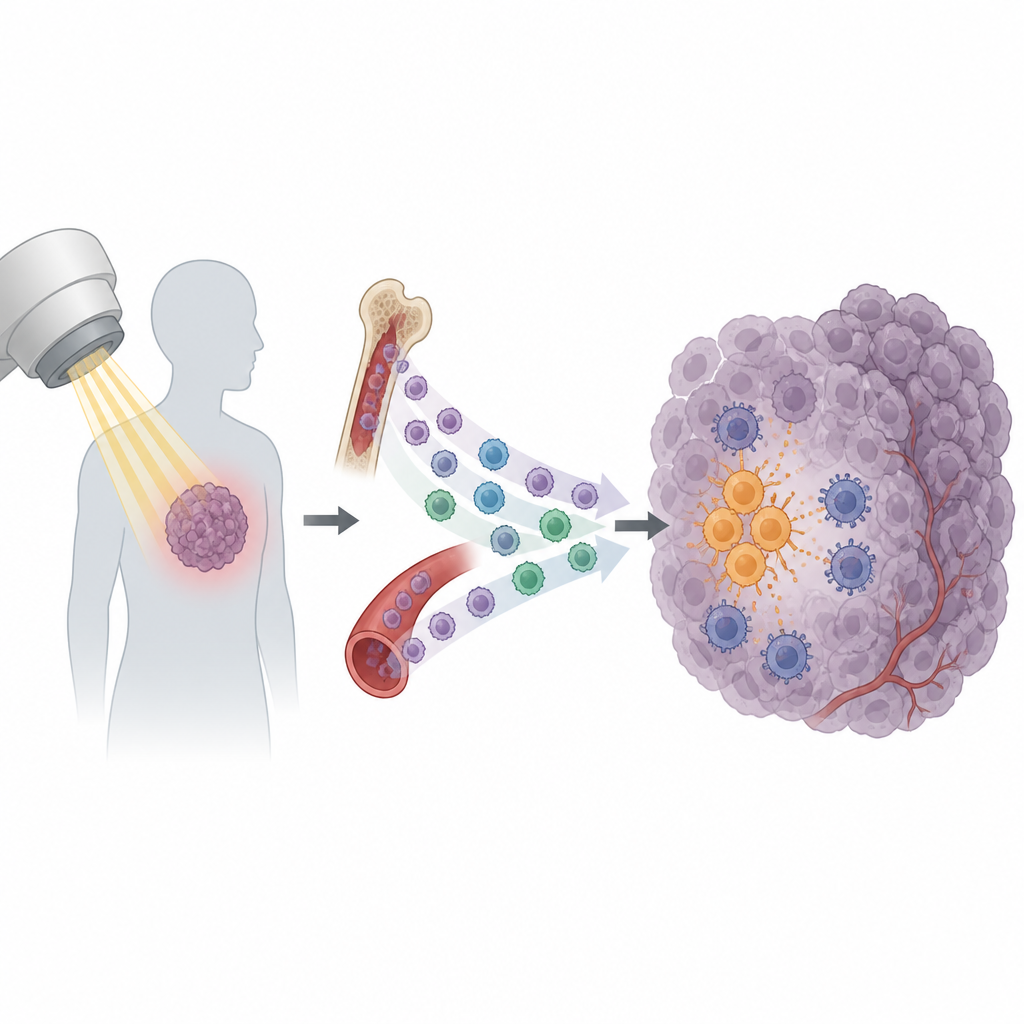
Un effetto a doppio taglio delle radiazioni
Le radiazioni non si limitano a rompere il DNA delle cellule tumorali. Inducono anche il rilascio da parte dei tumori di una raffica di segnali che richiamano cellule immunitarie. Alcuni di questi segnali favoriscono l’attivazione delle cellule T citotossiche, che possono riconoscere e attaccare le cellule tumorali. Ma altri sembrano avere l’effetto opposto. I ricercatori si sono concentrati su una sottopopolazione di cellule circolanti chiamate monociti. In diversi modelli murini di tumore, la radioterapia ha causato un netto aumento dei monociti che entrano nel tumore, mentre altri tipi di globuli bianchi sono cambiati di poco. Questo schema suggeriva che i monociti potessero essere attori chiave nel determinare se un tumore diventasse sensibile o resistente alla radioterapia.
Una scia chimica che attira cellule soppressive
Approfondendo, il gruppo ha scoperto che i tumori esposti alle radiazioni producevano più del segnale chimico CXCL13. I monociti che esprimono il recettore corrispondente, CXCR5, erano particolarmente inclini a invadere il tumore dopo il trattamento. Prima della radioterapia, il tumore aveva già predisposto questi monociti a distanza. Le cellule tumorali secernono il fattore di crescita VEGF nel circolo sanguigno, che attiva una cascata di segnali all’interno dei monociti nota come via PI3K–Akt–mTOR–HIF-1α. Questo cambiamento interno aumenta l’espressione di CXCR5 sulla loro superficie, creando di fatto una riserva circolante di monociti CXCR5-positivi pronta a seguire la scia di CXCL13 nei tumori irradiati.
Come le cellule reclutate zittiscono i killer tumorali
Una volta nel tumore, i monociti CXCR5-positivi non si comportavano come difensori utili. Al contrario, limitarono fortemente l’attività delle cellule T CD8, proprio quelle necessarie affinché il sistema immunitario elimini il cancro dopo le radiazioni. In test in vitro questi monociti rallentavano la proliferazione delle T e ne riducevano la produzione di molecole d’attacco chiave. L’effetto dipendeva in larga misura da PD-L1, una proteina checkpoint presente sui monociti che si lega a PD-1 sulle T e le induce a fermarsi. Topi privi di CXCR5, o tumori privi di CXCL13, mostravano un migliore controllo tumorale dopo radioterapia e T CD8 più attive. L’utilizzo di anticorpi per bloccare CXCL13 o PD-L1 migliorava ulteriormente l’efficacia della radioterapia in diversi modelli, delineando una catena chiara dal reclutamento dei monociti alla soppressione delle T e al fallimento del trattamento. 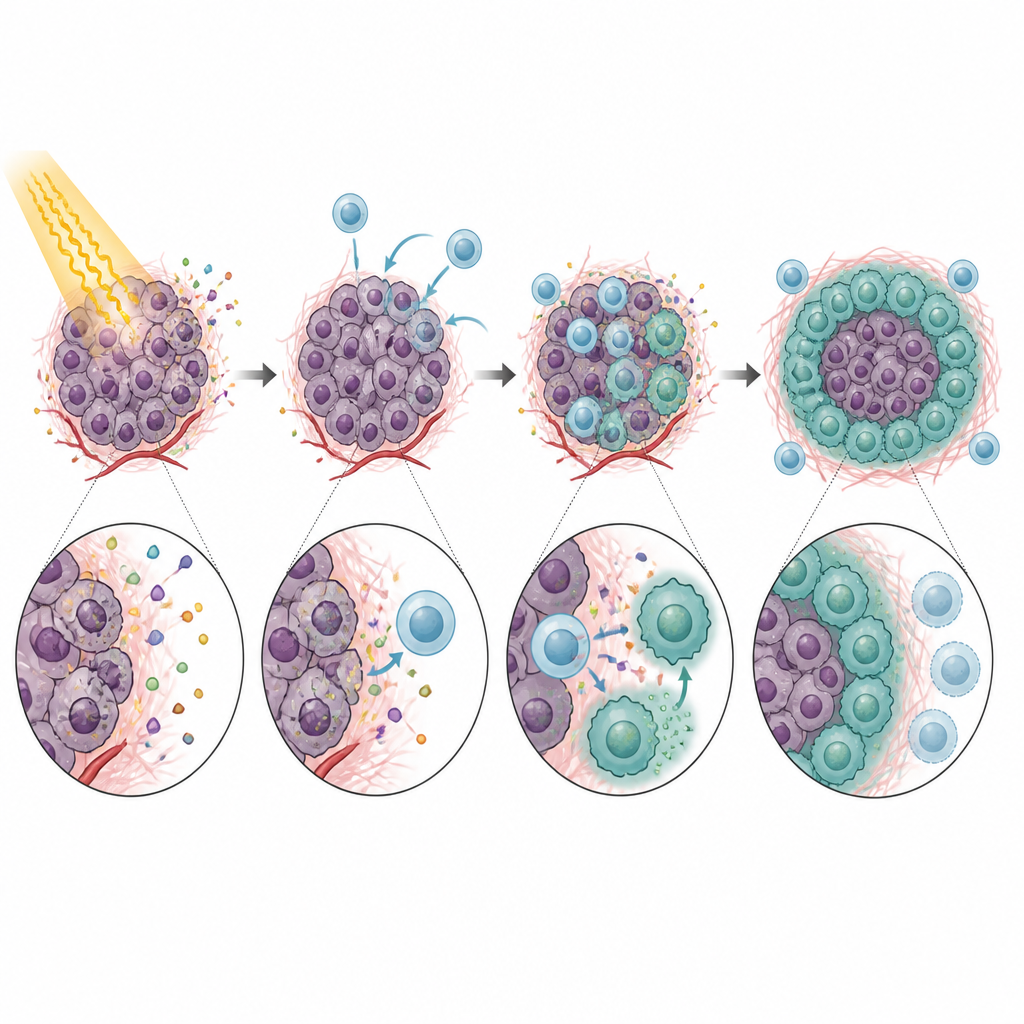
Da soppressori mobili a cellule scudo stabili
La storia non finisce con i monociti. Dopo essere entrati nel tumore, molti monociti CXCR5-positivi maturarono in macrofagi, un altro tipo di cellula immunitaria. Sotto l’influsso di un fattore di crescita indotto dalle radiazioni, GM-CSF, questi discendenti acquisirono caratteristiche di macrofagi di tipo M2, noti per attenuare le risposte immunitarie e favorire la riparazione dei tessuti. Questi macrofagi CXCR5-positivi erano ricchi di PD-L1 e di altri geni associati alla soppressione immunitaria, e risultavano particolarmente efficaci nel bloccare l’attività delle T. Ridurre i livelli di GM-CSF o interrompere l’asse CXCL13–CXCR5 diminuiva il numero di questi macrofagi di tipo M2 e migliorava la risposta tumorale alle radiazioni nei topi.
Indizi dai campioni dei pazienti e possibili nuove strategie
Per verificare se processi simili avvengono negli esseri umani, i ricercatori hanno esaminato dataset pubblici sul cancro e campioni di pazienti sottoposti a radioterapia. I tumori di pazienti trattati con radiazioni mostravano livelli più elevati di CXCR5, CD14 (un marcatore dei monociti umani) e PD-L1. Nel sangue, il numero di monociti aumentava dopo il trattamento nei pazienti la cui malattia poi progrediva, ma non in quelli i cui tumori si riducevano o restavano stabili. Nei campioni di cancro rettale, i tumori post-radioterapia contenevano più CXCL13 e più monociti e macrofagi CXCR5-positivi. In colture cellulari, i monociti umani esposti ai liquidi tumorali si comportavano in modo simile a quanto osservato nei topi, acquisendo CXCR5 tramite segnali indotti da VEGF ed esprimendo alti livelli di PD-L1.
Trasformare una debolezza in un vantaggio
Complessivamente, questo lavoro mostra che la radioterapia può involontariamente richiamare e rimodellare una popolazione di cellule immunitarie che proteggono il tumore dallo stesso trattamento pensato per distruggerlo. Aumentando CXCL13 nei tumori e il CXCR5 nei monociti tramite VEGF, la radioterapia crea una linea di approvvigionamento che porta monociti e macrofagi soppressivi, i quali poi disattivano le cellule T killer attraverso PD-L1. Nei modelli murini, interrompere questa catena in diversi punti — ad esempio bloccando VEGF, CXCL13, GM-CSF o PD-L1 — ha permesso alla radioterapia di funzionare meglio. Per i pazienti, questi risultati suggeriscono che associare la radioterapia con farmaci immunoterapici mirati potrebbe riportare l’equilibrio verso una vera risposta antitumorale e migliorare il controllo a lungo termine del cancro.
Citazione: Lei, Y., Jia, R., Chen, C. et al. CXCR5+ monocyte emigration impairs the radiation-induced antitumor immune response. Nat Commun 17, 4258 (2026). https://doi.org/10.1038/s41467-026-70858-6
Parole chiave: radioterapia, immunità tumorale, monociti, soppressione immunitaria, PD-L1