Clear Sky Science · pl
CXCR5+ emigracja monocytów osłabia promieniowaniem wywołaną odpowiedź immunologiczną przeciwnowotworową
Kiedy leczenie nowotworu działa przeciwko sobie
Radioterapia jest podstawą leczenia nowotworów i stosuje się ją u ponad połowy pacjentów. Ma na celu uszkodzenie komórek guza oraz pobudzenie układu odpornościowego do dokończenia zadania. Mimo to wiele guzów odradza się po pozornie udanej terapii. To badanie odkrywa zaskakującą przyczynę: po naświetlaniu do guza napływają pewne komórki odpornościowe, które zamiast pomagać w jego zniszczeniu, zaczynają go chronić. 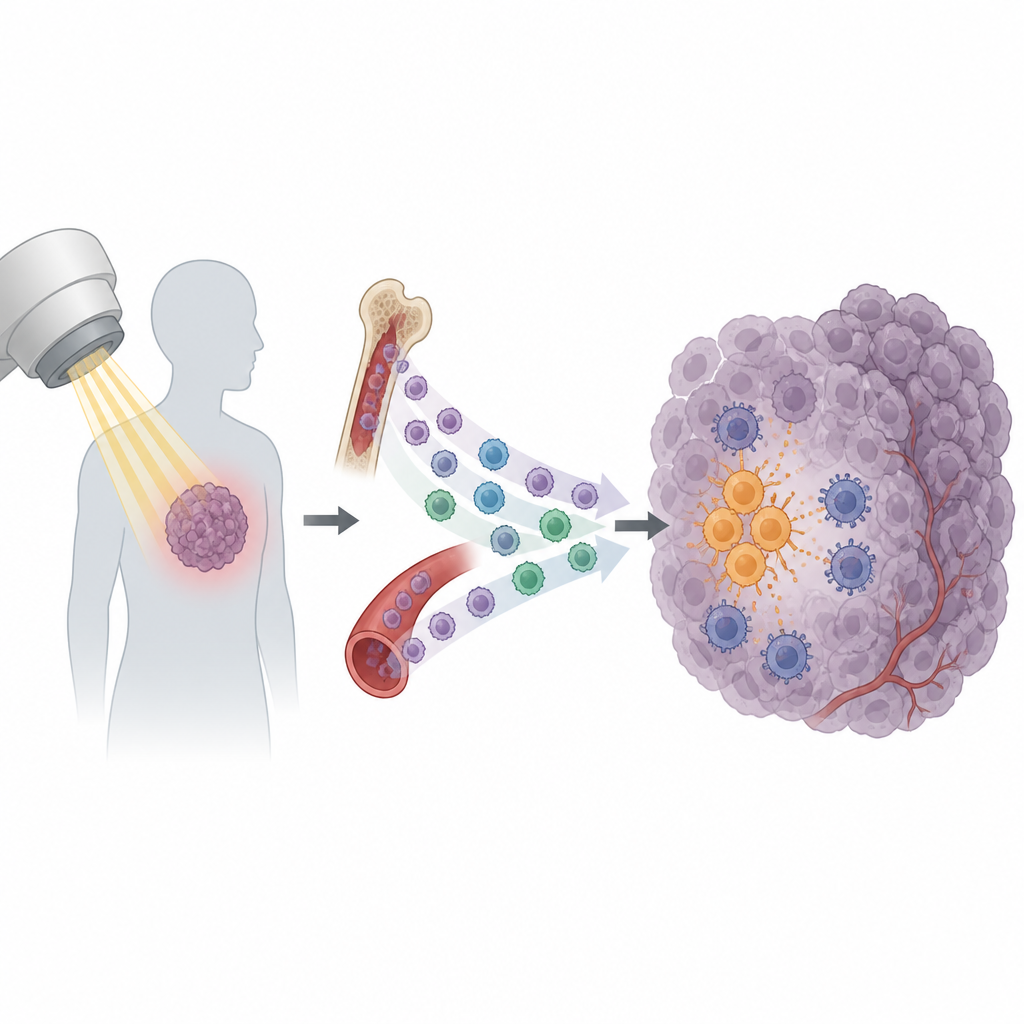
Obosieczny efekt promieniowania
Promieniowanie robi więcej niż tylko łamie DNA w komórkach nowotworowych. Powoduje też, że guzy uwalniają falę sygnałów przyciągających komórki odpornościowe. Część tych sygnałów pomaga aktywować komórki T zabójcze, które rozpoznają i atakują komórki guza. Inne jednak działają odwrotnie. Naukowcy skupili się na podzbiorze krążących komórek odpornościowych zwanych monocytami. W kilku modelach mysimy promieniowanie wywołało gwałtowny napływ monocytów do guza, podczas gdy inne typy białych krwinek zmieniały się niewiele. Ten wzorzec sugerował, że monocyty mogą odgrywać ważną rolę w tym, czy guz stanie się wrażliwy czy oporny na promieniowanie.
Chemiczny szlak przywabiający komórki supresorowe
Pogłębiając badania, zespół odkrył, że guzy po napromieniowaniu wytwarzały więcej sygnału chemicznego zwanego CXCL13. Monocyty niosące pasujący „odbiornik” CXCR5 były szczególnie skłonne napływać do guza po terapii. Jeszcze przed podaniem promieniowania sam guz przygotowywał te komórki z daleka. Komórki nowotworowe wydzielały czynnik wzrostu VEGF do krwiobiegu, co uruchamiało kaskadę sygnałów w monocytach znaną jako szlak PI3K–Akt–mTOR–HIF-1α. Ta wewnętrzna zmiana zwiększała ekspresję CXCR5 na ich powierzchni, tworząc w efekcie krążący zapas monocytów pozytywnych dla CXCR5 gotowych podążyć za śladem CXCL13 do naświetlonych guzów.
Jak zrekrutowane komórki wyciszają zabójców guza
Po wejściu do guza monocyty CXCR5+ nie zachowywały się jak pomocnicy. Zamiast tego silnie hamowały aktywność komórek CD8 T, czyli tych, które są potrzebne, aby układ odpornościowy oczyścił nowotwór po promieniowaniu. W testach laboratoryjnych te monocyty spowalniały proliferację limfocytów T i zmniejszały produkcję kluczowych cząsteczek ataku. Efekt ten w dużej mierze zależał od PD-L1 — białka hamującego na monocytach, które wiąże się z PD-1 na komórkach T i sygnalizuje im ustąpienie. Myszy pozbawione CXCR5 lub guzy bez CXCL13 wykazywały lepszą kontrolę guza po radioterapii i bardziej aktywne komórki CD8 T. Blokada CXCL13 lub PD-L1 przeciwciałami dodatkowo poprawiała efekt promieniowania w kilku modelach, wskazując na jasny ciąg od rekrutacji monocytów do supresji komórek T i niepowodzenia leczenia. 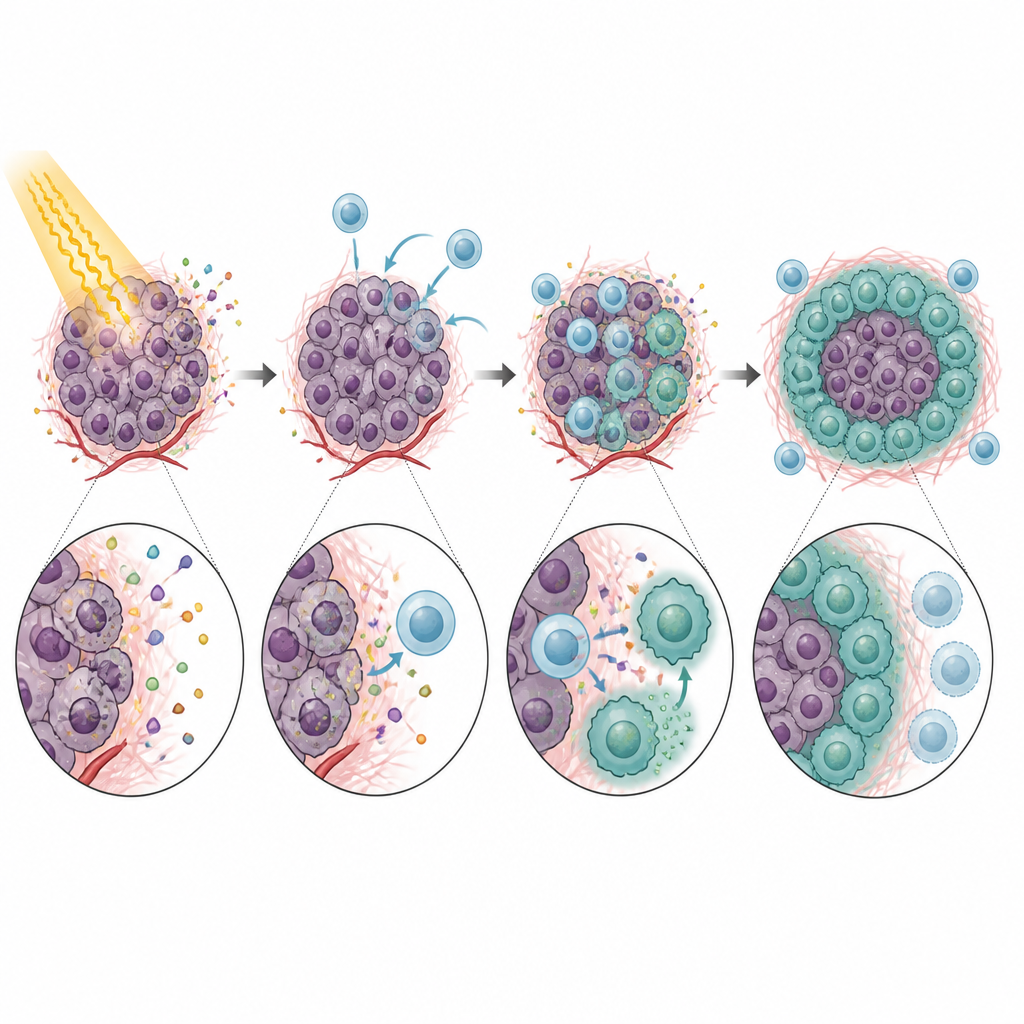
Od mobilnych supresorów do osiadłych komórek osłonowych
Na tym historia się nie kończyła. Po wejściu do guza wiele monocytów CXCR5+ dojrzewało w makrofagi — inny typ komórek odpornościowych. Pod wpływem czynnika wzrostu wywołanego promieniowaniem, GM-CSF, ich potomkowie przyjmowali cechy tzw. makrofagów podobnych do M2, które są znane z tłumienia odpowiedzi immunologicznych i wspierania naprawy tkanek. Te makrofagi CXCR5+ obfitowały w PD-L1 i inne geny związane z supresją immunologiczną i były szczególnie skuteczne w blokowaniu aktywności komórek T. Obniżenie poziomu GM-CSF lub zakłócenie osi CXCL13–CXCR5 zmniejszało liczbę tych makrofagów podobnych do M2 i poprawiało odpowiedź guza na promieniowanie u myszy.
Wskazówki z próbek pacjentów i możliwe nowe strategie
Aby sprawdzić, czy podobne procesy zachodzą u ludzi, badacze przeanalizowali publicznie dostępne zbiory danych onkologicznych oraz próbki od pacjentów poddanych radioterapii. Guzy pacjentów po naświetlaniu wykazywały wyższe poziomy CXCR5, CD14 (ludzki marker monocytów) i PD-L1. We krwi liczba monocytów wzrastała po leczeniu u pacjentów, u których choroba później postępowała, ale nie u tych, których guzy zmniejszyły się lub pozostały stabilne. W próbkach raka odbytnicy po radioterapii stwierdzono więcej CXCL13 oraz monocytów i makrofagów pozytywnych dla CXCR5. W hodowlach in vitro ludzkie monocyty wystawione na działanie płynów guza zachowywały się podobnie jak u myszy, zyskując CXCR5 dzięki sygnalizacji napędzanej przez VEGF i wykazując wysoką ekspresję PD-L1.
Przekształcanie słabości w zaletę
W całości praca ta pokazuje, że promieniowanie może niezamierzenie przyciągać i przekształcać populację komórek odpornościowych, które chronią guz przed terapią, która ma go zniszczyć. Poprzez zwiększenie CXCL13 w guzie oraz VEGF‑zależnego CXCR5 w monocytach, radioterapia tworzy „rurę” dostarczającą supresyjne monocyty i makrofagi, które następnie wyłączają komórki zabójcze poprzez PD-L1. W modelach mysich przerywanie tej drogi na różnych etapach, na przykład blokada VEGF, CXCL13, GM-CSF lub PD-L1, pozwalało promieniowaniu działać skuteczniej. Dla pacjentów wyniki te sugerują, że łączenie radioterapii z odpowiednio dobranymi lekami celującymi w układ odpornościowy może przywrócić przewagę odpowiedzi przeciwnowotworowej i poprawić długoterminową kontrolę choroby.
Cytowanie: Lei, Y., Jia, R., Chen, C. et al. CXCR5+ monocyte emigration impairs the radiation-induced antitumor immune response. Nat Commun 17, 4258 (2026). https://doi.org/10.1038/s41467-026-70858-6
Słowa kluczowe: radioterapia, odporność przeciwnowotworowa, monocyty, supresja immunologiczna, PD-L1