Clear Sky Science · nl
CXCR5+ monocytenmigratie schaadt de door bestraling geïnduceerde antitumorimmuunrespons
Wanneer kankerbehandeling tegen zichzelf werkt
Bestraling is een hoeksteen van de kankerzorg en wordt bij meer dan de helft van alle patiënten ingezet. Het is bedoeld om tumorcellen te beschadigen en het immuunsysteem op te roepen om het werk af te maken. Toch komen veel tumoren terug na een ogenschijnlijk succesvolle behandeling. Deze studie onthult een verrassende reden: bepaalde immuuncellen worden na bestraling naar de tumor geroepen en eindigen met het afschermen van de kanker in plaats van deze te helpen vernietigen. 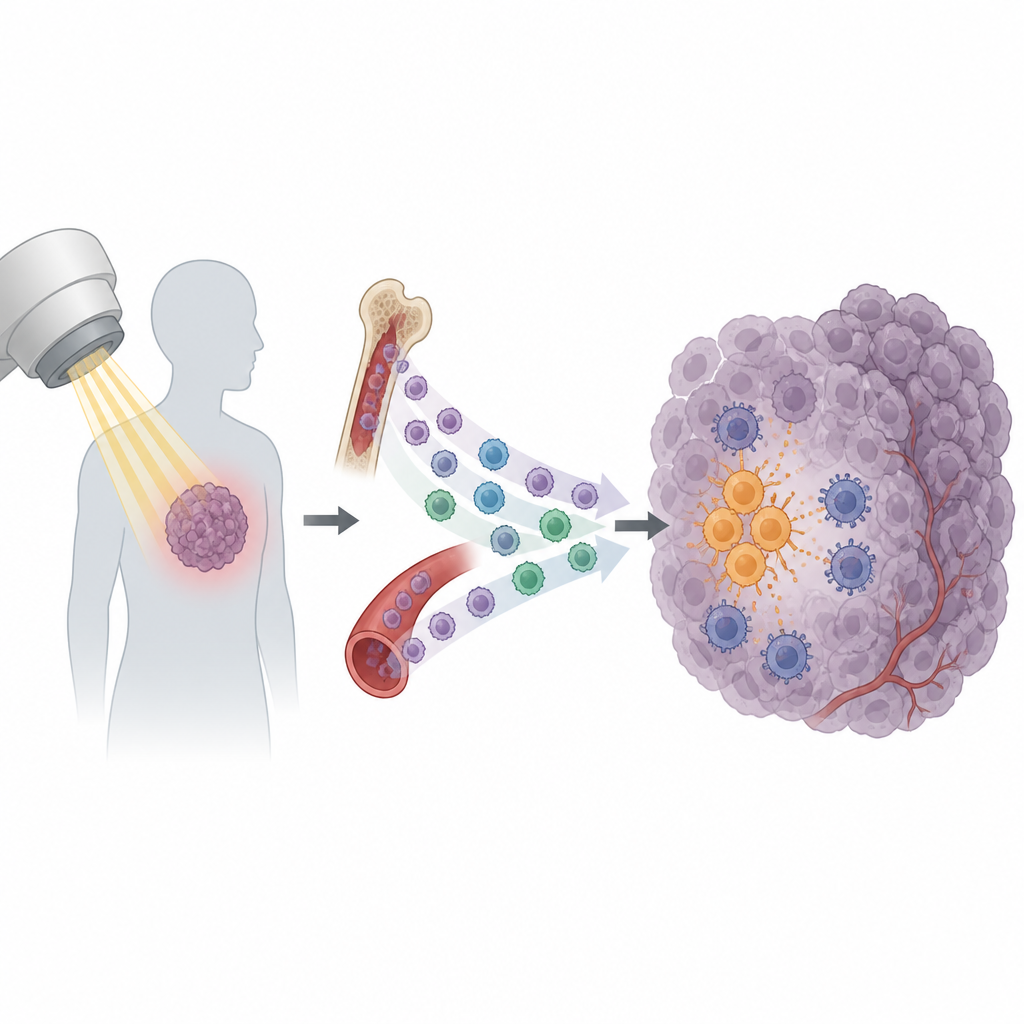
Een tweeërlei effect van bestraling
Bestraling doet meer dan alleen het breken van DNA in kankercellen. Het veroorzaakt ook dat tumoren een uitbarsting van signalen afgeven die immuuncellen aantrekken. Sommige van die signalen helpen bij het activeren van CD8-killercellen, die tumorcellen kunnen herkennen en aanvallen. Maar andere signalen lijken het tegenovergestelde effect te hebben. De onderzoekers richtten zich op een subset van circulerende immuuncellen, monocyten. In meerdere muizen-tumormodellen zorgde bestraling voor een sterke toename van monocyten die de tumor binnendrongen, terwijl andere typen witte bloedcellen weinig veranderden. Dit patroon suggereerde dat monocyten belangrijke spelers kunnen zijn bij de vraag of een tumor gevoelig of resistent wordt voor bestraling.
Een chemisch spoor dat onderdrukkende cellen lokt
Dieper graven liet zien dat aan bestraling blootgestelde tumoren meer van het chemische signaal CXCL13 produceerden. Monocyten die het bijpassende "ontvanger"molecuul CXCR5 dragen, waren bijzonder geneigd om na behandeling de tumor binnen te stromen. Voordat enige bestraling werd toegediend, had de kanker deze cellen op afstand al voorbereid. Tumorcellen scheidden de groeifactor VEGF in het bloed uit, die een keten van signalen in monocyten activeerde, bekend als het PI3K–Akt–mTOR–HIF-1α-pad. Deze interne veranderingen verhoogden CXCR5 op hun oppervlak en creëerden zo een circulerende reserve van CXCR5-positieve monocyten die klaar waren het CXCL13-spoor naar bestraalde tumoren te volgen.
Hoe gerekruteerde cellen tumorkillers tot zwijgen brengen
Eens in de tumor gedroegen CXCR5-positieve monocyten zich niet als behulpzame verdedigers. In plaats daarvan remden zij sterk de activiteit van CD8-T-cellen, de cellen die nodig zijn om kanker na bestraling te elimineren. In laboratoriumtests vertraagden deze monocyten de T-celproliferatie en verminderden ze de productie van belangrijke aanvalsmoleculen. Het effect berustte grotendeels op PD-L1, een remmend controle-eiwit op de monocyten dat PD-1 op T-cellen activeert en die cellen tot stilte maant. Muizen zonder CXCR5, of tumoren zonder CXCL13, toonden betere tumorcontrole na bestraling en actiever CD8-T-cellen. Het blokkeren van CXCL13 of PD-L1 met antilichamen versterkte in meerdere modellen het effect van bestraling, wat wijst op een duidelijke keten van monocytenrekrutering naar T-celonderdrukking en behandelingsfalen. 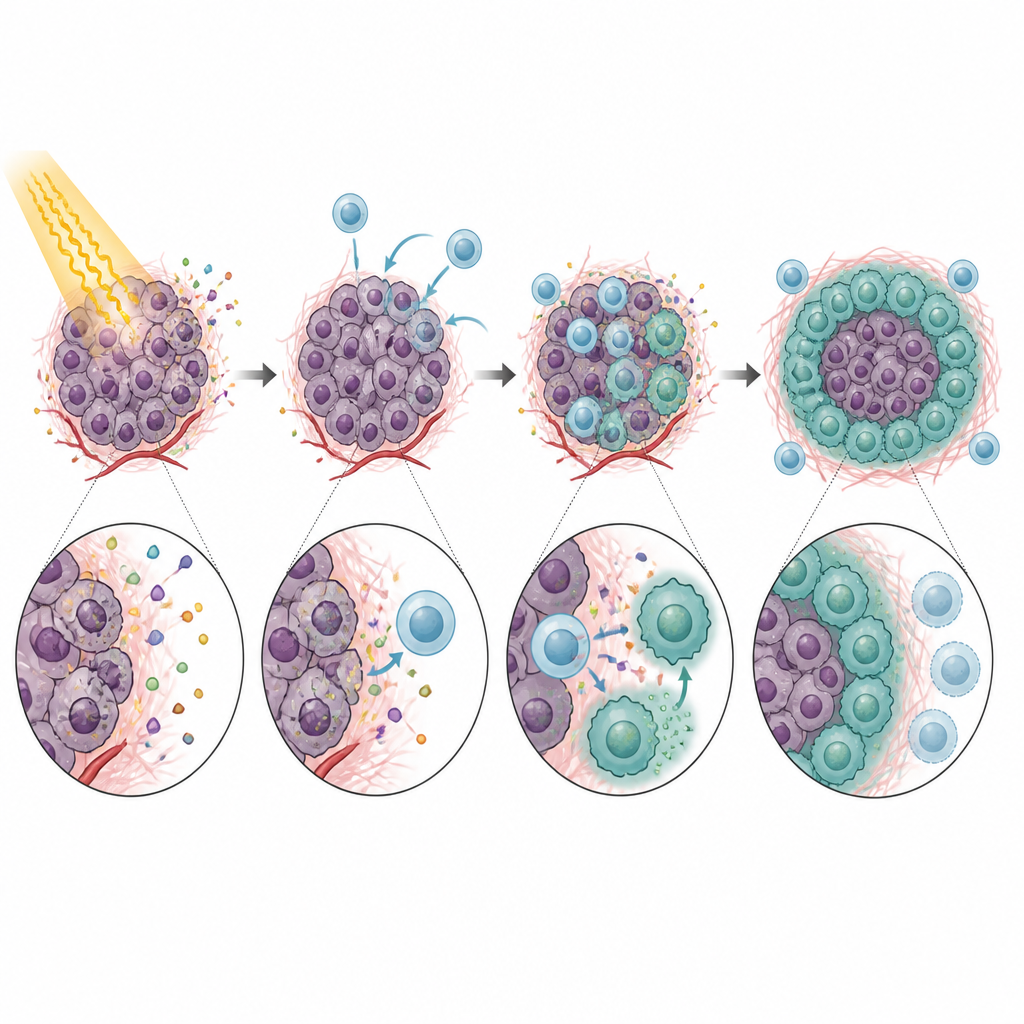
Van mobiele onderdrukkers naar zich vestigende schildcellen
Het verhaal eindigde niet bij monocyten. Na het binnendringen van de tumor rijpten veel CXCR5-positieve monocyten uit tot macrofagen, een ander type immuuncel. Onder invloed van een door bestraling geïnduceerde groeifactor, GM-CSF, kregen deze nakomelingen kenmerken van zogenaamde M2-achtige macrofagen, die bekendstaan om immuunreacties te dempen en weefselherstel te ondersteunen. Deze CXCR5-positieve macrofagen waren rijk aan PD-L1 en andere genen die met immuunsuppressie geassocieerd zijn, en ze waren bijzonder effectief in het blokkeren van T-celactiviteit. Het verlagen van GM-CSF-niveaus of het verstoren van de CXCL13–CXCR5-as verminderde het aantal van deze M2-achtige macrofagen en verbeterde de tumorrespons op bestraling bij muizen.
Winkjes uit patiëntmonsters en mogelijke nieuwe strategieën
Om te onderzoeken of vergelijkbare processen bij mensen plaatsvinden, bekeken de onderzoekers openbaar beschikbare kanker-datasets en monsters van patiënten die radiotherapie kregen. Tumoren van patiënten die bestraling hadden ondergaan vertoonden hogere niveaus van CXCR5, CD14 (een humane monocytenmarker) en PD-L1. In bloedmonsters nam het aantal monocyten toe na behandeling bij patiënten van wie de ziekte later progredeerde, maar niet bij degenen wiens tumoren krompen of stabiel bleven. In endeldarmkankermonsters bevatten tumoren na radiotherapie meer CXCL13 en CXCR5-positieve monocyten en macrofagen. In celkweek gedroegen humane monocyten die aan tumorresten werden blootgesteld zich vergelijkbaar met die in muizen: ze kregen CXCR5 via VEGF-gestuurde signalering en gingen hoge PD-L1-expressie vertonen.
Een zwakte in een voordeel veranderen
Samengevat laat dit werk zien dat bestraling onbedoeld een populatie immuuncellen kan aantrekken en hervormen die tumoren beschermt tegen juist die behandeling die ze zou moeten vernietigen. Door CXCL13 in tumoren te verhogen en VEGF-gestuurde CXCR5 in monocyten te stimuleren, creëert bestraling een pijplijn die onderdrukkende monocyten en macrofagen levert, die vervolgens killert-cellen uitschakelen via PD-L1. In muismodellen maakte het onderbreken van deze pijplijn op verschillende punten—zoals het blokkeren van VEGF, CXCL13, GM-CSF of PD-L1—het mogelijk dat bestraling effectiever werkte. Voor patiënten suggereren deze bevindingen dat het combineren van radiotherapie met zorgvuldig gekozen immuungerichte geneesmiddelen de balans weer in het voordeel van een echte antitumorrespons kan brengen en de lange termijn tumorcontrole kan verbeteren.
Bronvermelding: Lei, Y., Jia, R., Chen, C. et al. CXCR5+ monocyte emigration impairs the radiation-induced antitumor immune response. Nat Commun 17, 4258 (2026). https://doi.org/10.1038/s41467-026-70858-6
Trefwoorden: radiotherapie, tumorimmuniteit, monocyten, immuunsuppressie, PD-L1