Clear Sky Science · sv
CXCR5+ monocytutvandring försvagar radiationsinducerat antitumörimmunrespons
När cancerbehandling vänder sig mot sig själv
Strålbehandling är en hörnsten i cancerbehandlingen och används hos mer än hälften av alla patienter. Den är avsedd att skada tumörceller och mobilisera immunförsvaret för att avsluta uppdraget. Ändå återkommer många tumörer efter till synes framgångsrik behandling. Denna studie avslöjar en överraskande förklaring: vissa immunceller dras in i tumören efter strålning och hamnar i stället för att hjälpa till att skydda cancern. 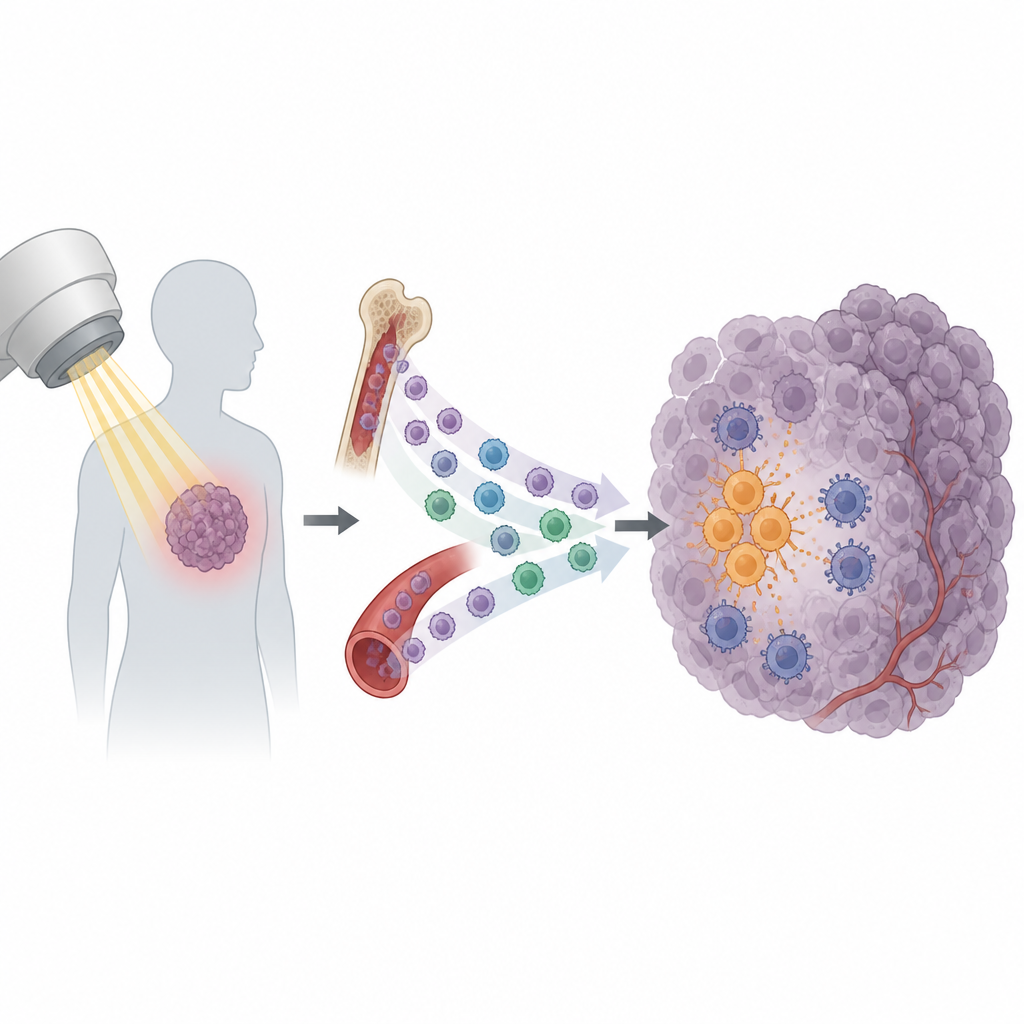
En tveeggad effekt av strålning
Strålning gör mer än att bara bryta DNA i cancerceller. Den får också tumörer att släppa ut en våg av signaler som lockar immunceller. Några av dessa signaler hjälper till att aktivera mördande T‑celler, som kan känna igen och angripa tumörceller. Men andra verkar ha motsatt effekt. Forskarna koncentrerade sig på en undergrupp av cirkulerande immunceller kallade monocyter. I flera musmodeller orsakade strålning en kraftig ökning av monocyter som trängde in i tumören, medan andra typer vita blodkroppar förändrades lite. Detta mönster antydde att monocyter kan vara viktiga aktörer för om en tumör blir känslig eller resistent mot strålning.
En kemisk ledtråd som lockar fram undertryckande celler
Genom att gräva djupare fann teamet att tumörer som utsattes för strålning producerade mer av en kemisk signal kallad CXCL13. Monocyter som bär en matchande "mottagarmolekyl", CXCR5, var särskilt benägna att strömma in i tumören efter behandling. Redan innan någon strålning gavs hade cancern på distans förberett dessa celler. Tumörceller utsöndrade tillväxtfaktorn VEGF i blodomloppet, vilket slog på en kedja av signaler inne i monocyterna känd som PI3K, Akt, mTOR och HIF‑1α‑vägen. Denna interna omkoppling ökade CXCR5 på deras yta och skapade effektivt ett cirkulerande förråd av CXCR5‑positiva monocyter redo att följa CXCL13‑spåret in i bestrålade tumörer.
Hur rekryterade celler tystar tumörmördare
När de väl var inne i tumören beter sig inte CXCR5‑positiva monocyter som hjälpsamma försvarare. Istället dämpade de starkt aktiviteten hos CD8‑T‑celler — de celler som behövs för att immunförsvaret ska rensa bort cancer efter strålning. I laboratorietester bromsade dessa monocyter T‑cellernas tillväxt och minskade deras produktion av viktiga angreppsmolekyler. Effekten berodde till stor del på PD‑L1, ett kontrollprote on på monocyterna som engagerar PD‑1 på T‑celler och instruerar dem att stå tillbaka. Möss utan CXCR5, eller tumörer utan CXCL13, visade bättre tumörkontroll efter strålning och mer aktiva CD8‑T‑celler. Att blockera CXCL13 eller PD‑L1 med antikroppar förbättrade ytterligare strålningens effekt i flera modeller, vilket pekar på en tydlig kedja från monocytrekrytering till T‑cellsundertryck och behandlingsmisslyckande. 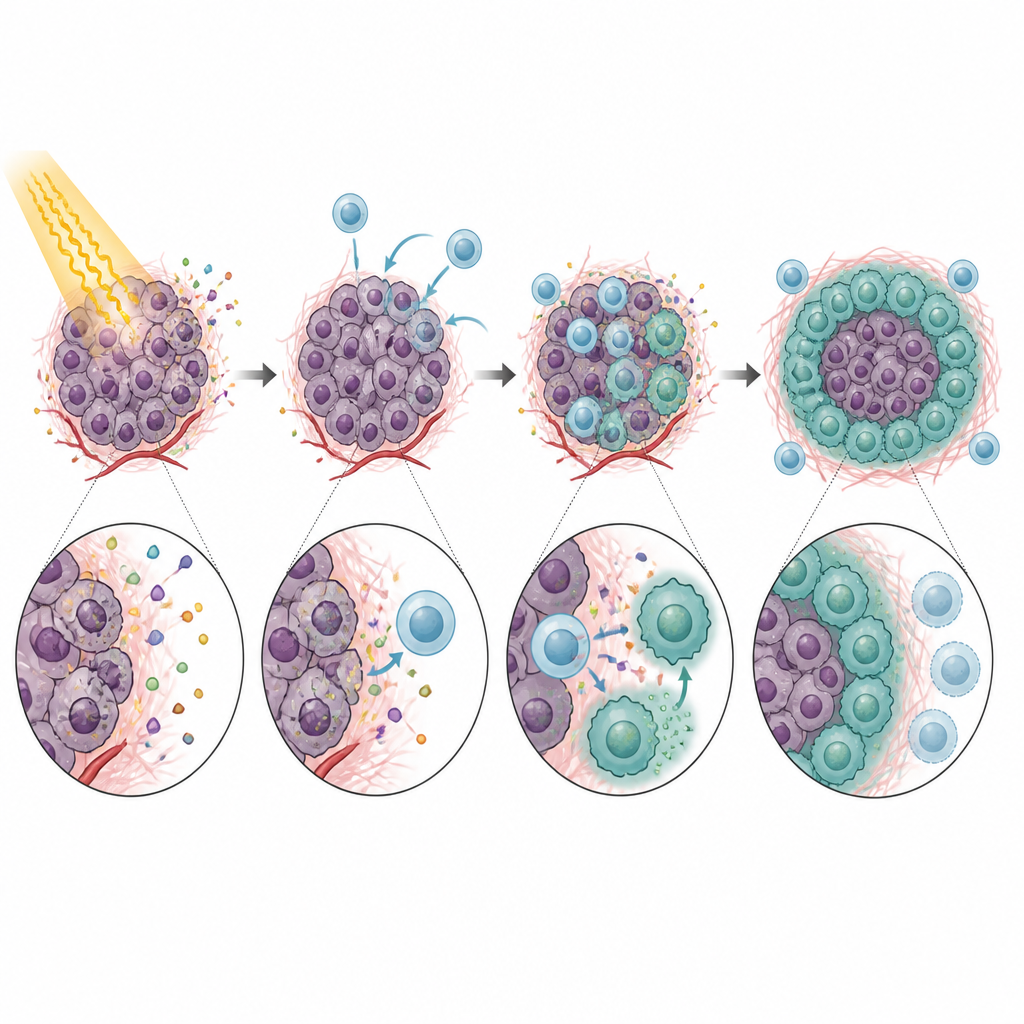
Från rörliga undertryckare till bofasta skyddsceller
Berättelsen slutade inte med monocyter. Efter att ha gått in i tumören mognade många CXCR5‑positiva monocyter till makrofager, en annan typ av immuncell. Under inflytande av en strålningsinducerad tillväxtfaktor kallad GM‑CSF fick dessa efterföljare drag av så kallade M2‑lika makrofager, som är kända för att dämpa immunsvar och stödja vävnadsreparation. Dessa CXCR5‑positiva makrofager var rika på PD‑L1 och andra gener kopplade till immunundertryckning, och de var särskilt effektiva på att blockera T‑cellsaktivitet. Att minska GM‑CSF‑nivåer eller störa CXCL13–CXCR5‑axeln minskade antalet av dessa M2‑lika makrofager och förbättrade tumörsvaren på strålning hos möss.
Ledtrådar från patientprover och möjliga nya strategier
För att undersöka om liknande processer sker hos människor analyserade forskarna offentligt tillgängliga cancerset och prover från patienter som fått radioterapi. Tumörer från patienter som genomgått strålning visade högre nivåer av CXCR5, CD14 (en mänsklig monocytsmarkör) och PD‑L1. I blodprover ökade antalet monocyter efter behandling hos patienter vars sjukdom senare progredierade, men inte hos dem vars tumörer krympte eller förblev stabila. I rektalcancerprover innehöll tumörer efter radioterapi fler CXCL13‑ och CXCR5‑positiva monocyter och makrofager. I cellkulturer beter sig mänskliga monocyter som de i möss när de exponeras för tumörvätskor: de får CXCR5 genom VEGF‑driven signalering och uttrycker höga nivåer av PD‑L1.
Att vända en svaghet till en fördel
Sammanfattningsvis visar detta arbete att strålning oavsiktligt kan kalla in och omforma en population immunceller som skyddar tumörer från den behandling som är avsedd att förstöra dem. Genom att öka CXCL13 i tumörer och VEGF‑driven CXCR5 i monocyter skapar strålning en pipeline som levererar undertryckande monocyter och makrofager, vilka sedan stänger av mördande T‑celler via PD‑L1. I musmodeller gjorde avbrott i denna pipeline på flera punkter — såsom att blockera VEGF, CXCL13, GM‑CSF eller PD‑L1 — att strålningen fungerade bättre. För patienter tyder dessa fynd på att kombinera radioterapi med noggrant valda immuntargeterade läkemedel kan återställa balansen mot ett verkligt antitumörsvar och förbättra långsiktig kontroll av cancer.
Citering: Lei, Y., Jia, R., Chen, C. et al. CXCR5+ monocyte emigration impairs the radiation-induced antitumor immune response. Nat Commun 17, 4258 (2026). https://doi.org/10.1038/s41467-026-70858-6
Nyckelord: strålbehandling, tumörimmunitet, monocyter, immunundertryckning, PD-L1