Clear Sky Science · fr
L’émigration des monocytes CXCR5+ compromet la réponse immunitaire antitumorale induite par la radiothérapie
Quand le traitement du cancer se retourne contre lui-même
La radiothérapie est un pilier des soins contre le cancer, utilisée chez plus de la moitié des patients. Elle vise à endommager les cellules tumorales et à mobiliser le système immunitaire pour achever l’élimination. Pourtant, de nombreuses tumeurs récidivent après un traitement apparemment réussi. Cette étude met au jour une raison surprenante : certaines cellules immunitaires sont attirées dans la tumeur après irradiation et finissent par protéger le cancer au lieu de l’aider à disparaître. 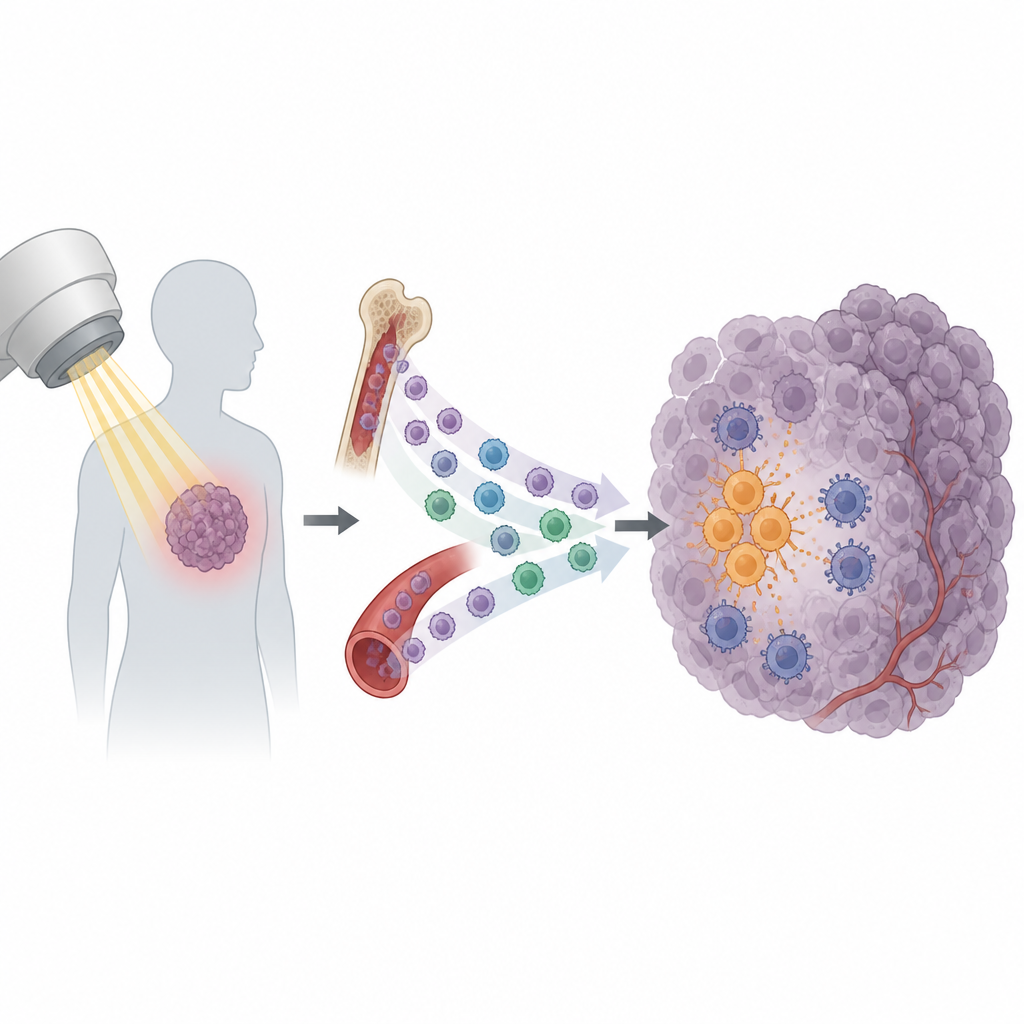
Un effet à double tranchant de la radiothérapie
La radiation ne se contente pas d’endommager l’ADN des cellules cancéreuses. Elle provoque aussi une libération de signaux par la tumeur qui recrutent des cellules immunitaires. Certains de ces signaux favorisent l’activation des lymphocytes T cytotoxiques, capables de reconnaître et d’attaquer les cellules tumorales. Mais d’autres semblent produire l’effet inverse. Les chercheurs se sont concentrés sur un sous-ensemble de cellules circulantes appelées monocytes. Dans plusieurs modèles murins de tumeur, l’irradiation a entraîné une hausse marquée de l’entrée de monocytes dans la tumeur, alors que d’autres types de globules blancs changeaient peu. Ce schéma suggérait que les monocytes pouvaient jouer un rôle déterminant dans la sensibilité ou la résistance tumorale à la radiothérapie.
Une piste chimique qui attire des cellules suppressives
En creusant plus loin, l’équipe a constaté que les tumeurs exposées à la radiothérapie produisaient davantage d’un signal chimique nommé CXCL13. Les monocytes exprimant le récepteur correspondant, CXCR5, étaient particulièrement susceptibles d’affluer dans la tumeur après le traitement. Avant toute irradiation, la tumeur avait déjà commencé à préparer ces cellules à distance. Les cellules tumorales sécrétaient le facteur de croissance VEGF dans la circulation, ce qui activait une cascade de signalisation dans les monocytes connue sous le nom de voie PI3K–Akt–mTOR–HIF-1α. Ce remaniement intracellulaire augmentait l’expression de CXCR5 à leur surface, créant ainsi un réservoir circulant de monocytes CXCR5+ prêts à suivre la piste CXCL13 vers les tumeurs irradiées.
Comment les cellules recrutées musellent les tueurs tumoraux
Une fois dans la tumeur, les monocytes CXCR5+ ne se comportaient pas comme des défenseurs utiles. Au contraire, ils limitaient fortement l’activité des lymphocytes T CD8+, précisément les cellules nécessaires à l’élimination tumorale après irradiation. In vitro, ces monocytes ralentissaient la prolifération des T et réduisaient leur production de molécules d’attaque clés. Cet effet dépendait en grande partie de PD-L1, une protéine de point de contrôle exprimée par les monocytes qui se lie à PD-1 sur les T et leur ordonne de s’arrêter. Des souris dépourvues de CXCR5, ou des tumeurs déficientes en CXCL13, présentaient un meilleur contrôle tumoral après irradiation et des CD8+ plus actifs. Le blocage de CXCL13 ou de PD-L1 par des anticorps améliorait encore l’efficacité de la radiothérapie dans plusieurs modèles, établissant une chaîne claire du recrutement des monocytes à la suppression des T et à l’échec du traitement. 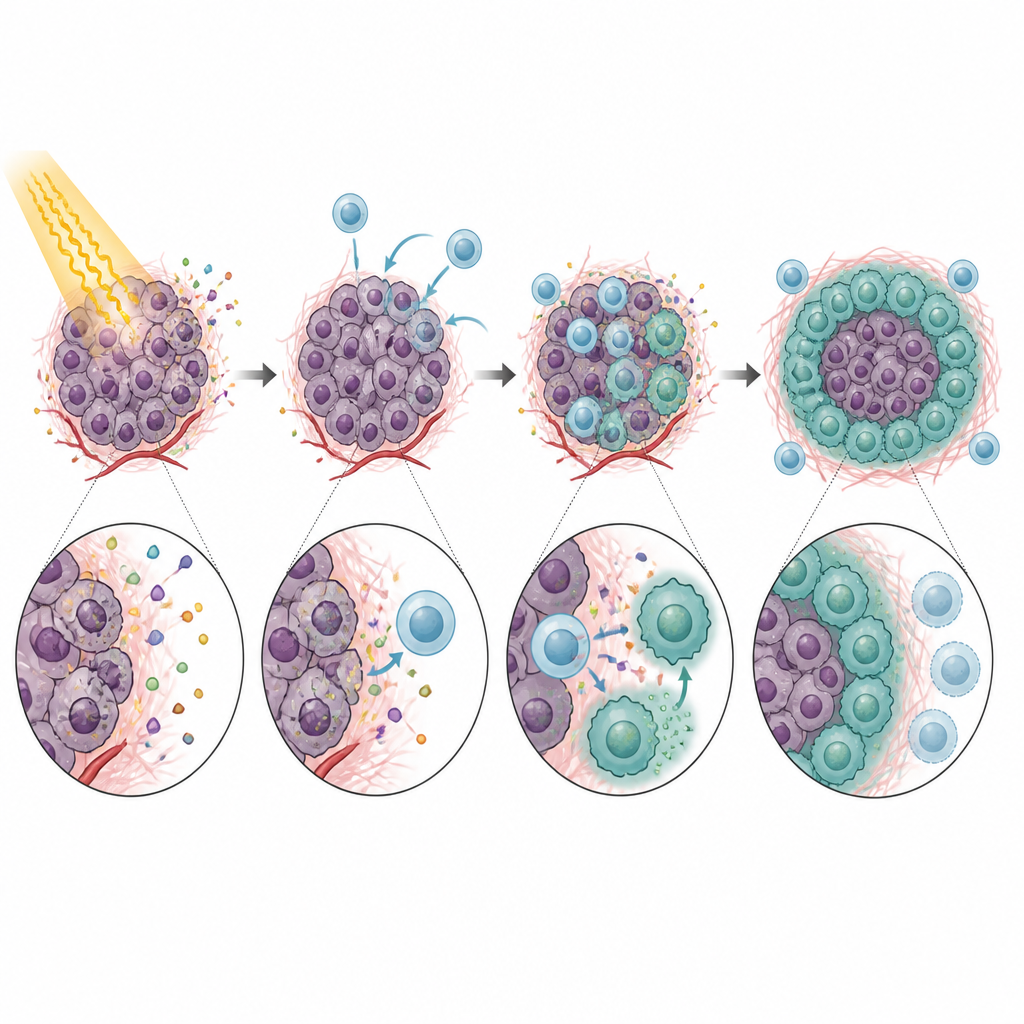
De suppresseurs mobiles à des macrophages protecteurs installés
L’histoire ne s’arrêtait pas aux monocytes. Après leur entrée dans la tumeur, beaucoup de monocytes CXCR5+ ont mûri en macrophages, un autre type de cellule immunitaire. Sous l’influence d’un facteur de croissance induit par la radiothérapie, le GM-CSF, ces descendants ont acquis des caractéristiques de macrophages de type M2, connus pour atténuer les réponses immunitaires et favoriser la réparation tissulaire. Ces macrophages CXCR5+ exprimaient beaucoup de PD-L1 et d’autres gènes associés à la suppression immunitaire, et s’avéraient particulièrement efficaces pour bloquer l’activité des lymphocytes T. La réduction des niveaux de GM-CSF ou l’interruption de l’axe CXCL13–CXCR5 diminuait le nombre de ces macrophages de type M2 et améliorait la réponse tumorale à la radiothérapie chez la souris.
Indices dans des échantillons de patients et stratégies potentielles
Pour vérifier si des processus similaires se produisent chez l’humain, les chercheurs ont examiné des bases de données publiques et des échantillons de patients ayant reçu une radiothérapie. Les tumeurs de patients irradiés présentaient des niveaux plus élevés de CXCR5, CD14 (un marqueur humain des monocytes) et PD-L1. Dans le sang, le nombre de monocytes augmentait après traitement chez les patients dont la maladie a progressé par la suite, mais pas chez ceux dont la tumeur régressait ou restait stable. Dans des prélèvements de cancer rectal, les tumeurs post-radiothérapie contenaient davantage de CXCL13 et de monocytes et macrophages CXCR5+. En culture cellulaire, les monocytes humains exposés aux fluides tumoraux se comportaient comme chez la souris, acquérant CXCR5 via une signalisation induite par le VEGF et exprimant un fort niveau de PD-L1.
Transformer une faiblesse en avantage
Au total, ce travail montre que la radiothérapie peut, de façon non intentionnelle, attirer et reprogrammer une population de cellules immunitaires qui protège les tumeurs contre le traitement censé les détruire. En augmentant CXCL13 dans les tumeurs et l’expression de CXCR5 dans les monocytes via le VEGF, la radiothérapie crée un circuit qui livre des monocytes et des macrophages suppressifs, lesquels éteignent ensuite les lymphocytes T cytotoxiques via PD-L1. Dans des modèles murins, interrompre ce circuit à plusieurs niveaux — en bloquant le VEGF, CXCL13, GM-CSF ou PD-L1 — a permis d’améliorer l’efficacité de la radiothérapie. Pour les patients, ces résultats suggèrent que combiner la radiothérapie avec des agents immunomodulateurs ciblés pourrait rétablir une réponse antitumorale efficace et améliorer le contrôle à long terme du cancer.
Citation: Lei, Y., Jia, R., Chen, C. et al. CXCR5+ monocyte emigration impairs the radiation-induced antitumor immune response. Nat Commun 17, 4258 (2026). https://doi.org/10.1038/s41467-026-70858-6
Mots-clés: radiothérapie, immunité tumorale, monocytes, suppression immunitaire, PD-L1