Clear Sky Science · de
CXCR5+ Monocyten‑Emigration beeinträchtigt die strahleninduzierte antitumorale Immunantwort
Wenn die Krebsbehandlung gegen sich selbst arbeitet
Die Strahlentherapie ist ein Pfeiler der Krebsbehandlung und kommt bei mehr als der Hälfte aller Patientinnen und Patienten zum Einsatz. Sie zielt darauf ab, Tumorzellen zu schädigen und das Immunsystem zu mobilisieren, damit es die Arbeit beendet. Dennoch kehren viele Tumoren nach scheinbar erfolgreicher Behandlung zurück. Diese Studie legt einen überraschenden Grund offen: Bestimmte Immunzellen werden nach der Bestrahlung in den Tumor gelockt und schützen den Krebs, anstatt bei seiner Zerstörung zu helfen. 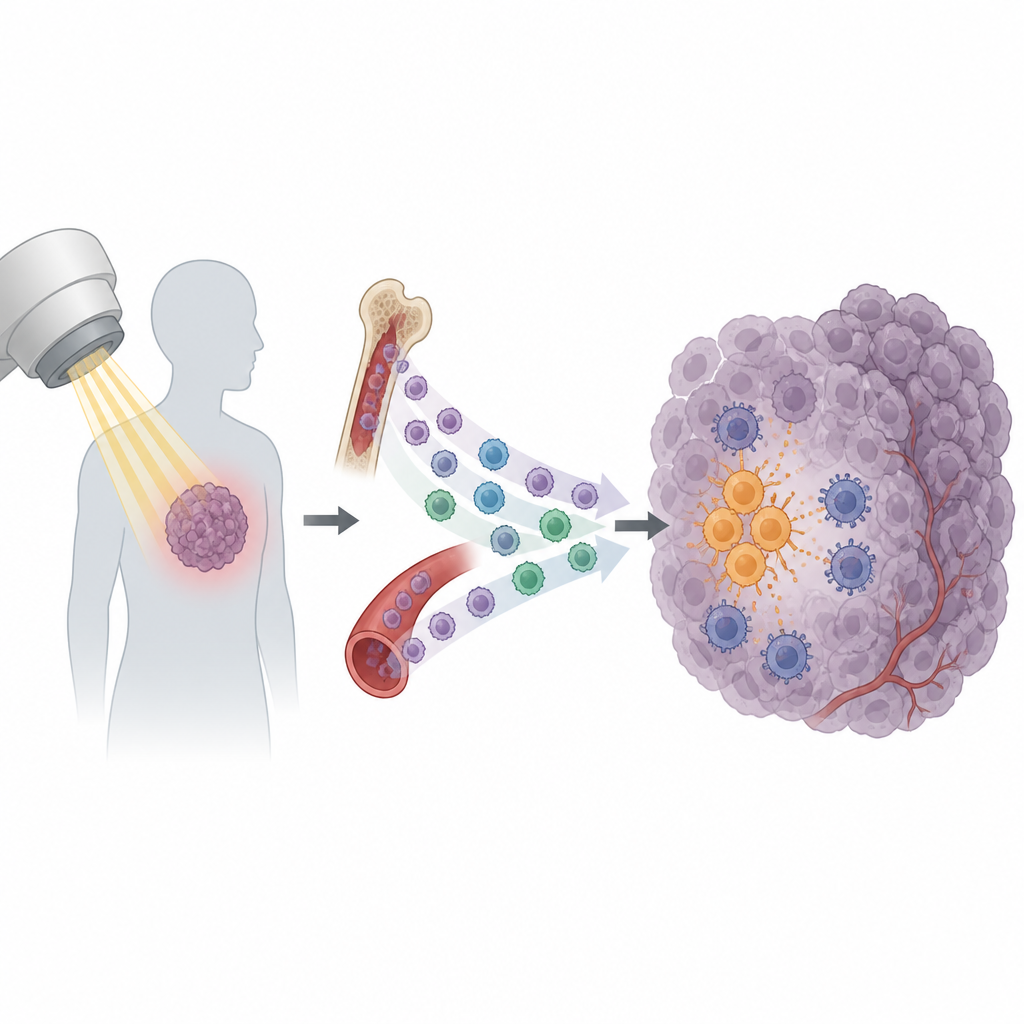
Eine zweischneidige Wirkung der Strahlung
Strahlung bewirkt mehr, als nur DNA in Krebszellen zu zerstören. Sie veranlasst Tumoren auch, einen Schub von Signalen freizusetzen, die Immunzellen anziehen. Einige dieser Signale helfen, CD8-Killerzellen zu aktivieren, die Tumorzellen erkennen und angreifen können. Andere scheinen jedoch den gegenteiligen Effekt zu haben. Die Forschenden konzentrierten sich auf eine Untergruppe zirkulierender Immunzellen, die Monozyten genannt werden. In mehreren Maus-Tumormodellen führte Strahlung zu einem starken Anstieg von Monozyten, die in den Tumor einwanderten, während sich andere weiße Blutkörperchen kaum veränderten. Dieses Muster deutete darauf hin, dass Monozyten wichtige Akteure dafür sein könnten, ob ein Tumor strahlensensibel oder strahlenresistent wird.
Eine chemische Spur, die suppressive Zellen anlockt
Bei tiefergehenden Untersuchungen fanden die Autoren heraus, dass bestrahlte Tumoren verstärkt das chemische Signal CXCL13 produzierten. Monozyten mit dem passenden „Empfänger“-Molekül CXCR5 auf ihrer Oberfläche strömten besonders stark in den Tumor nach der Behandlung. Schon vor der Strahlung hatte der Tumor diese Zellen aus der Ferne vorbereitet: Tumorzellen schütteten den Wachstumsfaktor VEGF ins Blut, der eine Signalkaskade in den Monozyten aktivierte (PI3K, Akt, mTOR und HIF‑1α). Diese interne Umprogrammierung erhöhte CXCR5 an ihrer Oberfläche und schuf so einen zirkulierenden Vorrat an CXCR5-positiven Monozyten, die der CXCL13‑Spur in bestrahlte Tumoren folgen konnten.
Wie rekrutierte Zellen Tumorkiller stilllegen
Einmal im Tumor angekommen, verhielten sich CXCR5-positive Monozyten nicht wie hilfreiche Verteidiger. Stattdessen dämpften sie stark die Aktivität von CD8-T-Zellen, den Zellen, die benötigt werden, damit das Immunsystem Krebs nach der Strahlung beseitigen kann. In Laborversuchen verlangsamten diese Monozyten das Wachstum von T‑Zellen und verringerten die Produktion wichtiger Angriffsmediatoren. Dieser Effekt beruhte weitgehend auf PD‑L1, einem Checkpoint-Protein auf den Monozyten, das an PD‑1 auf T‑Zellen bindet und sie zur Zurückhaltung auffordert. Mäuse ohne CXCR5 oder Tumoren ohne CXCL13 zeigten nach Strahlung eine bessere Tumorkontrolle und aktivere CD8-T-Zellen. Das Blockieren von CXCL13 oder PD‑L1 mit Antikörpern verbesserte in mehreren Modellen die Wirkung der Strahlung weiter und weist auf eine klare Kette von Monozytenrekrutierung über T‑Zell‑Suppression bis hin zum Therapieversagen hin. 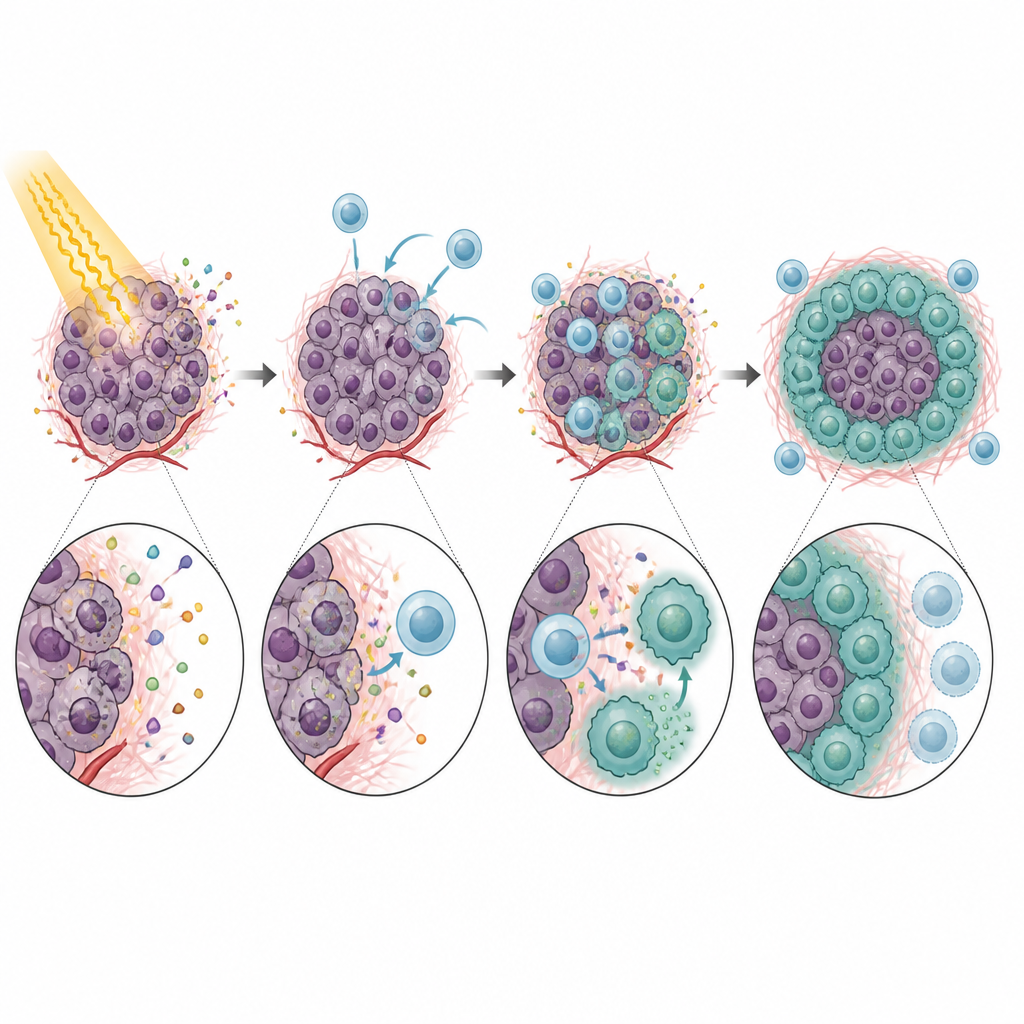
Von mobilen Unterdrückern zu sesshaften Schutzzellen
Die Geschichte endete nicht bei den Monozyten. Nach dem Eindringen in den Tumor differenzierten viele CXCR5-positive Monozyten zu Makrophagen, einer anderen Immunzellart. Unter dem Einfluss eines strahleninduzierten Wachstumsfaktors namens GM‑CSF nahmen diese Nachfahren Merkmale sogenannter M2‑ähnlicher Makrophagen an, die dafür bekannt sind, Immunantworten zu dämpfen und Gewebe zu reparieren. Diese CXCR5‑positiven Makrophagen wiesen hohe PD‑L1‑Spiegel und andere Gene auf, die mit Immunsuppression assoziiert sind, und sie waren besonders wirksam darin, T‑Zell‑Aktivität zu blockieren. Eine Verringerung von GM‑CSF oder die Störung der CXCL13–CXCR5‑Achse reduzierte die Zahl dieser M2‑ähnlichen Makrophagen und verbesserte die Tumorantwort auf Strahlung bei Mäusen.
Hinweise aus Patientenproben und mögliche neue Strategien
Um zu prüfen, ob ähnliche Prozesse beim Menschen ablaufen, analysierten die Forschenden öffentlich verfügbare Krebsdatensätze und Proben von Patientinnen und Patienten unter Radiotherapie. Tumoren nach Strahlung zeigten höhere Werte von CXCR5, CD14 (ein menschlicher Monozytenmarker) und PD‑L1. In Blutproben stieg die Monozytenzahl nach der Behandlung bei Patientinnen und Patienten an, deren Erkrankung später progredient wurde, nicht jedoch bei denen, deren Tumoren schrumpften oder stabil blieben. In Rektumkrebsproben fanden sich nach Radiotherapie mehr CXCL13 und CXCR5‑positive Monozyten und Makrophagen. In Zellkultur verhielten sich menschliche Monozyten, die Tumorflüssigkeiten ausgesetzt waren, ähnlich wie in Mäusen: Sie gewannen CXCR5 durch VEGF‑getriebene Signalwege und exprimierten viel PD‑L1.
Eine Schwäche in einen Vorteil verwandeln
Insgesamt zeigt diese Arbeit, dass Strahlung unbeabsichtigt eine Population von Immunzellen anlocken und umgestalten kann, die Tumoren vor genau der Behandlung schützt, die sie zerstören soll. Durch die Erhöhung von CXCL13 in Tumoren und VEGF‑getriebener CXCR5‑Expression in Monozyten schafft die Strahlung eine Pipeline, die suppressive Monozyten und Makrophagen liefert, die Killer‑T‑Zellen über PD‑L1 ausschalten. In Mausmodellen ermöglichte die Unterbrechung dieser Pipeline an verschiedenen Stellen — etwa durch Blockade von VEGF, CXCL13, GM‑CSF oder PD‑L1 — eine wirksamere Strahlentherapie. Für Patientinnen und Patienten deuten diese Befunde darauf hin, dass die Kombination von Radiotherapie mit gezielt ausgewählten immunmodulierenden Wirkstoffen das Gleichgewicht wieder zugunsten einer echten antitumoralen Reaktion verschieben und die langfristige Kontrolle von Krebs verbessern könnte.
Zitation: Lei, Y., Jia, R., Chen, C. et al. CXCR5+ monocyte emigration impairs the radiation-induced antitumor immune response. Nat Commun 17, 4258 (2026). https://doi.org/10.1038/s41467-026-70858-6
Schlüsselwörter: Radiotherapie, Tumorimmunität, Monozyten, Immunsuppression, PD-L1