Clear Sky Science · zh
由血清素受体5-HT2A对谷氨酸受体mGlu2的别构激活
脑内“门卫”如何联手
脑细胞表面布满感知谷氨酸和血清素等化学信使的微小“门卫”蛋白。该研究表明,两种长期与精神分裂症和帕金森病相关的此类门卫不仅并列工作:它们在物理上配对,使其中一个悄然增强另一个的活性。理解这种协作关系可以帮助科学家设计更精确、且副作用更少的调节脑信号的药物。
细胞表面的信号传递
许多常用药物作用于一大类细胞表面蛋白——G 蛋白偶联受体(GPCR)。每种 GPCR 检测特定的外部信号并把信息传入细胞内。由于单个神经细胞可同时展示数十种 GPCR,研究者长期疑惑这些受体如何避免发出混乱信息。一个假设是不同的 GPCR 在物理上结合在一起,形成成对或更大的群体以共享信息。但这种分组是否确实影响信号处理一直存在激烈争论。
大脑中令人意外的搭档
研究者聚焦于在情绪、感知和运动相关脑区出现的一对受体:代谢型谷氨酸受体 mGlu2 与血清素受体 5-HT2A。两者都是抗精神病药的靶点,早期工作提示它们在活体脑组织中形成功能性配对。团队在此提出两个关键问题:这些受体是否确实在细胞表面直接接触?如果是,这种物理接触是否改变了 mGlu2 的行为?
证明受体确实接触
为确定 mGlu2 与 5-HT2A 是否真正结合,作者使用了实验室培养的人类细胞,并在每种受体上标记了微小的荧光标记。当被标记的蛋白彼此靠近时,能量可从一个标记跳到另一个,产生可测量的信号。实验在两种受体同时存在时显示了强信号,表明它们在细胞表面聚集在一起。团队随后采用巧妙的化学方法,在每个受体中引入特定位置的“钩子”,使得当受体靠近时可以被锁定在一起。由此得到的交联复合物证实 mGlu2 与 5-HT2A 通过埋藏在细胞膜内的特定区域相互接触。
一个受体悄然激活另一个
接着,科学家检验这种接触是否改变 mGlu2 的响应。利用灵敏的荧光传感器和生化读出,他们监测了 mGlu2 的构象和活性状态。当 5-HT2A 存在时,即使不额外添加谷氨酸,更多的 mGlu2 受体转入“开启”构象,并在细胞内显示出小但显著的信号增加。阻断 mGlu2 本身能消除此效应,但用 5-HT2A 的配体将其开启或关闭并不能改变这种现象,而且一个无法激活其常规信号通路的 5-HT2A 突变体仍然能增强 mGlu2。这意味着 5-HT2A 更像是一个支撑性的支架而非主动开关:它的存在及物理接触稳定了 mGlu2 的活性构象。
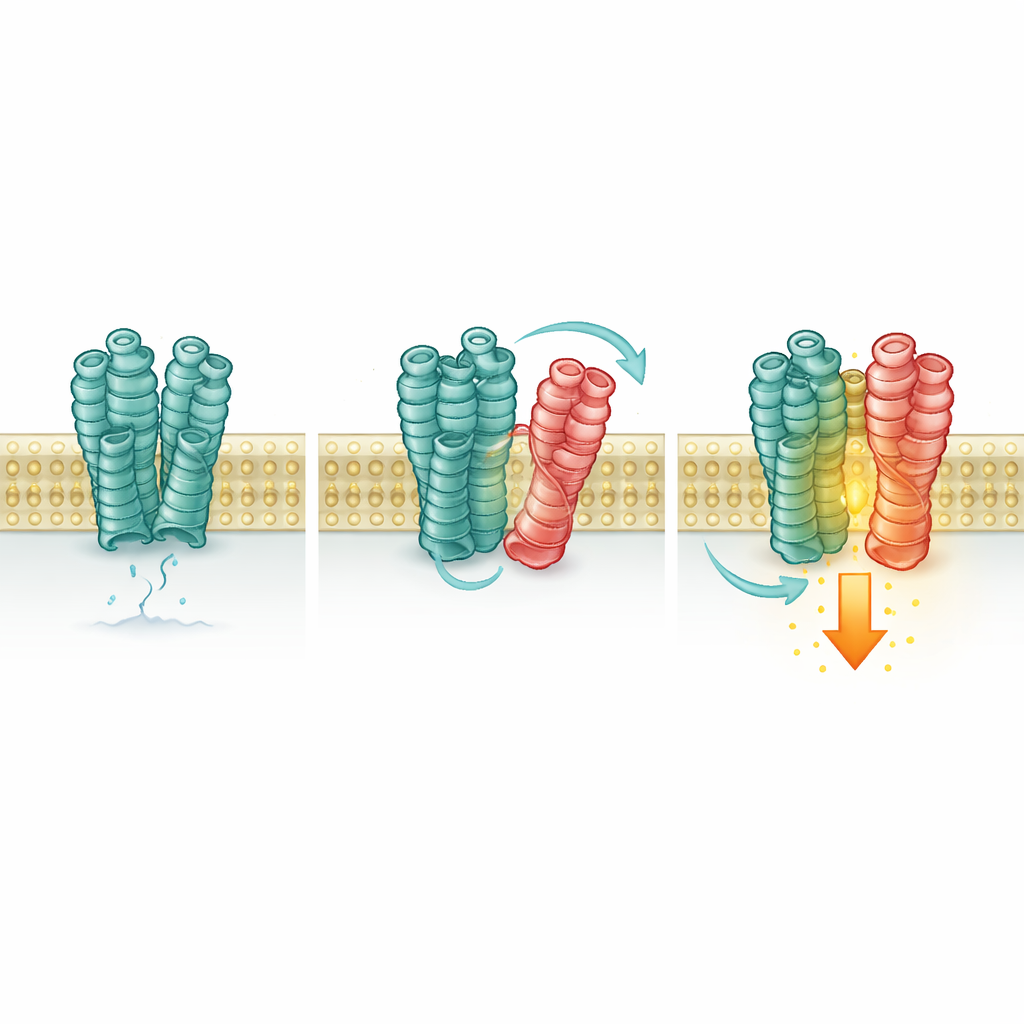
还有许多其他伙伴参与
故事并不止于血清素。作者筛选了另外 44 种 GPCR,观察它们是否也能以类似方式影响 mGlu2。其中若干受体,包括多种多巴胺受体和另一种血清素亚型,也将 mGlu2 推向其活性状态,而其他一些影响甚微。一个多巴胺受体 D1 在没有额外谷氨酸的情况下明显提高了 mGlu2 的基线活性,亦与偏向“开启”位置的物理配对一致。相比之下,作为对照的一个毒蕈碱型(muscarinic)受体既未与 mGlu2 强烈相互作用,也未改变其活性。
这对脑疾病为何重要
这项工作表明,某些脑内受体并非独自等待各自的化学钥匙。通过形成小型复合体,一个受体可以别构性地(间接地)调整另一个受体的行为。就 mGlu2 与 5-HT2A 而言,这意味着与血清素相关的受体可以在自身不主动发出信号时,仍然塑造谷氨酸信号的处理方式。由于这些受体配对与精神分裂症、帕金森病及其他可能的疾病有关,它们为药物设计提供了一个吸引人的新角度:针对配对中某一成员的药物或可被设计为调节另一方的活性,从而对复杂脑回路实现更微妙的控制。
引用: Gai, S., Lin, L., Meng, J. et al. Allosteric activation of the glutamate receptor mGlu2 by the serotonin receptor 5-HT2A. Nat Commun 17, 3303 (2026). https://doi.org/10.1038/s41467-026-69939-3
关键词: GPCR 异源体, mGlu2 受体, 5-HT2A 受体, 别构调制, 精神分裂症