Clear Sky Science · de
Allosterische Aktivierung des Glutamatrezeptors mGlu2 durch den Serotoninrezeptor 5-HT2A
Wie Wächter der Gehirnzellen zusammenarbeiten
Gehirnzellen sind mit winzigen „Wächter“-Proteinen bedeckt, die chemische Botenstoffe wie Glutamat und Serotonin wahrnehmen. Diese Studie zeigt, dass zwei solcher Wächter, die lange mit Schizophrenie und Parkinson in Verbindung gebracht wurden, nicht nur nebeneinander arbeiten: Sie koppeln sich physisch so, dass der eine stillschweigend die Aktivität des anderen verstärkt. Das Verständnis dieser Partnerschaft könnte Wissenschaftlern helfen, Medikamente zu entwickeln, die Gehirnsignale präziser und mit weniger Nebenwirkungen feinabstimmen.
Signale an der Zelloberfläche
Viele gebräuchliche Medikamente wirken auf eine große Familie von Zelloberflächenproteinen, die G-Protein-gekoppelte Rezeptoren oder GPCRs genannt werden. Jeder GPCR erkennt bestimmte äußere Signale und leitet die Botschaft ins Zellinnere weiter. Da eine einzelne Nervenzelle gleichzeitig Dutzende von GPCR-Typen zeigen kann, haben Forscher lange darüber nachgedacht, wie diese Rezeptoren vermischte Signale vermeiden. Ein Vorschlag ist, dass sich verschiedene GPCRs physisch zusammenschließen und Paare oder größere Gruppen bilden, die Informationen teilen. Ob solche Zusammenschlüsse jedoch wirklich die Signalverarbeitung beeinflussen, ist heftig diskutiert worden.
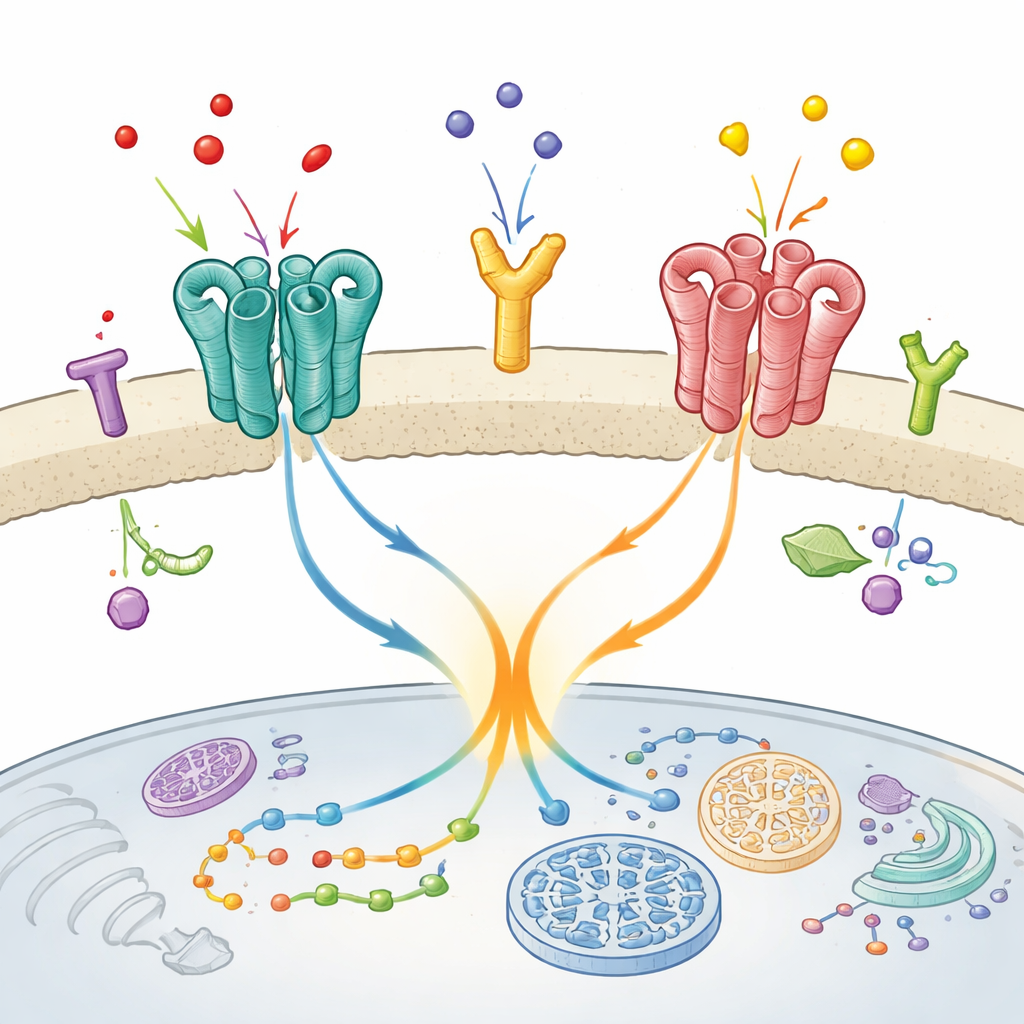
Eine überraschende Partnerschaft im Gehirn
Die Forscher konzentrierten sich auf ein spezielles Duo, das in Hirnregionen vorkommt, die an Stimmung, Wahrnehmung und Bewegung beteiligt sind: den metabotropen Glutamatrezeptor mGlu2 und den Serotoninrezeptor 5-HT2A. Beide sind Ziele von antipsychotischen Medikamenten, und frühere Arbeiten deuteten darauf hin, dass sie in lebendem Hirngewebe ein funktionales Paar bilden. Hier stellten die Autoren zwei zentrale Fragen: Sitzen diese Rezeptoren wirklich in direktem Kontakt auf der Zelloberfläche, und falls ja, verändert dieser physische Kontakt das Verhalten von mGlu2?
Den Nachweis, dass die Rezeptoren sich berühren
Um zu untersuchen, ob mGlu2 und 5-HT2A tatsächlich zusammenkommen, verwendeten die Autoren in Laboren gezüchtete menschliche Zellen und markierten jeden Rezeptor mit winzigen fluoreszierenden Markern. Wenn die markierten Proteine nah genug beieinander liegen, kann Energie von einem Marker zum anderen springen und ein messbares Signal erzeugen. Diese Experimente zeigten ein starkes Signal, wenn beide Rezeptoren vorhanden waren, was darauf hindeutet, dass sie an der Zelloberfläche zusammenklumpen. Das Team nutzte dann einen cleveren chemischen Trick und brachte speziell platzierte „Haken“ in jeden Rezeptor ein, sodass sie, wenn sie nahe beieinander sind, miteinander verriegelt werden können. Die daraus resultierenden quervernetzten Komplexe bestätigten, dass mGlu2 und 5-HT2A über bestimmte Abschnitte, die in der Zellmembran verborgen liegen, miteinander in Kontakt stehen.
Ein Rezeptor schaltet den anderen stillschweigend ein
Als Nächstes überprüften die Wissenschaftler, ob dieser Kontakt die Reaktion von mGlu2 verändert. Mit empfindlichen Fluoreszenzsensoren und biochemischen Messgrößen beobachteten sie die Konformation und den Aktivitätszustand von mGlu2. In Gegenwart von 5-HT2A, selbst ohne zusätzliches Glutamat, wechselten mehr mGlu2-Rezeptoren in ihre „an“-Konformation und zeigten einen kleinen, aber signifikanten Anstieg der Signalübertragung innerhalb der Zelle. Das Blockieren von mGlu2 selbst beseitigte diesen Effekt, doch das Ein- oder Ausschalten von 5-HT2A mit seinen eigenen Wirkstoffen tat dies nicht, und ein mutiertes 5-HT2A, das seinen üblichen Signalweg nicht aktivieren kann, verstärkte dennoch mGlu2. Das bedeutet, dass 5-HT2A eher wie eine unterstützende Schiene als wie ein aktiver Schalter wirkt: Allein seine Anwesenheit und der physische Kontakt stabilisieren die aktive Form von mGlu2.
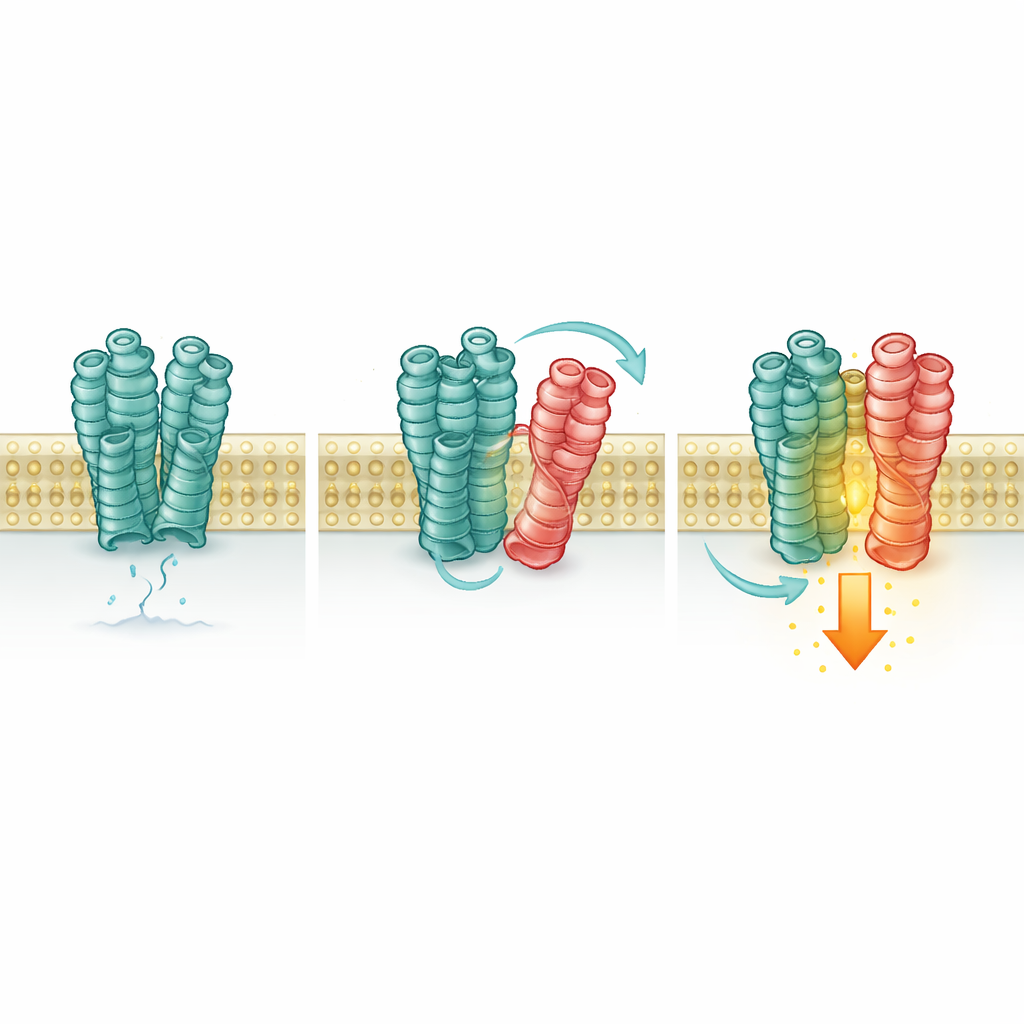
Viele weitere Partner mischen mit
Die Geschichte endet nicht beim Serotonin. Die Autoren testeten 44 weitere GPCRs, um zu sehen, ob sie mGlu2 in ähnlicher Weise beeinflussen können. Mehrere, darunter mehrere Dopaminrezeptoren und ein weiterer Serotoninuntertyp, schubsten mGlu2 ebenfalls in Richtung seines aktiven Zustands, während andere wenig Effekt zeigten. Ein Dopaminrezeptor, D1, erhöhte deutlich die Grundaktivität von mGlu2 in Abwesenheit von zusätzlichem Glutamat, was erneut mit einer physischen Partnerschaft übereinstimmt, die die „an“-Position begünstigt. Im Gegensatz dazu interagierte ein als Kontrolle verwendeter muscarinerger Rezeptor weder stark mit mGlu2 noch veränderte er dessen Aktivität.
Warum das für Hirnerkrankungen wichtig ist
Diese Arbeit zeigt, dass bestimmte Gehirnrezeptoren mehr tun, als unabhängig auf ihre eigenen chemischen Schlüssel zu warten. Durch die Bildung kleiner Verbände kann ein Rezeptor allosterisch, also indirekt, das Verhalten eines anderen feinabstimmen. Im Fall von mGlu2 und 5-HT2A bedeutet das, dass serotoninverknüpfte Rezeptoren beeinflussen können, wie Glutamatsignale verarbeitet werden, selbst wenn sie selbst nicht aktiv signalisieren. Da diese Rezeptorpartnerschaften mit Schizophrenie, Parkinson und möglicherweise anderen Erkrankungen in Verbindung stehen, bieten sie einen attraktiven neuen Ansatz für die Wirkstoffentwicklung: Medikamente, die ein Mitglied eines Paares anvisieren, könnten so gestaltet werden, dass sie die Aktivität des anderen modulieren und so eine subtilere Kontrolle über komplexe Hirnschaltkreise ermöglichen.
Zitation: Gai, S., Lin, L., Meng, J. et al. Allosteric activation of the glutamate receptor mGlu2 by the serotonin receptor 5-HT2A. Nat Commun 17, 3303 (2026). https://doi.org/10.1038/s41467-026-69939-3
Schlüsselwörter: GPCR-Heteromere, mGlu2-Rezeptor, 5-HT2A-Rezeptor, allosterische Modulation, Schizophrenie