Clear Sky Science · sv
Allosterisk aktivering av glutamatreceptorn mGlu2 av serotoninreceptorn 5‑HT2A
Hur hjärnans portvakter samarbetar
Hjärnceller är täckta av små ”portvakt”‑proteiner som känner av kemiska budbärare som glutamat och serotonin. Denna studie visar att två sådana portvakter, länge kopplade till schizofreni och Parkinsons sjukdom, gör mer än att bara verka sida vid sida: de bildar fysiska partnerskap så att den ena tyst förstärker den andras aktivitet. Att förstå detta samarbete kan hjälpa forskare att utforma läkemedel som finjusterar hjärnsignaler med större precision och färre biverkningar.
Signaler vid cellens yta
Många vanliga läkemedel verkar på en stor familj av cellytproteiner som kallas G protein‑kopplade receptorer, eller GPCR:er. Varje GPCR upptäcker särskilda yttre signaler och förmedlar budskapet in i cellen. Eftersom en enda nervcell kan visa dussintals typer av GPCR:er samtidigt har forskare länge undrat hur dessa receptorer undviker att sända förvirrade eller motstridiga signaler. Ett förslag är att olika GPCR:er fysiskt går ihop och bildar par eller större grupper som delar information. Men om sådana grupperingar verkligen påverkar hur signaler bearbetas har varit föremål för intensiv debatt.
En överraskande allians i hjärnan
Forskarlaget fokuserade på ett särskilt par som finns i hjärnregioner involverade i humör, perception och rörelse: den metabotropa glutamatreceptorn mGlu2 och serotoninreceptorn 5‑HT2A. Båda är mål för antipsykotiska läkemedel, och tidigare arbete har antytt att de bildar ett funktionellt par i levande hjärnvävnad. Här ställde teamet två nyckelfrågor: Sitter dessa receptorer verkligen i direkt kontakt på cellytan, och om så är fallet, förändrar denna fysiska kontakt mGlu2:s beteende?
Bevisa att receptorerna rör vid varandra
För att se om mGlu2 och 5‑HT2A verkligen går ihop använde författarna humana celler odlade i laboratoriet och märkte varje receptor med små fluorescerande markörer. När de märka proteinerna kommer tillräckligt nära kan energi hoppa från en markör till en annan och skapa en mätbar signal. Dessa experiment visade en stark signal när båda receptorerna var närvarande, vilket indikerar att de klustrar ihop sig på cellytan. Teamet använde sedan ett smart kemiskt knep och införde särskilt placerade ”krokar” i vardera receptorn så att de, när de låg nära varandra, kunde låsas samman. De resulterande tvärbundna komplexen bekräftade att mGlu2 och 5‑HT2A är i kontakt genom specifika sektioner inne i cellmembranet.
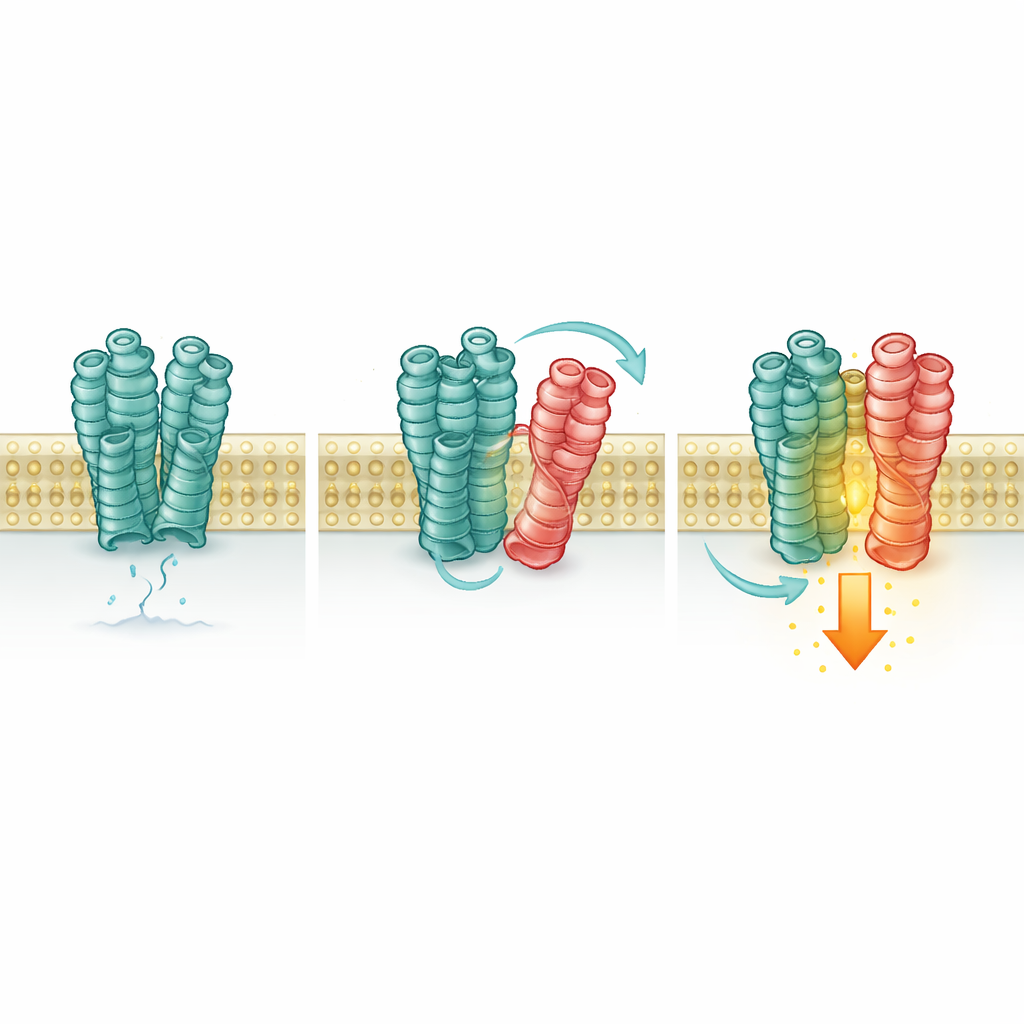
En receptor tyst slår på en annan
Nästa steg var att testa om denna kontakt förändrar hur mGlu2 reagerar. Med känsliga fluorescerande sensorer och biokemiska avläsningar övervakade de mGlu2:s form och aktivitetsstatus. När 5‑HT2A var närvarande, även utan tillsatt glutamat, skiftade fler mGlu2‑receptorer till sin "på"‑konformation och visade en liten men statistiskt signifikant ökning av signaleringen inuti cellen. Blockera mGlu2 i sig tog bort denna effekt, men att slå på eller av 5‑HT2A med dess egna läkemedel gjorde det inte, och en mutant 5‑HT2A som inte kan aktivera sin vanliga signalväg ökade ändå mGlu2. Detta betyder att 5‑HT2A agerar mer som ett stödjande stag än som en aktiv omkopplare: dess blotta närvaro och fysiska kontakt stabiliserar mGlu2:s aktiva form.
Många andra partners ansluter
Berättelsen slutar inte med serotonin. Författarna skannade 44 andra GPCR:er för att se om de på liknande sätt kunde påverka mGlu2. Flera, inklusive flera dopaminreceptorer och en annan serotoninsubtyp, puttade också mGlu2 mot dess aktiva tillstånd, medan andra hade liten effekt. En dopaminreceptor, D1, ökade tydligt mGlu2:s baslinjeaktivitet i avsaknad av extra glutamat, vilket återigen stämmer med en fysisk partnerskap som gynnar den "på"‑positionen. I kontrast interagerade en muskarin receptor som användes som kontroll varken starkt med mGlu2 eller förändrade dess aktivitet.
Varför detta betyder något för hjärnsjukdomar
Detta arbete visar att vissa hjärnreceptorer gör mer än att sitta självständigt och vänta på sina egna kemiska nycklar. Genom att bilda små sammansättningar kan en receptor allosteriskt, det vill säga indirekt, finjustera beteendet hos en annan. I fallet mGlu2 och 5‑HT2A innebär detta att serotonin‑kopplade receptorer kan forma hur glutamatsignaler bearbetas, även när de själva inte aktivt signalerar. Eftersom dessa receptorpartnerskap är kopplade till schizofreni, Parkinsons sjukdom och möjligen andra tillstånd, erbjuder de en lockande ny vinkel för läkemedelsutveckling: läkemedel som riktar sig mot en medlem i ett par kan utformas för att modulera den andras aktivitet och därigenom ge mer subtil kontroll över komplexa hjärnkretsar.
Citering: Gai, S., Lin, L., Meng, J. et al. Allosteric activation of the glutamate receptor mGlu2 by the serotonin receptor 5-HT2A. Nat Commun 17, 3303 (2026). https://doi.org/10.1038/s41467-026-69939-3
Nyckelord: GPCR-heteromerer, mGlu2-receptor, 5-HT2A-receptor, allosterisk modulering, schizofreni