Clear Sky Science · ar
التنشيط التحالفي لمستقبل الغلوتامات mGlu2 بواسطة مستقبل السيروتونين 5-HT2A
كيف يتكاتف حراس البوابة في الخلايا العصبية
تغطي الخلايا العصبية بروتينات صغيرة تعمل كـ«حراس بوابة» تستشعر رُسالَات كيميائية مثل الغلوتامات والسيروتونين. تُظهر هذه الدراسة أن اثنين من هؤلاء الحراس، المرتبطين طويلاً بالفصام وداء باركنسون، لا يكتفيان بالعمل جنبًا إلى جنب: بل يتآزران فعليًا بحيث يعزز أحدهما نشاط الآخر بهدوء. وفهم هذا الشراكة قد يساعد العلماء على تصميم عقاقير تضبط إشارات الدماغ بدقة أكبر وبآثار جانبية أقل.
الإشارات على سطح الخلية
العديد من الأدوية الشائعة تعمل على عائلة هائلة من بروتينات سطح الخلية تُدعى مستقبلات مرتبطة بالبروتين G، أو GPCRs. يكتشف كل مستقبل من هذه المستقبلات إشارات خارجية معينة وينقل الرسالة إلى داخل الخلية. وبما أن خلية عصبية واحدة قد تعرض عشرات أنواع GPCR في آن واحد، تساءل الباحثون منذ زمن طويل كيف تتفادى هذه المستقبلات إرسال رسائل مُختلِطة. أحد الاقتراحات هو أن مستقبلات GPCR المختلفة تنضم ماديًا معًا، مكونة أزواجًا أو مجموعات أكبر تتشارك المعلومات. لكن ما إذا كانت مثل هذه التجمعات تؤثر فعلاً على معالجة الإشارات ظل موضوع نقاش حاد.
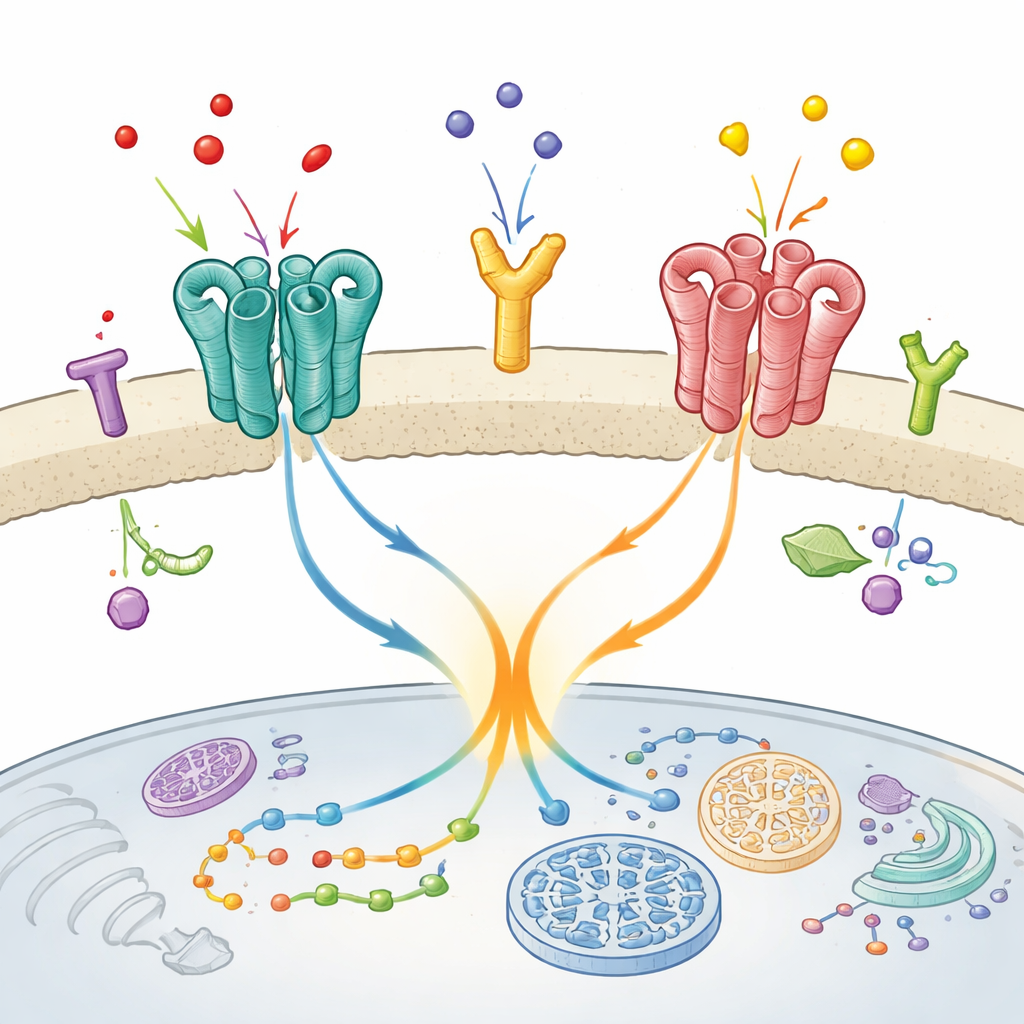
شراكة مفاجئة في الدماغ
ركز الباحثون على ثنائي محدد يوجد في مناطق دماغية تشارك في المزاج والإدراك والحركة: مستقبل الغلوتامات المتحوِّر mGlu2 ومُستقبل السيروتونين 5-HT2A. كلاهما هدف لأدوية مضادة للذهان، وأشارت أعمال سابقة إلى أنهما يشكلان زوجًا وظيفيًا في أنسجة الدماغ الحية. هنا، طرح الفريق سؤالين رئيسيين: هل تجلس هذه المستقبلات فعلًا على اتصال مباشر على سطح الخلية، وإذا كان الأمر كذلك، هل يغير ذلك الاتصال المادي سلوك mGlu2؟
إثبات تلامس المستقبلات
للاطلاع على ما إذا كان mGlu2 و5-HT2A يقتربان فعلاً من بعضهما، استخدم المؤلفون خلايا بشرية مزروعة في المختبر ووضعوا علامات فلورية صغيرة على كل مستقبل. عندما تقترب البروتينات الموسومة بما فيه الكفاية، يمكن للطاقة أن تنتقل من علامة إلى أخرى، مكوّنةً إشارة يمكن قياسها. أظهرت هذه التجارب إشارة قوية عند وجود كلا المستقبلين، مما يدل على أنهما يتجمعان على سطح الخلية. ثم استخدم الفريق حيلة كيميائية ذكية، حيث أدخلوا «خطاطيف» موضوعة بعناية في كل مستقبل بحيث، عند التقارب، يمكن قفلها معًا. أكدت المعقدات المربوطة الناتجة أن mGlu2 و5-HT2A يتلامسان عبر أجزاء محددة مدفونة في غشاء الخلية.
مستقبل يفعِّل آخر بهدوء
بعد ذلك، اختبر العلماء ما إذا كان هذا الاتصال يغير استجابة mGlu2. باستخدام مجسات فلورية حساسة وقراءات بيوكيميائية، راقبوا شكل وحالة نشاط mGlu2. عندما كان 5-HT2A موجودًا، حتى من دون غلوتامات مضافة، انتقل عدد أكبر من مستقبلات mGlu2 إلى تأقلمها «المُنشَط» وأظهر زيادة صغيرة لكنها ذات دلالة في الإشارات داخل الخلية. إزالة مفعول mGlu2 ذاته أزالت هذا التأثير، لكن تشغيل أو إيقاف 5-HT2A بأدويته لم يفعل ذلك، ونشاط شكل طافر من 5-HT2A لا يستطيع تفعيل مساره الإشاري المعتاد عزَّز أيضًا mGlu2. هذا يعني أن 5-HT2A يعمل أشبه بدعامة داعمة أكثر من كونه مفتاحًا نشطًا: وجوده المادي وتلامسه يثبِّت الشكل النشط لـmGlu2.
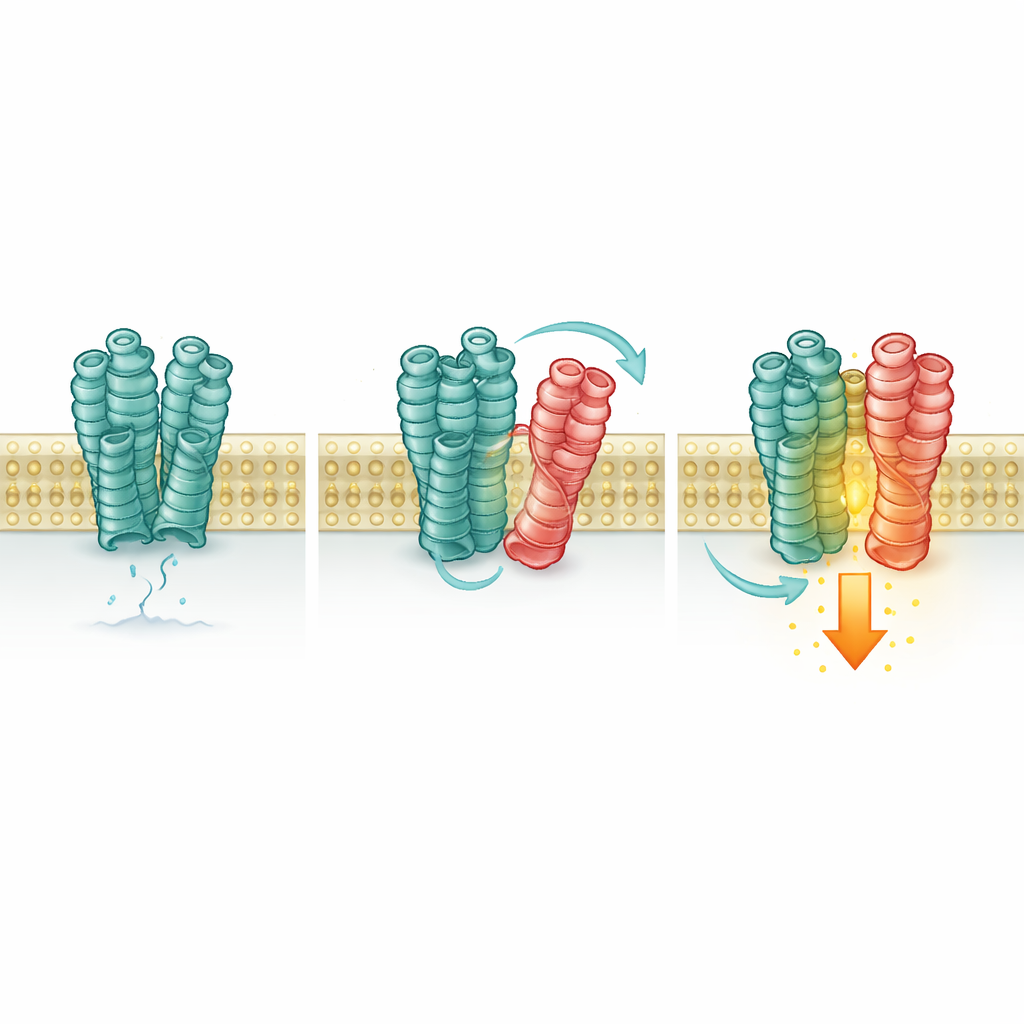
انضمام شركاء آخرين أيضًا
القصة لا تنتهي مع السيروتونين. فحص المؤلفون 44 مستقبلًا آخر من GPCR ليروا ما إذا كان بإمكانها التأثير بالمثل على mGlu2. ساهم عدة منها، بما في ذلك مستقبلات الدوبامين المتعددة ونوع آخر من السيروتونين، في دفع mGlu2 نحو حالته النشطة، بينما كان لآخرين تأثير ضئيل. أحد مستقبلات الدوبامين، D1، زاد بوضوح النشاط الأساسي لـmGlu2 في غياب غلوتامات إضافية، وهو ما يتوافق مرة أخرى مع شراكة مادية تُفضِّل الوضعية «المُشغَّلة». بالمقابل، مستقبل مسكاريني استُخدم كضابط لم يتفاعل بقوة مع mGlu2 ولا غيّر نشاطه.
لماذا يهم هذا لاضطرابات الدماغ
تُظهر هذه الدراسة أن بعض مستقبلات الدماغ تفعل أكثر من الجلوس مستقلَّةً في انتظار مفاتيحها الكيميائية. بتشكيلها تجمّعات صغيرة، يمكن لمستقبل واحد أن يضبط بطريقة تحالفيّة، أو غير مباشرة، سلوك آخر. في حالة mGlu2 و5-HT2A، يعني ذلك أن مستقبلات المرتبطة بالسيروتونين يمكن أن تشكِّل كيفية معالجة إشارات الغلوتامات، حتى عندما لا تكون مُفعَّلة بنفسها. وبما أن هذه الشراكات المستقبلية مرتبطة بالفصام وداء باركنسون وربما حالات أخرى، فإنها تقدّم زاوية جديدة جذابة لتصميم الأدوية: فالعقاقير التي تستهدف أحد أعضاء الزوج قد تُصمَّم لتعديل نشاط الآخر، ما يوفر سيطرة أدق على دوائر دماغية معقّدة.
الاستشهاد: Gai, S., Lin, L., Meng, J. et al. Allosteric activation of the glutamate receptor mGlu2 by the serotonin receptor 5-HT2A. Nat Commun 17, 3303 (2026). https://doi.org/10.1038/s41467-026-69939-3
الكلمات المفتاحية: متغايرات GPCR, مستقبل mGlu2, مستقبل 5-HT2A, التعديل التحالفي, الفصام