Clear Sky Science · es
Activación alostérica del receptor de glutamato mGlu2 por el receptor de serotonina 5-HT2A
Cómo se asocian los guardianes de las células cerebrales
Las células cerebrales están cubiertas por diminutas proteínas “guardianas” que detectan mensajeros químicos como el glutamato y la serotonina. Este estudio muestra que dos de esos guardianes, vinculados desde hace tiempo a la esquizofrenia y la enfermedad de Parkinson, hacen algo más que trabajar uno al lado del otro: se asocian físicamente para que uno potencie discretamente la actividad del otro. Comprender esta asociación podría ayudar a diseñar fármacos que ajusten las señales cerebrales con mayor precisión y menos efectos secundarios.
Señales en la superficie celular
Muchos medicamentos de uso común actúan sobre una gran familia de proteínas en la superficie celular llamadas receptores acoplados a proteínas G, o GPCR. Cada GPCR detecta señales externas concretas y transmite el mensaje al interior de la célula. Dado que una sola neurona puede mostrar docenas de tipos de GPCR a la vez, los investigadores se han preguntado durante mucho tiempo cómo evitan estos receptores enviar mensajes mezclados. Una propuesta es que distintos GPCR se unan físicamente, formando pares o grupos mayores que comparten información. Pero si tales agrupamientos realmente influyen en el procesamiento de señales ha sido motivo de intenso debate.
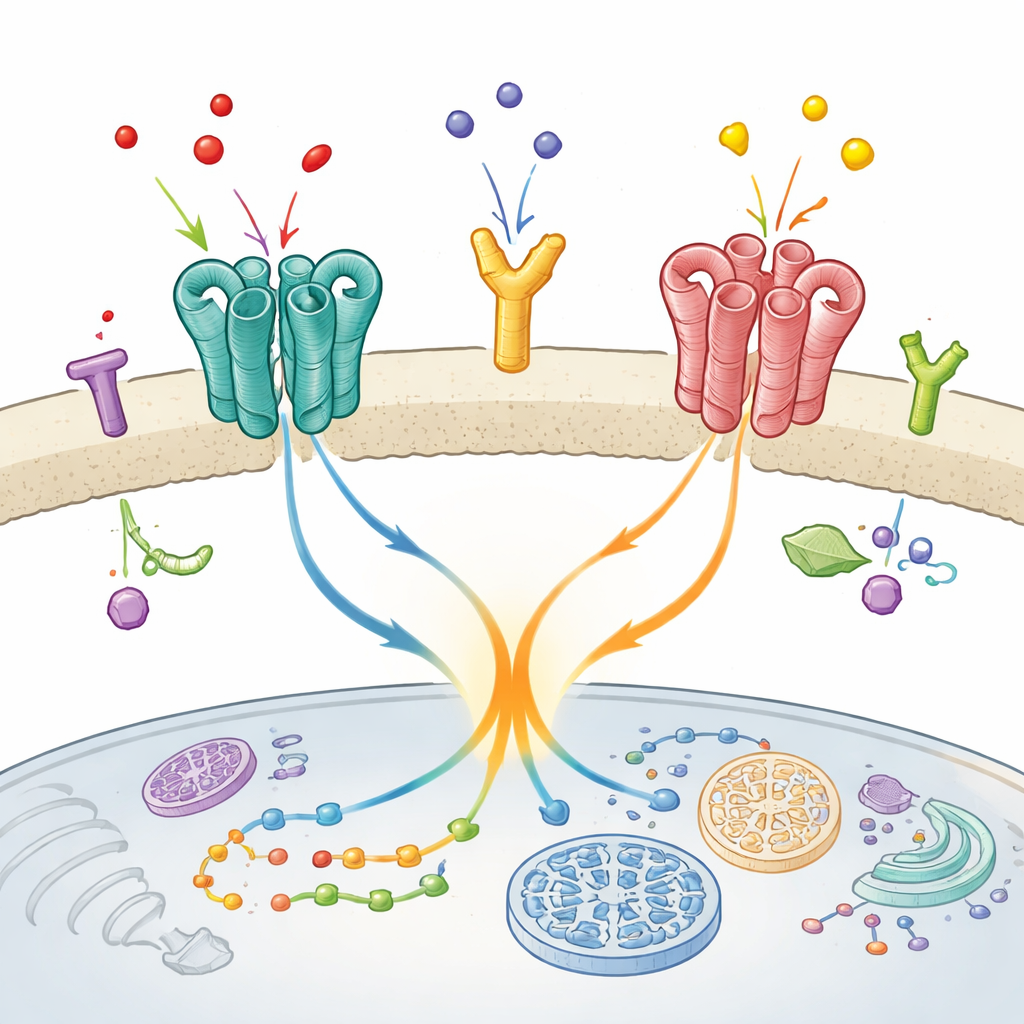
Una asociación sorprendente en el cerebro
Los investigadores se centraron en un dúo específico encontrado en regiones cerebrales implicadas en el estado de ánimo, la percepción y el movimiento: el receptor metabotrópico de glutamato mGlu2 y el receptor de serotonina 5-HT2A. Ambos son dianas de fármacos antipsicóticos, y trabajos anteriores sugerían que forman un par funcional en tejido cerebral vivo. Aquí, el equipo planteó dos preguntas clave: ¿estos receptores realmente se sitúan en contacto directo en la superficie celular y, de ser así, ese contacto físico cambia el comportamiento de mGlu2?
Demostrando que los receptores se tocan
Para ver si mGlu2 y 5-HT2A realmente se unen, los autores usaron células humanas cultivadas en el laboratorio y marcaron cada receptor con diminutos marcadores fluorescentes. Cuando las proteínas marcadas se acercan lo suficiente, la energía puede saltar de un marcador al otro, generando una señal medible. Estos experimentos mostraron una señal fuerte cuando estaban presentes ambos receptores, lo que indica que se agrupan en la superficie celular. El equipo utilizó después un ingenioso truco químico, introduciendo “anzuelo s” colocados de forma específica en cada receptor para que, al aproximarse, pudieran bloquearse entre sí. Los complejos entrecruzados resultantes confirmaron que mGlu2 y 5-HT2A contactan entre sí a través de secciones concretas incrustadas en la membrana celular.
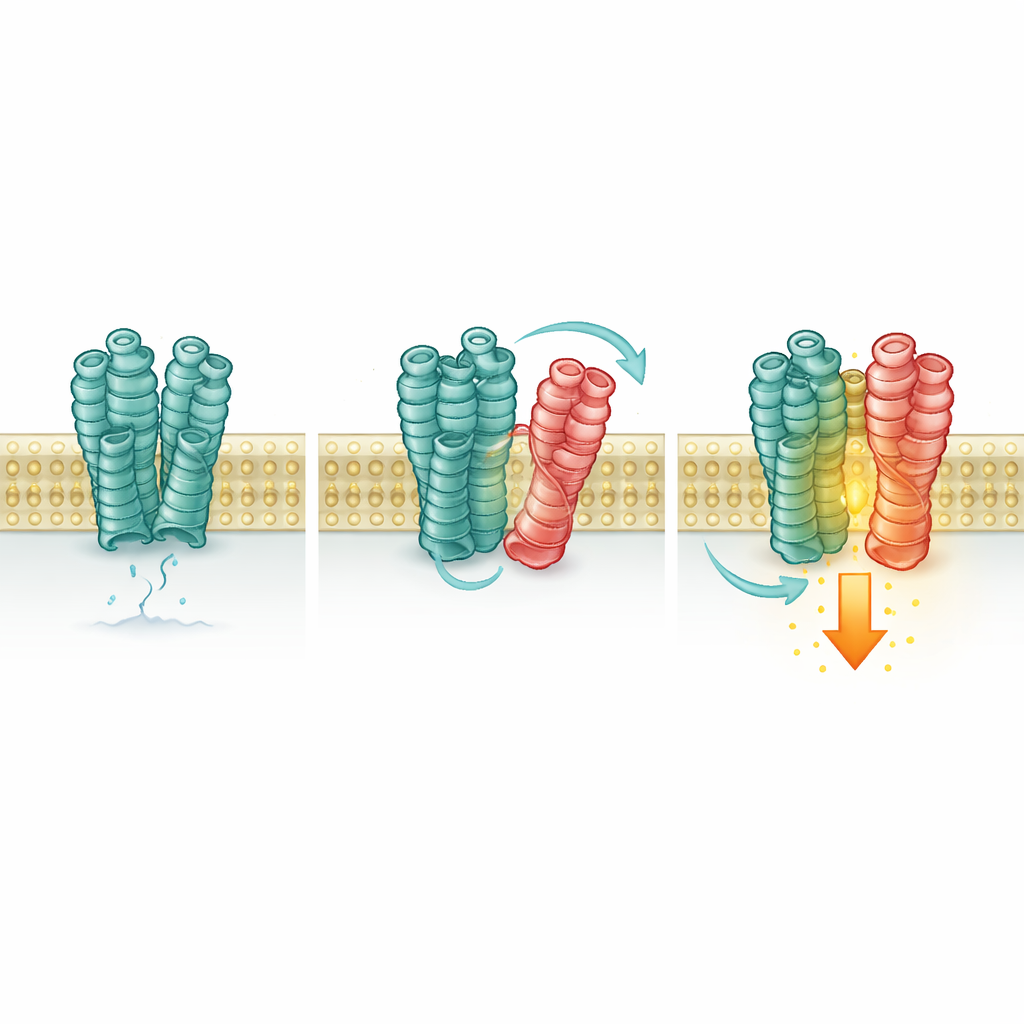
Un receptor activa discretamente a otro
A continuación, los científicos probaron si este contacto cambia la respuesta de mGlu2. Usando sensores fluorescentes sensibles y medidas bioquímicas, monitorizaron la conformación y el estado de actividad de mGlu2. Cuando 5-HT2A estaba presente, incluso sin añadir glutamato, más receptores mGlu2 cambiaron a su conformación “activada” y mostraron un pequeño pero significativo aumento de señalización dentro de la célula. Bloquear mGlu2 eliminó este efecto, pero activar o desactivar 5-HT2A con sus propios fármacos no lo hizo, y una variante mutante de 5-HT2A incapaz de activar su vía de señalización habitual todavía potenció a mGlu2. Esto significa que 5-HT2A actúa más como un soporte que como un interruptor activo: su mera presencia, y el contacto físico, estabiliza la forma activa de mGlu2.
Muchos otros socios se suman
La historia no termina con la serotonina. Los autores cribaron 44 GPCR adicionales para ver si podían influir de forma similar en mGlu2. Varios, incluidos múltiples receptores de dopamina y otro subtipo de serotonina, también empujaron a mGlu2 hacia su estado activo, mientras que otros tuvieron poco efecto. Un receptor de dopamina, D1, aumentó claramente la actividad basal de mGlu2 en ausencia de glutamato añadido, lo que vuelve a ser coherente con una asociación física que favorece la posición “encendida”. En contraste, un receptor muscarínico usado como control ni interactuó de forma intensa con mGlu2 ni alteró su actividad.
Por qué esto importa para los trastornos cerebrales
Este trabajo demuestra que ciertos receptores cerebrales hacen más que permanecer independientes esperando sus propias llaves químicas. Al formar pequeños ensamblajes, un receptor puede modular alostéricamente, o de forma indirecta, el comportamiento de otro. En el caso de mGlu2 y 5-HT2A, esto significa que los receptores vinculados a la serotonina pueden moldear cómo se procesan las señales de glutamato, incluso cuando no están señalando activamente. Dado que estas asociaciones de receptores están relacionadas con la esquizofrenia, la enfermedad de Parkinson y posiblemente otras condiciones, ofrecen un ángulo atractivo para el diseño de fármacos: medicamentos que se dirijan a un miembro de un par podrían diseñarse para modular la actividad del otro, proporcionando un control más sutil sobre circuitos cerebrales complejos.
Cita: Gai, S., Lin, L., Meng, J. et al. Allosteric activation of the glutamate receptor mGlu2 by the serotonin receptor 5-HT2A. Nat Commun 17, 3303 (2026). https://doi.org/10.1038/s41467-026-69939-3
Palabras clave: Heterómeros de GPCR, Receptor mGlu2, Receptor 5-HT2A, Modulación alostérica, Esquizofrenia