Clear Sky Science · pt
Ativação alostérica do receptor de glutamato mGlu2 pelo receptor de serotonina 5-HT2A
Como os porteiros das células cerebrais se unem
As células cerebrais estão cobertas por minúsculas proteínas “porteiras” que detectam mensageiros químicos como glutamato e serotonina. Este estudo mostra que duas dessas porteiras, historicamente ligadas à esquizofrenia e à doença de Parkinson, fazem mais do que atuar lado a lado: elas se unem fisicamente de modo que uma aumenta discretamente a atividade da outra. Compreender essa parceria pode ajudar cientistas a projetar drogas que ajustem sinais cerebrais com maior precisão e menos efeitos colaterais.
Sinais na superfície celular
Muitos medicamentos de uso comum atuam numa grande família de proteínas na superfície celular chamadas receptores acoplados à proteína G, ou GPCRs. Cada GPCR detecta sinais externos específicos e transmite a mensagem para dentro da célula. Como um único neurônio pode exibir dezenas de tipos de GPCR ao mesmo tempo, os pesquisadores há muito se perguntam como esses receptores evitam enviar mensagens confusas. Uma hipótese é que diferentes GPCRs se unem fisicamente, formando pares ou grupos maiores que compartilham informação. Mas se tais agrupamentos realmente importam para o processamento dos sinais tem sido alvo de intenso debate.
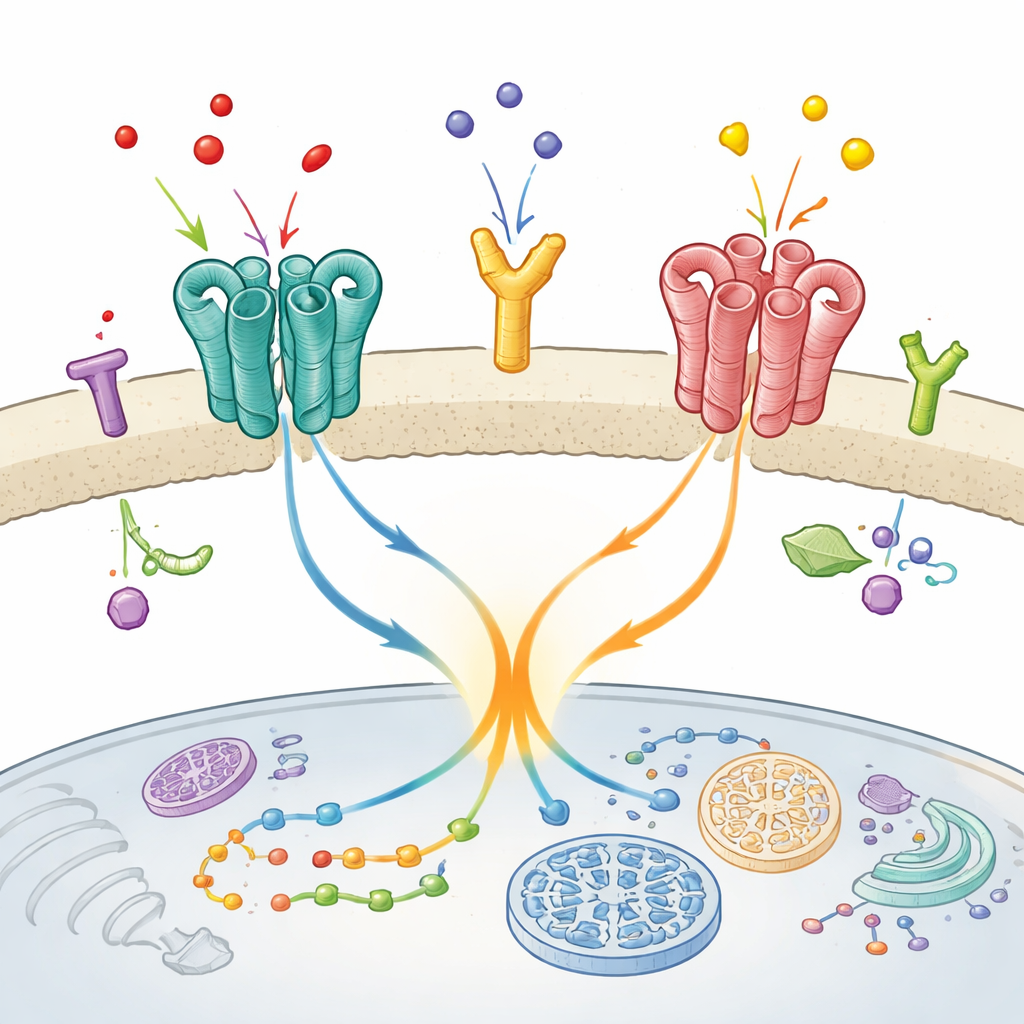
Uma parceria surpreendente no cérebro
Os pesquisadores focaram em um dúo específico encontrado em regiões cerebrais envolvidas no humor, percepção e movimento: o receptor metabotrópico de glutamato mGlu2 e o receptor de serotonina 5-HT2A. Ambos são alvos de antipsicóticos, e trabalhos anteriores sugeriram que eles formam um par funcional em tecido cerebral vivo. Aqui, a equipe perguntou duas questões-chave: esses receptores realmente ficam em contato direto na superfície celular e, em caso afirmativo, esse contato físico altera o comportamento do mGlu2?
Provando que os receptores se tocam
Para verificar se mGlu2 e 5-HT2A realmente se aproximam, os autores usaram células humanas cultivadas em laboratório e marcaram cada receptor com pequenos marcadores fluorescentes. Quando as proteínas marcadas se aproximam suficientemente, energia pode saltar de um marcador para o outro, gerando um sinal mensurável. Esses experimentos mostraram um sinal forte quando ambos os receptores estavam presentes, indicando que eles se agrupam na superfície celular. A equipe então usou um truque químico engenhoso, introduzindo “ganchos” colocados estrategicamente em cada receptor para que, quando próximos, pudessem ser travados juntos. Os complexos entrecruzados resultantes confirmaram que mGlu2 e 5-HT2A se contatam por meio de seções específicas enterradas na membrana celular.
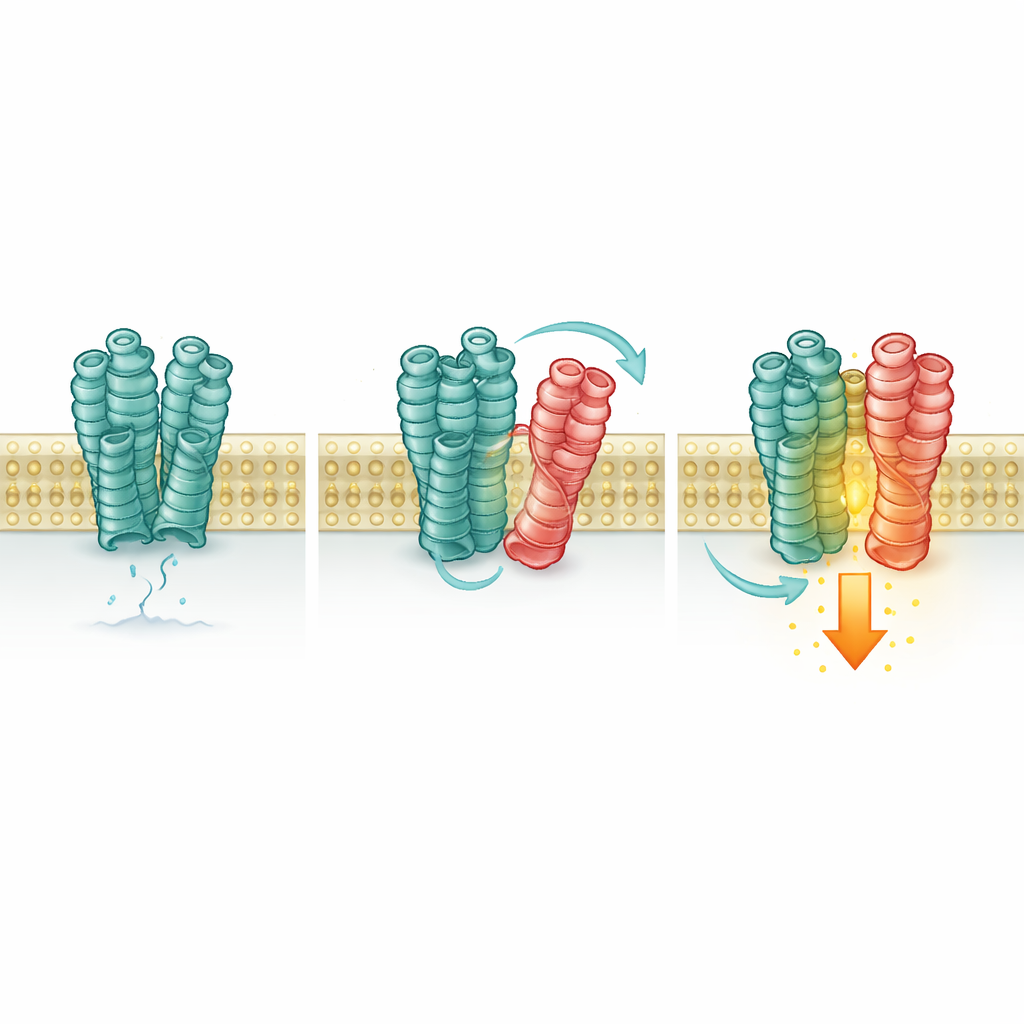
Um receptor ativa discretamente outro
Em seguida, os cientistas testaram se esse contato altera a resposta de mGlu2. Usando sensores fluorescentes sensíveis e leituras bioquímicas, monitoraram a conformação e o estado de atividade do mGlu2. Quando 5-HT2A estava presente, mesmo sem glutamato adicional, mais receptores mGlu2 mudavam para sua conformação “ativa” e exibiam um aumento pequeno, porém significativo, na sinalização intracelular. Bloquear o próprio mGlu2 eliminou esse efeito, mas ligar ou desligar o 5-HT2A com suas próprias drogas não o fez, e uma variante mutante do 5-HT2A incapaz de ativar sua via de sinalização habitual ainda aumentava o mGlu2. Isso significa que o 5-HT2A age mais como um suporte estabilizador do que como um interruptor ativo: sua mera presença, e o contato físico, estabilizam a forma ativa do mGlu2.
Muitos outros parceiros entram em cena
A história não termina com a serotonina. Os autores triaram outros 44 GPCRs para ver se eles poderiam influenciar o mGlu2 de maneira semelhante. Vários, incluindo múltiplos receptores de dopamina e outro subtipo de serotonina, também empurraram o mGlu2 em direção ao seu estado ativo, enquanto outros tiveram pouco efeito. Um receptor de dopamina, D1, aumentou claramente a atividade basal do mGlu2 na ausência de glutamato extra, novamente consistente com uma parceria física que favorece a posição “ativa”. Em contraste, um receptor muscarínico usado como controle nem interagiu fortemente com o mGlu2 nem alterou sua atividade.
Por que isso importa para transtornos cerebrais
Este trabalho demonstra que certos receptores cerebrais fazem mais do que ficar isolados esperando por suas próprias chaves químicas. Ao formar pequenas assembleias, um receptor pode, alostericamente ou indiretamente, ajustar o comportamento de outro. No caso de mGlu2 e 5-HT2A, isso significa que receptores ligados à serotonina podem moldar como sinais de glutamato são processados, mesmo quando não estão sinalizando ativamente. Como essas parcerias de receptores estão associadas à esquizofrenia, à doença de Parkinson e possivelmente a outras condições, elas oferecem um novo ângulo atraente para o desenho de fármacos: medicamentos que miram um membro do par podem ser concebidos para modular a atividade do outro, proporcionando um controle mais sutil sobre circuitos cerebrais complexos.
Citação: Gai, S., Lin, L., Meng, J. et al. Allosteric activation of the glutamate receptor mGlu2 by the serotonin receptor 5-HT2A. Nat Commun 17, 3303 (2026). https://doi.org/10.1038/s41467-026-69939-3
Palavras-chave: Heterômeros de GPCR, Receptor mGlu2, Receptor 5-HT2A, Modulação alostérica, Esquizofrenia