Clear Sky Science · pl
Allosteryczna aktywacja receptora glutaminianowego mGlu2 przez receptor serotoniny 5-HT2A
Jak strażnicy komórek nerwowych łączą siły
Komórki mózgowe pokryte są drobnymi białkowymi „strażnikami”, które wykrywają chemiczne przekaźniki, takie jak glutaminian i serotonina. Badanie to pokazuje, że dwaj tacy strażnicy, od dawna powiązani ze schizofrenią i chorobą Parkinsona, nie tylko działają obok siebie: fizycznie łączą się ze sobą, tak że jeden dyskretnie wzmacnia aktywność drugiego. Zrozumienie tego partnerstwa może pomóc naukowcom w projektowaniu leków, które precyzyjniej i z mniejszą ilością skutków ubocznych będą regulować sygnały mózgowe.
Sygnały na powierzchni komórki
Wiele powszechnie stosowanych leków działa na dużą rodzinę białek powierzchni komórkowej zwanych receptorami sprzężonymi z białkami G, czyli GPCR. Każdy GPCR wykrywa określone sygnały zewnętrzne i przekazuje informację do wnętrza komórki. Ponieważ pojedyncza komórka nerwowa może jednocześnie eksponować dziesiątki typów GPCR, badacze od dawna zastanawiali się, jak te receptory unikają mieszania sygnałów. Jedna z propozycji mówi, że różne GPCR łączą się fizycznie, tworząc pary lub większe zespoły, które dzielą się informacją. Jednak to, czy takie ugrupowania rzeczywiście mają znaczenie dla przetwarzania sygnałów, było przedmiotem ożywionej dyskusji.
Zaskakujące partnerstwo w mózgu
Naukowcy skupili się na konkretnym duecie występującym w obszarach mózgu zaangażowanych w nastrój, percepcję i ruch: receptorze metabotropowym glutaminianu mGlu2 oraz receptorze serotoniny 5-HT2A. Oba są celami leków przeciwpsychotycznych, a wcześniejsze prace sugerowały, że tworzą funkcjonalną parę w żywej tkance mózgowej. W tej pracy zespół postawił dwa kluczowe pytania: czy te receptory rzeczywiście stykają się bezpośrednio na powierzchni komórki i jeśli tak, czy ten kontakt zmienia zachowanie mGlu2?
Udowodnienie kontaktu receptorów
Aby sprawdzić, czy mGlu2 i 5-HT2A faktycznie się łączą, autorzy użyli hodowanych w laboratorium komórek ludzkich i oznaczyli każdy receptor maleńkimi znacznikami fluorescencyjnymi. Gdy oznaczone białka zbliżają się na odpowiednią odległość, energia może przeskoczyć z jednego markera na drugi, co daje mierzalny sygnał. Eksperymenty wykazały silny sygnał, gdy oba receptory były obecne, co wskazuje, że grupują się razem na powierzchni komórki. Zespół zastosował następnie sprytny chemiczny trik, wprowadzając specjalnie umieszczone „haczyki” w każdym receptorze, tak że gdy są blisko, można je zablokować razem. Powstałe skoniugatowane kompleksy potwierdziły, że mGlu2 i 5-HT2A stykają się przez konkretne fragmenty umieszczone w błonie komórkowej.
Jeden receptor dyskretnie włącza drugi
Następnie naukowcy sprawdzili, czy ten kontakt zmienia odpowiedź mGlu2. Korzystając z czułych sensorów fluorescencyjnych i biochemicznych odczytów, monitorowali konformację i stan aktywności mGlu2. Gdy 5-HT2A był obecny, nawet bez dodanego glutaminianu, więcej receptorów mGlu2 przechodziło w konformację „włączoną” i wykazywało niewielki, lecz istotny wzrost sygnalizacji wewnątrz komórki. Zablokowanie samego mGlu2 usuwało ten efekt, ale włączanie lub wyłączanie 5-HT2A za pomocą jego własnych leków nie miało takiego wpływu, a mutant 5-HT2A, który nie może aktywować swojego zwykłego szlaku sygnałowego, nadal potęgował mGlu2. Oznacza to, że 5-HT2A działa bardziej jak wspierające usztywnienie niż aktywny przełącznik: jego sama obecność i fizyczny kontakt stabilizują aktywną formę mGlu2.
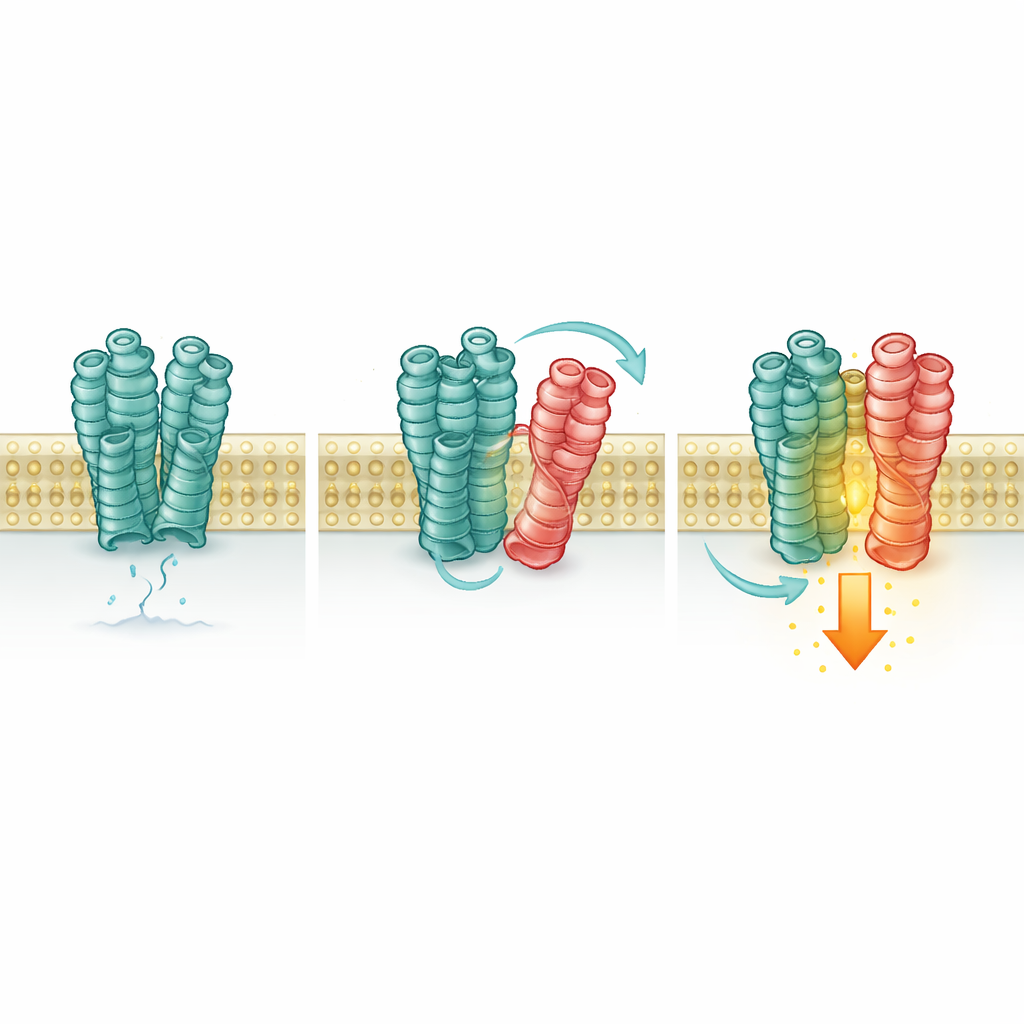
Wielu innych partnerów dołącza
Historia nie kończy się na serotoninowych receptorach. Autorzy przeskanowali 44 inne GPCR, aby sprawdzić, czy mogą w podobny sposób wpływać na mGlu2. Kilka z nich, w tym kilka receptorów dopaminowych i inny podtyp serotoniny, również pchnęło mGlu2 w kierunku stanu aktywnego, podczas gdy inne miały niewielki efekt. Jeden receptor dopaminy, D1, wyraźnie zwiększał aktywność podstawową mGlu2 w nieobecności dodatkowego glutaminianu, co ponownie jest zgodne z fizycznym partnerstwem sprzyjającym pozycji „włączonej”. Natomiast receptor muskarynowy użyty jako kontrola ani nie wchodził silnie w interakcję z mGlu2, ani nie zmieniał jego aktywności.
Dlaczego to ma znaczenie dla chorób mózgu
Praca ta pokazuje, że pewne receptory mózgowe robią więcej niż tylko niezależne oczekiwanie na swoje chemiczne klucze. Tworząc małe zespoły, jeden receptor może allosterycznie, czyli pośrednio, dostroić zachowanie drugiego. W przypadku mGlu2 i 5-HT2A oznacza to, że receptory powiązane z serotoniną mogą kształtować przetwarzanie sygnałów glutaminianowych, nawet gdy same nie prowadzą aktywnej sygnalizacji. Ponieważ te partnerstwa receptorowe wiążą się ze schizofrenią, chorobą Parkinsona i prawdopodobnie innymi schorzeniami, oferują atrakcyjny nowy kierunek w projektowaniu leków: leki celujące w jednego członka pary mogą być zaprojektowane tak, by modulować aktywność drugiego, zapewniając bardziej subtelną kontrolę nad złożonymi obwodami mózgowymi.
Cytowanie: Gai, S., Lin, L., Meng, J. et al. Allosteric activation of the glutamate receptor mGlu2 by the serotonin receptor 5-HT2A. Nat Commun 17, 3303 (2026). https://doi.org/10.1038/s41467-026-69939-3
Słowa kluczowe: heteromery GPCR, receptor mGlu2, receptor 5-HT2A, modulacja allosteryczna, schizofrenia