Clear Sky Science · tr
Serotonin reseptörü 5-HT2A tarafından glutamat reseptörü mGlu2'nin allosterik aktivasyonu
Beyin Hücresi Kapı Bekçileri Nasıl İş Birliği Yapıyor
Beyin hücrelerinin yüzeyi, glutamat ve serotonin gibi kimyasal haberci molekülleri algılayan küçük “kapı bekçisi” proteinlerle kaplıdır. Bu çalışma, şizofreni ve Parkinson hastalığıyla uzun süredir ilişkilendirilen iki böyle kapı bekçisinin yan yana çalışmaktan daha fazlasını yaptığını gösteriyor: biri, diğerinin aktivitesini sessizce artırmak için fiziksel olarak birleşiyor. Bu ortaklığı anlamak, bilim insanlarının beyin sinyallerini daha hassas ve daha az yan etkiyle ayarlayan ilaçlar tasarlamasına yardımcı olabilir.
Hücre Yüzeyindeki Sinyaller
Pek çok yaygın ilaç, G proteinine bağlı reseptörler ya da kısaca GPCR olarak adlandırılan büyük bir hücre yüzeyi protein ailesi üzerinde etki eder. Her GPCR belirli dış sinyalleri algılar ve mesajı hücre içine iletir. Tek bir nöron aynı anda onlarca farklı GPCR türünü gösterebildiğinden, araştırmacılar bu reseptörlerin karışık mesaj göndermekten nasıl kaçındığını uzun zamandır merak ediyor. Bir öneri, farklı GPCR'lerin fiziksel olarak bir araya gelerek çiftler veya daha büyük gruplar oluşturması ve bilgi paylaşmasıdır. Ne var ki bu tür gruplaşmaların sinyallerin işlenmesi üzerinde gerçekten önemli olup olmadığı tartışmalı kaldı.
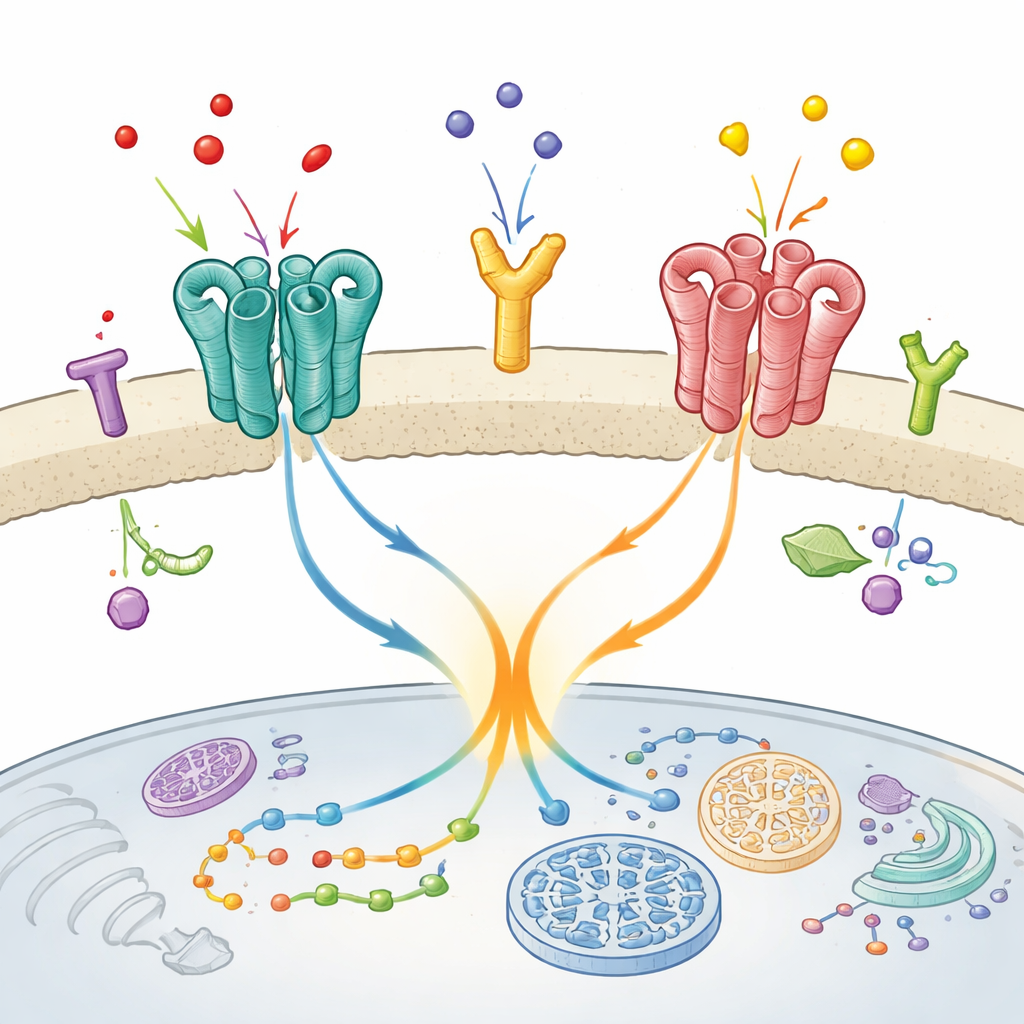
Beyinde Sürpriz Bir Ortaklık
Araştırmacılar duygu, algı ve hareketle ilgili beyin bölgelerinde bulunan belirli bir ikiliye odaklandı: metabotropik glutamat reseptörü mGlu2 ve serotonin reseptörü 5-HT2A. Her ikisi de antipsikotik ilaçların hedefidir ve önceki çalışmalar bunların canlı beyin dokusunda işlevsel bir çift oluşturduğunu düşündürmüştü. Burada ekip iki temel soruyu yöneltti: Bu reseptörler hücre yüzeyinde gerçekten doğrudan temas halinde mi bulunuyor ve eğer öyleyse bu fiziksel temas mGlu2'nin davranışını değiştiriyor mu?
Reseptörlerin Temas Ettiğini Kanıtlamak
mGlu2 ve 5-HT2A'nın gerçekten bir araya gelip gelmediğini görmek için yazarlar hücre kültüründe büyütülmüş insan hücrelerini kullandılar ve her bir reseptörü küçük floresan işaretleyicilerle etiketlediler. Etiketli proteinler yeterince yakın hareket ettiğinde, enerjinin bir işaretleyiciden diğerine atlamasıyla ölçülebilir bir sinyal oluşur. Bu deneyler, her iki reseptör var olduğunda güçlü bir sinyal gösterdi ve bunun hücre yüzeyinde kümelendiklerini işaret ettiği anlaşıldı. Ekip daha sonra akıllıca bir kimyasal numara kullanarak her iki reseptöre özel yerlere “kancalar” yerleştirdi; yakın olduklarında bu kancalar sayesinde birbirlerine kilitlenebiliyorlardı. Ortaya çıkan çapraz bağlanmış kompleksler, mGlu2 ve 5-HT2A'nın hücre zarı içinde gömülü belirli bölümler aracılığıyla birbirleriyle temas ettiğini doğruladı.
Bir Reseptör Sessizce Diğerini Açıyor
Sonra bilim insanları bu temasın mGlu2'nin yanıtını değiştirip değiştirmediğini test etti. Hassas floresan sensörler ve biyokimyasal ölçümler kullanarak mGlu2'nin şekil ve aktivite durumunu izlediler. 5-HT2A bulunduğunda, ek glutamat eklenmemiş olsa bile daha fazla mGlu2 reseptörü “açık” konformasyona kaydı ve hücre içindeki sinyalde küçük ama anlamlı bir artış gösterdi. mGlu2'nin kendisini engellemek bu etkiyi ortadan kaldırdı, fakat 5-HT2A'nın kendi ilaçlarıyla açılıp kapatılması etkiyi değiştirmedi ve olağan sinyal yolunu aktive edemeyen bir 5-HT2A mutantı yine de mGlu2'yi artırdı. Bu, 5-HT2A'nın aktif bir anahtar gibi değil, destekleyici bir kızak gibi davrandığını gösteriyor: sadece varlığı ve fiziksel teması, mGlu2'nin aktif formunu stabilize ediyor.
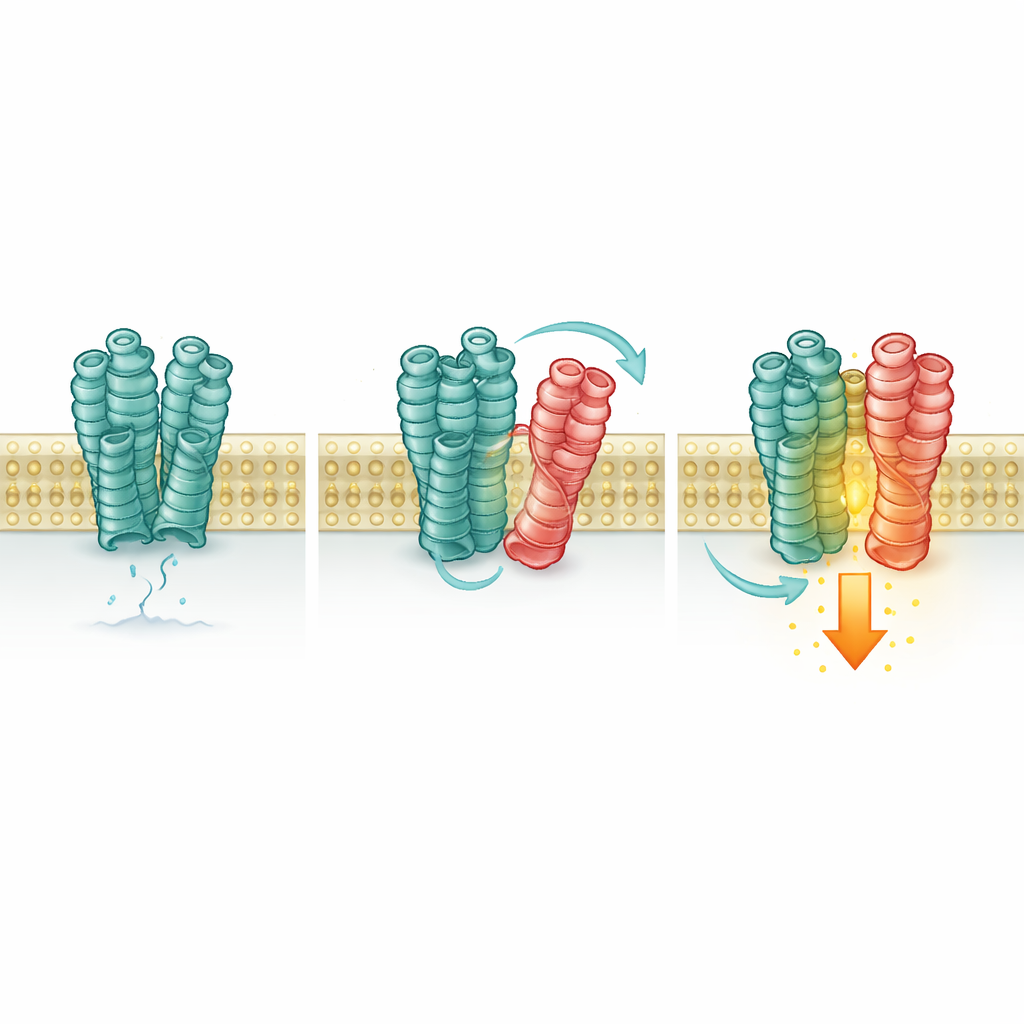
Çok Sayıda Başka Ortak da Dahil Oluyor
Hikâye sadece serotoninin ötesinde devam ediyor. Yazarlar, diğer 44 GPCR'yi tarayarak bunların mGlu2'yi benzer şekilde etkileyip etkileyemeyeceğine baktılar. Birkaçı, birden çok dopamin reseptörü ve başka bir serotonin alt türü dahil, mGlu2'yi aktif durumuna doğru itti; diğerleri ise az etki gösterdi. Bir dopamin reseptörü olan D1, ekstra glutamat yokluğunda mGlu2'nin bazal aktivitesini açıkça artırdı; bu da yine “açık” konumu tercih eden fiziksel bir ortaklığa işaret ediyor. Buna karşılık, kontrol amaçlı kullanılan bir muskarinik reseptör ne mGlu2 ile güçlü etkileşim gösterdi ne de onun aktivitesini değiştirdi.
Bunun Beyin Bozuklukları İçin Önemi
Bu çalışma, belirli beyin reseptörlerinin kendi kimyasal anahtarlarını bekleyerek yalnız başına oturmaktan daha fazlasını yaptığını gösteriyor. Küçük topluluklar oluşturarak bir reseptör, dolaylı yani allosterik yollarla diğerinin davranışını ayarlayabiliyor. mGlu2 ve 5-HT2A örneğinde, serotonine bağlı reseptörler aktif olarak sinyal göndermeseler bile glutamat sinyallerinin nasıl işleneceğini biçimlendirebiliyor. Bu reseptör ortaklıkları şizofreni, Parkinson hastalığı ve muhtemelen diğer durumlarla ilişkilendirildiğinden, ilaç tasarımı için çekici yeni bir yaklaşım sunuyor: Bir çiftin bir üyesini hedef alan ilaçlar, diğerinin aktivitesini de düzenleyecek biçimde tasarlanarak karmaşık beyin devreleri üzerinde daha ince ayarlı kontrol sağlayabilir.
Atıf: Gai, S., Lin, L., Meng, J. et al. Allosteric activation of the glutamate receptor mGlu2 by the serotonin receptor 5-HT2A. Nat Commun 17, 3303 (2026). https://doi.org/10.1038/s41467-026-69939-3
Anahtar kelimeler: GPCR heteromerleri, mGlu2 reseptörü, 5-HT2A reseptörü, allosterik modülasyon, şizofreni