Clear Sky Science · nl
Allosterische activatie van de glutamaatreceptor mGlu2 door de serotoninereceptor 5‑HT2A
Hoe poortwachters van hersencellen samenwerken
Hersencellen zijn bedekt met kleine “poortwachter”-eiwitten die chemische boodschappers zoals glutamaat en serotonine waarnemen. Deze studie laat zien dat twee van zulke poortwachters, lang in verband gebracht met schizofrenie en de ziekte van Parkinson, meer doen dan naast elkaar functioneren: ze vormen fysiek een partnerschap waarbij de ene stilletjes de activiteit van de andere versterkt. Inzicht in deze samenwerking kan onderzoekers helpen medicijnen te ontwerpen die hersensignalen gerichter bijsturen met minder bijwerkingen.
Signalen aan het celoppervlak
Veel algemeen gebruikte geneesmiddelen werken op een grote familie van eiwitten aan het celoppervlak die G-eiwitgekoppelde receptoren of GPCRs worden genoemd. Elke GPCR detecteert specifieke externe signalen en geeft het bericht door naar binnen in de cel. Omdat één zenuwcel tegelijk tientallen soorten GPCRs kan tonen, vragen onderzoekers zich al lang af hoe deze receptoren voorkomen dat er verwarrende, gemengde signalen worden verzonden. Een voorstel is dat verschillende GPCRs fysiek samenkomen, paren of grotere groepen vormen die informatie delen. Of zulke samenvoegingen echt gevolgen hebben voor signaalverwerking is echter fel bediscussieerd.
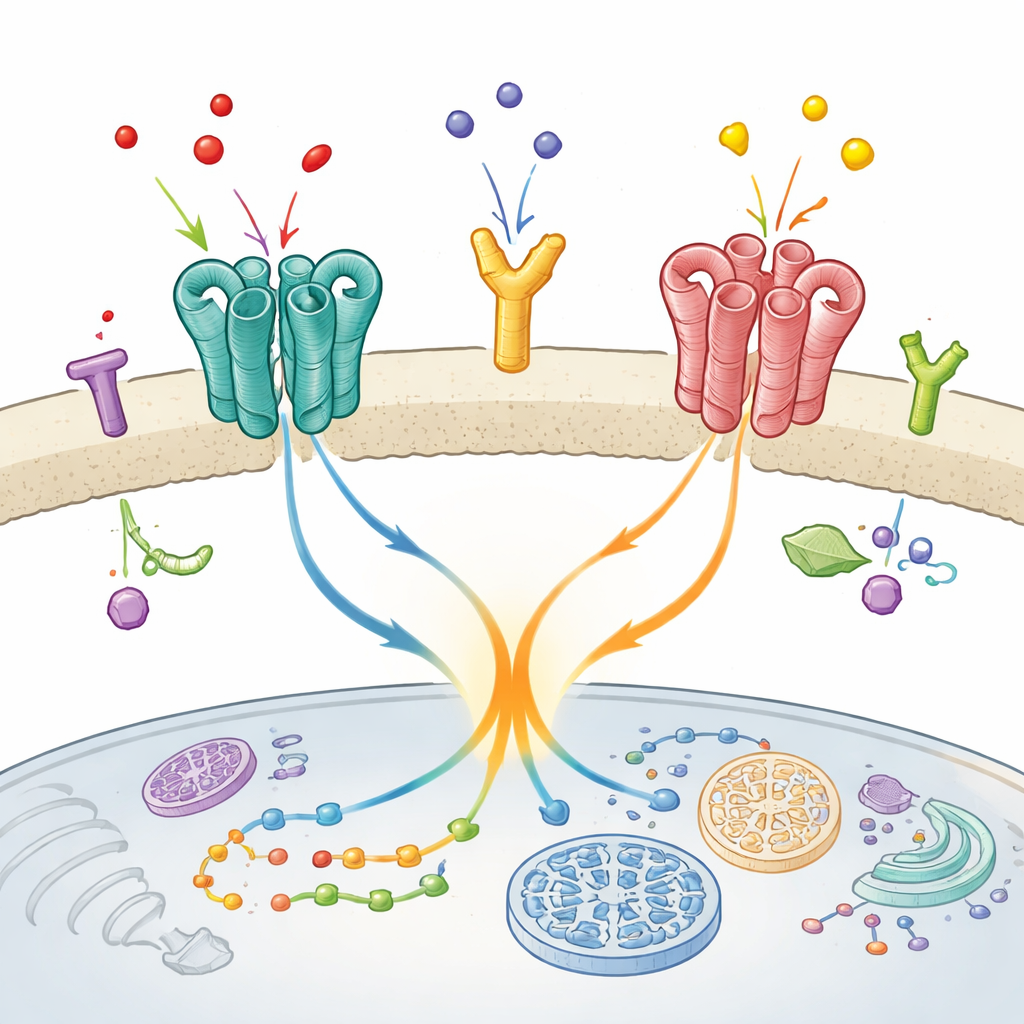
Een verrassende samenwerking in de hersenen
De onderzoekers richtten zich op een specifiek duo dat voorkomt in hersengebieden die betrokken zijn bij stemming, waarneming en beweging: de metabotrope glutamaatreceptor mGlu2 en de serotoninereceptor 5‑HT2A. Beide zijn doelwitten van antipsychotica, en eerder werk suggereerde dat ze in levend hersenweefsel een functioneel paar vormen. Hier stelden de onderzoekers twee kernvragen: liggen deze receptoren echt in direct contact op het celoppervlak, en zo ja, verandert dat fysieke contact de werking van mGlu2?
Aantonen dat de receptoren elkaar raken
Om te bepalen of mGlu2 en 5‑HT2A daadwerkelijk samenkomen, gebruikten de auteurs in het laboratorium gekweekte menselijke cellen en labelden elke receptor met kleine fluorescente markeringen. Wanneer de gemarkeerde eiwitten dicht genoeg naderen, kan energie van het ene merkteken naar het andere overspringen en een meetbaar signaal creëren. Deze experimenten lieten een sterk signaal zien wanneer beide receptoren aanwezig waren, wat erop wijst dat ze op het celoppervlak samenklonteren. Het team gebruikte vervolgens een slimme chemische truc: ze introduceerden speciaal geplaatste “haken” in elke receptor zodat ze, wanneer dicht bij elkaar, vergrendeld konden worden. De daardoor ontstane gekruiste complexen bevestigden dat mGlu2 en 5‑HT2A elkaar raken via specifieke gedeelten die in het celmembraan liggen.
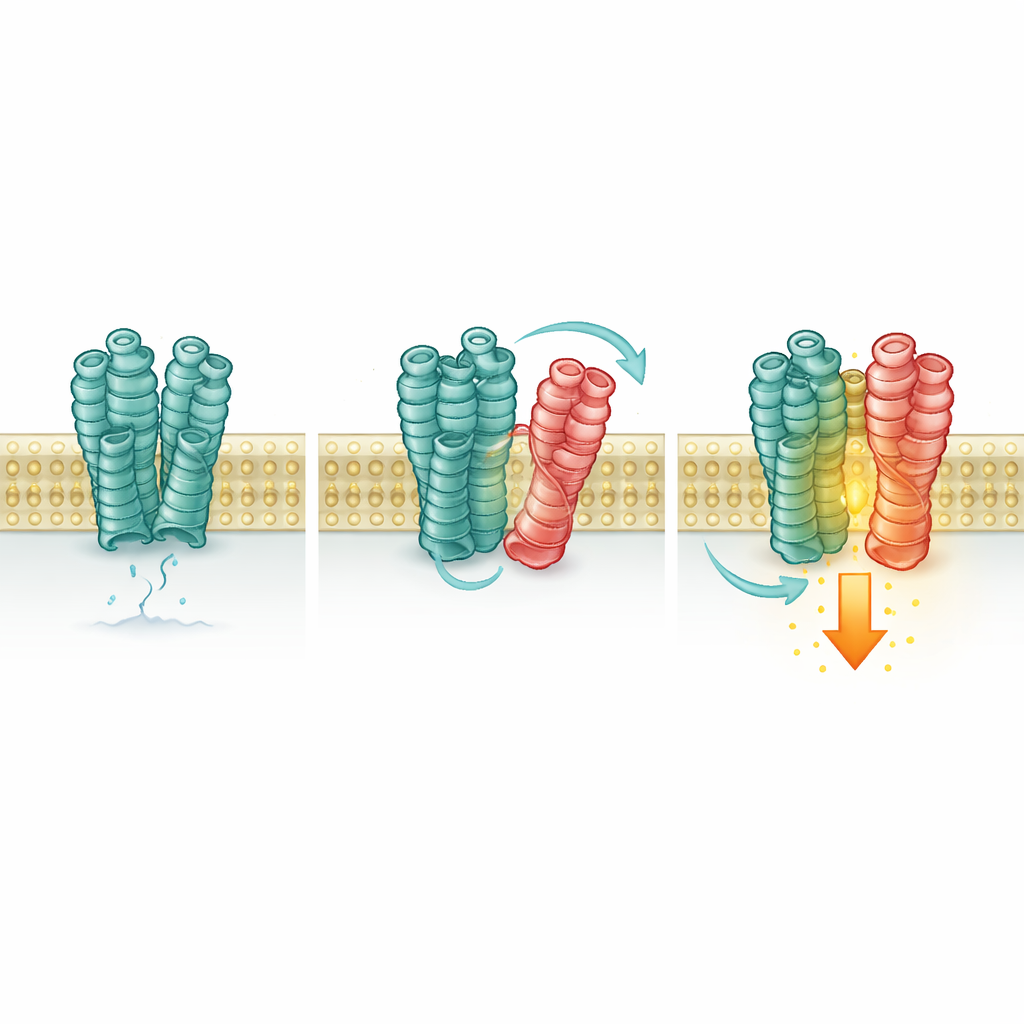
De ene receptor schakelt stilletjes een andere in
Vervolgens testten de wetenschappers of dit contact de respons van mGlu2 verandert. Met gevoelige fluorescente sensoren en biochemische metingen volgden ze de vorm en de activiteitsstatus van mGlu2. Wanneer 5‑HT2A aanwezig was, trad er, zelfs zonder extra glutamaat, een verschuiving op waarbij meer mGlu2-receptoren in hun “aan”-conformatie gingen en een kleine maar significante toename van signaaltransductie binnen de cel lieten zien. Het blokkeren van mGlu2 zelf verwijderde dit effect, maar het aan- of uitzetten van 5‑HT2A met zijn eigen medicijnen deed dat niet, en een mutant 5‑HT2A die zijn gebruikelijke signaalroute niet kan activeren versterkte mGlu2 nog steeds. Dit betekent dat 5‑HT2A meer fungeert als een ondersteunende beugel dan als een actieve schakelaar: haar loutere aanwezigheid en fysiek contact stabiliseert de actieve vorm van mGlu2.
Veel andere partners doen mee
Het verhaal stopt niet bij serotonine. De auteurs screeneden 44 andere GPCRs om te zien of zij mGlu2 op vergelijkbare wijze konden beïnvloeden. Meerdere receptoren, waaronder verschillende dopaminereceptoren en een andere serotonine-subtype, duwden mGlu2 eveneens richting zijn actieve toestand, terwijl anderen weinig effect hadden. Eén dopaminereceptor, D1, verhoogde duidelijk de basale activiteit van mGlu2 in afwezigheid van extra glutamaat, wat opnieuw consistent is met een fysiek partnerschap dat de “aan”-positie bevordert. Ter vergelijking had een muscarinereceptor die als controle diende noch sterke interactie met mGlu2 noch invloed op zijn activiteit.
Waarom dit belangrijk is voor hersenaandoeningen
Dit werk toont aan dat bepaalde hersenreceptoren meer doen dan onafhankelijk wachten op hun eigen chemische sleutel. Door kleine assemblages te vormen kan de ene receptor allosterisch, of indirect, het gedrag van een andere bijsturen. In het geval van mGlu2 en 5‑HT2A betekent dit dat serotonine‑gekoppelde receptoren kunnen bepalen hoe glutamaatsignalen worden verwerkt, zelfs wanneer ze zelf niet actief signaleren. Omdat deze receptorpartnerschappen verband houden met schizofrenie, de ziekte van Parkinson en mogelijk andere aandoeningen, bieden ze een aantrekkelijk nieuw perspectief voor medicijnontwerp: geneesmiddelen die zich op één lid van een paar richten, zouden zodanig kunnen worden ontwikkeld dat ze de activiteit van de andere moduleren en zo subtielere controle over complexe hersencircuits mogelijk maken.
Bronvermelding: Gai, S., Lin, L., Meng, J. et al. Allosteric activation of the glutamate receptor mGlu2 by the serotonin receptor 5-HT2A. Nat Commun 17, 3303 (2026). https://doi.org/10.1038/s41467-026-69939-3
Trefwoorden: GPCR heteromeren, mGlu2-receptor, 5-HT2A-receptor, allosterische modulatie, schizofrenie