Clear Sky Science · ru
Аллостерическая активация глутаматного рецептора mGlu2 рецептором серотонина 5-HT2A
Как «сторожи» клеточной мембраны объединяются в команды
Клетки мозга покрыты крошечными «сторожевыми» белками, которые улавливают химические передатчики, такие как глутамат и серотонин. В этом исследовании показано, что два таких белка, давно связанные с шизофренией и болезнью Паркинсона, делают не просто работу бок о бок: они физически объединяются, и один тихо усиливает активность другого. Понимание этого партнерства может помочь учёным разработать препараты, которые тоньше настраивают мозговые сигналы с большей точностью и меньшими побочными эффектами.
Сигналы на поверхности клетки
Многие широко применяемые лекарства действуют на большую семью белков на поверхности клетки, называемых рецепторами, сопряжёнными с G-белком, или GPCR. Каждый GPCR распознаёт определённые внешние сигналы и передаёт сообщение внутрь клетки. Поскольку одна нервная клетка может одновременно экспрессировать десятки типов GPCR, исследователи давно задаются вопросом, как эти рецепторы избегают сумбурной передачи сигналов. Одна из гипотез заключается в том, что разные GPCR физически объединяются, образуя пары или более крупные комплексы, которые обмениваются информацией. Тем не менее, имеет ли такое объединение реальное значение для обработки сигналов, оставалось предметом ожесточённых споров.
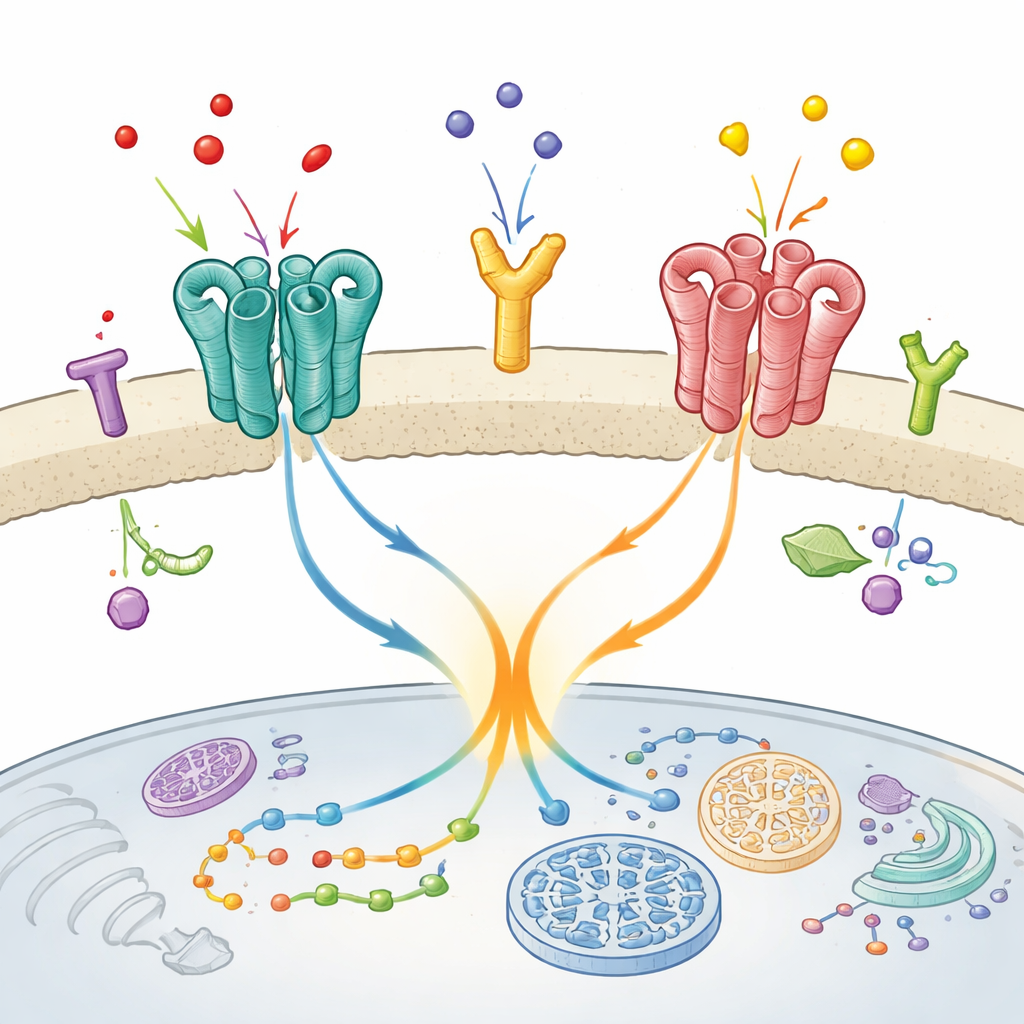
Неожиданное партнерство в мозге
Исследователи сосредоточились на конкретном дуэте, обнаруживаемом в областях мозга, вовлечённых в настроение, восприятие и движение: метаботропный глутаматный рецептор mGlu2 и серотониновый рецептор 5-HT2A. Оба являются мишенями антипсихотических препаратов, и предыдущие работы указывали на то, что они образуют функциональную пару в живой ткани мозга. В этой работе команда поставила два ключевых вопроса: действительно ли эти рецепторы находятся в непосредственном контакте на поверхности клетки, и если да, изменяет ли такой физический контакт поведение mGlu2?
Доказательства того, что рецепторы соприкасаются
Чтобы выяснить, действительно ли mGlu2 и 5-HT2A сближаются, авторы использовали выращенные в лаборатории человеческие клетки и пометили каждый рецептор крошечными флуоресцентными маркерами. Когда помеченные белки подходят достаточно близко, энергия может переходить от одного маркера к другому, создавая измеримый сигнал. Эти эксперименты показали сильный сигнал при наличии обоих рецепторов, что указывает на их кластеризацию на поверхности клетки. Команда затем применила хитрый химический приём: ввела в каждый рецептор специально расположенные «крючки», так что, оказавшись рядом, их можно было запереть вместе. Полученные перекрёстно-связанные комплексы подтвердили, что mGlu2 и 5-HT2A контактируют через определённые участки, погружённые в клеточную мембрану.
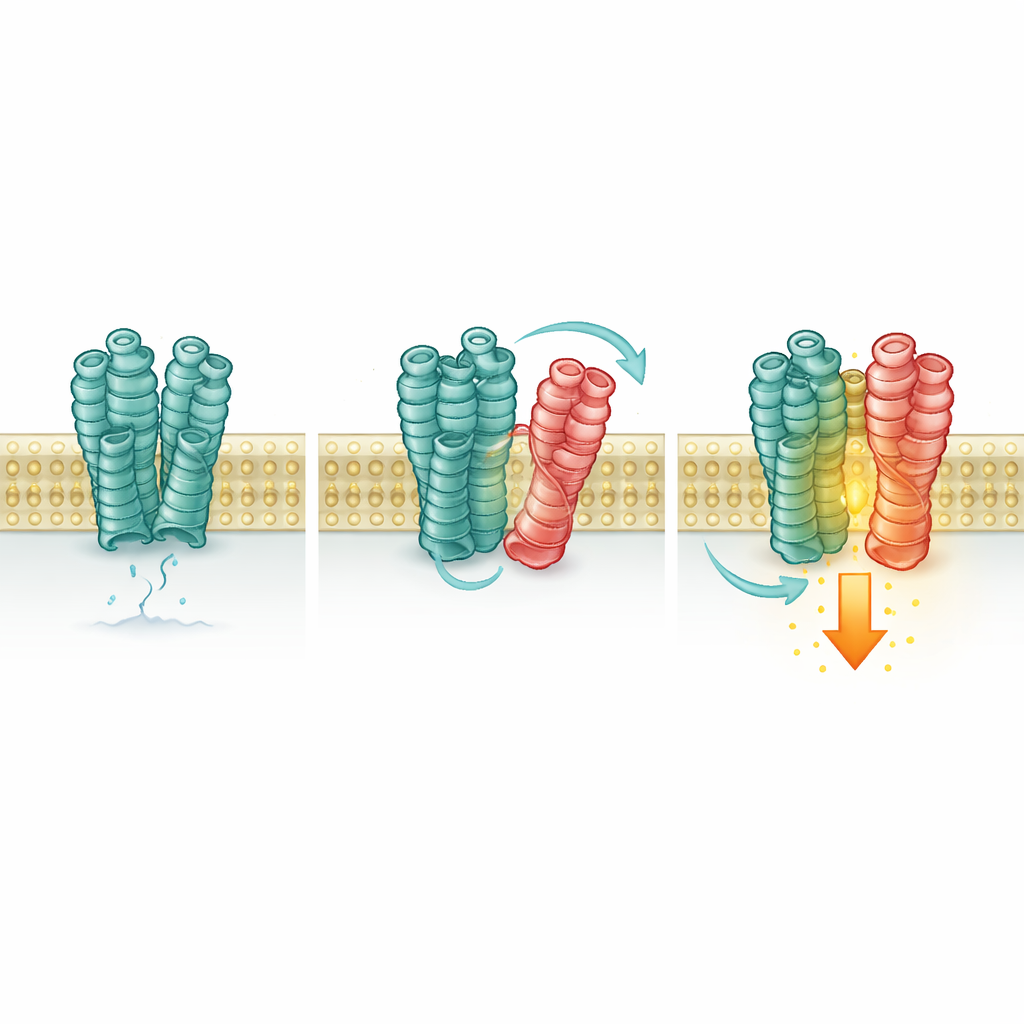
Один рецептор молча включает другой
Далее учёные проверили, меняет ли этот контакт ответ mGlu2. С помощью чувствительных флуоресцентных датчиков и биохимических показателей они отслеживали конформацию и состояние активности mGlu2. В присутствии 5-HT2A, даже без добавления глутамата, больше рецепторов mGlu2 переходило в их «включённую» конформацию и демонстрировало небольшое, но значимое повышение сигнальной активности внутри клетки. Блокирование самого mGlu2 устраняло этот эффект, тогда как включение или выключение 5-HT2A его не отменяло, а мутант 5-HT2A, неспособный активировать свой обычный сигнальный путь, всё равно усиливал mGlu2. Это означает, что 5-HT2A действует скорее как опорный брус, чем как активный переключатель: его простое присутствие и физический контакт стабилизируют активную форму mGlu2.
Много других партнёров подключаются
История на этом не заканчивается серотонином. Авторы протестировали 44 других GPCR, чтобы выяснить, могут ли они аналогичным образом влиять на mGlu2. Несколько из них, в том числе несколько дофаминовых рецепторов и другой подтип серотонинового рецептора, также смещали mGlu2 в направлении его активного состояния, тогда как другие оказывали мало влияния. Один дофаминовый рецептор, D1, явно повышал базовую активность mGlu2 в отсутствие дополнительного глутамата, что снова согласуется с физическим партнёрством, способствующим «включённому» положению. Напротив, мускариновый рецептор, использованный как контроль, не взаимодействовал сильно с mGlu2 и не изменял его активности.
Почему это важно для заболеваний мозга
Эта работа показывает, что некоторые рецепторы мозга делают больше, чем просто сидят отдельно в ожидании своих химических ключей. Образуя небольшие комплексы, один рецептор может аллостерически, или косвенно, настраивать поведение другого. В случае mGlu2 и 5-HT2A это означает, что рецепторы, связанные с серотонином, могут формировать то, как обрабатываются глутаматные сигналы, даже когда сами они активно не сигнализируют. Поскольку эти рецепторные партнёрства связаны с шизофренией, болезнью Паркинсона и, возможно, другими состояниями, они предлагают привлекательный новый подход для разработки лекарств: препараты, нацеленные на одного члена пары, можно сконструировать так, чтобы модулировать активность другого, обеспечивая более тонкий контроль над сложными мозговыми цепями.
Цитирование: Gai, S., Lin, L., Meng, J. et al. Allosteric activation of the glutamate receptor mGlu2 by the serotonin receptor 5-HT2A. Nat Commun 17, 3303 (2026). https://doi.org/10.1038/s41467-026-69939-3
Ключевые слова: гетеромеры GPCR, рецептор mGlu2, рецептор 5-HT2A, аллостерическая модуляция, шизофрения