Clear Sky Science · he
הפעלת אלוסטרית של קולטני הגלוטמט mGlu2 על ידי קולטון הסרוטונין 5-HT2A
איך שומרי הסף של תאי המוח משתפים פעולה
תאי המוח מצופים בחלבוני "שומרי סף" זעירים החשים מוליכי אותות כימיים כמו גלוטמט וסרוטונין. מחקר זה מראה ששני שומרי סף כאלה, המקושרים מזה זמן לסקיזופרניה ולמחלת פרקינסון, עושים יותר מאשר לפעול זה לצד זה: הם מצטרפים פיזית כך שאחד משפר בדממה את פעילותו של השני. הבנת שותפות זו עשויה לסייע למדענים לעצב תרופות שמדייקות את אותות המוח ביתר דיוק ולמזער תופעות לוואי.
אותות על פני התא
תרופות רבות פועלות על משפחה ענקית של חלבוני־ממברנה הנקראים קולטני G‑חלבון, או GPCR. כל GPCR מזהה אות חיצוני מסוים ומעביר את המסר לתוך התא. מאחר שתא עצב יחיד יכול להציג בו־זמנית עשרות סוגי GPCR, חוקרים תהו זמן רב כיצד קולטן אחד לא יבלבל את איתותיו עם אחרים. הצעה אחת היא שקולטנים שונים מצטרפים פיזית, יוצרים זוגות או קבוצות גדולות יותר שמשתפות מידע. אולם האם סוגי צירופים כאלה באמת משפיעים על עיבוד האותות הייתה שאלה שנויה במחלוקת.
שותפות מפתיעה במוח
החוקרים התמקדו בצמד ספציפי שנמצא באזורים מוחיים המעורבים במצב רוח, בתפיסה ובתנועה: הקולטן מטבוטרופי לגלוטמט mGlu2 וקולטן הסרוטונין 5‑HT2A. שניהם הם מטרות של תרופות אנטי־פסיכוטיות, ועבודות קודמות הציעו שהם יוצרים זוג תפקודי ברקמות מוח חיות. כאן הצוות חקר שתי שאלות מרכזיות: האם קולטנים אלה באמת יושבים במגע ישיר על פני התא, ואם כן — האם מגע פיזי כזה משנה את התנהגות mGlu2?
הוכחת המגע בין הקולטנים
כדי לבדוק האם mGlu2 ו‑5‑HT2A אכן מתקרבים זה לזה השתמשו החוקרים בתאי אדם שגודלו במעבדה וסימנו כל קולטן בסמנים פלאורוסנטיים זעירים. כשהחלבונים המסומנים מתקרבים מספיק, אנרגיה יכולה לעבור ממסמן למסמן השני ולטעון איתות שניתן למדוד. הניסויים הראו אות חזק כאשר שני הקולטנים היו נוכחים, מה שמעיד על צרופות על פני התא. הצוות השתמש לאחר מכן במכחול כימי יצירתי, הכניס "מקרסים" ממוקמים במדויק לכל קולטן כך שכאשר הם קרובים ניתן לנעולם יחד. המורכבים החוצים שנוצרו אישרו ש‑mGlu2 ו‑5‑HT2A באים במגע דרך מקטעים ספציפיים שקבורים בממברנת התא.
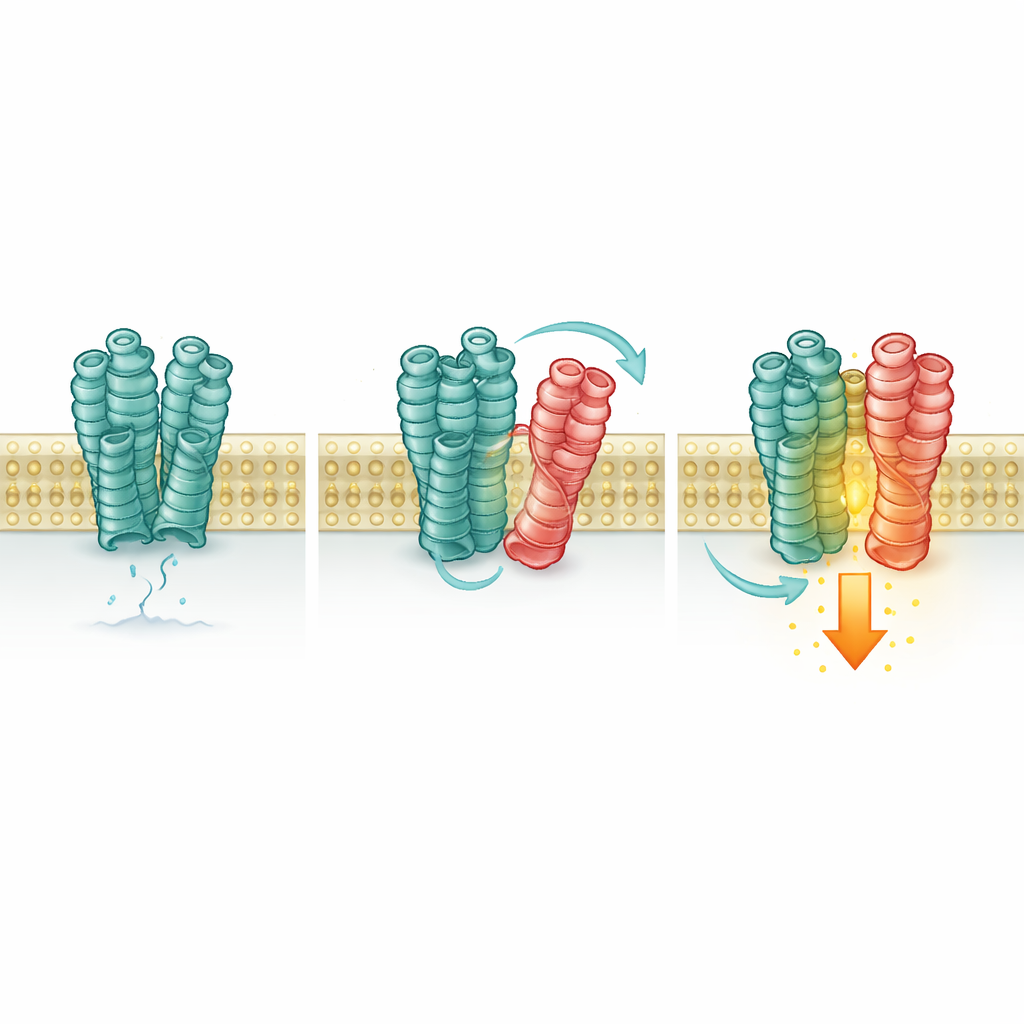
קולטן אחד מדליק בדממה את השני
בהמשך בדקו המדענים האם מגע זה משנה את תגובת mGlu2. בעזרת חיישנים פלאורוסנטיים רגישים ותוצאות ביוכימיות הם ניטרו את צורתו ומצב הפעילות של mGlu2. כאשר 5‑HT2A היה נוכח, אפילו ללא גלוטמט נוסף, יותר מולקולות mGlu2 עברו לקונפורמציה ה"פעילה" והראו עלייה קטנה אך משמעותית באיתות בתוך התא. חסימת mGlu2 עצמה הסירה השפעה זו, אך הפעלת או כיבוי 5‑HT2A בעזרת תרופותיו לא עשתה זאת, וגרסה מוזוטה של 5‑HT2A שלא יכולה להפעיל את מסלול האיתות הרגיל שלה עדיין הגברה את mGlu2. משמעות הדבר היא ש‑5‑HT2A מתנהג יותר כמו תומך מאשר מתג פעיל: נוכחותו והמגע הפיזי מייצבים את הצורה הפעילה של mGlu2.
עוד שותפים מצטרפים
הסיפור אינו מסתיים בסרוטונין. המחברוּת סרקו 44 GPCRים נוספים כדי לבדוק האם גם הם יכולים להשפיע בדומה על mGlu2. כמה מהם, כולל מספר קולטני דופמין ותת‑סוג נוסף של סרוטונין, גם דחפו את mGlu2 לעבר מצבו הפעיל, בעוד שאחרים השפיעו מעט. קולטן דופמין אחד, D1, הגדיל בבירור את פעילות הבסיס של mGlu2 בהיעדר גלוטמט נוסף, שוב בהתאמה לשותפות פיזית המעדיפה את המצב ה"מופעל". לעומת זאת, קולטן מוסקריני שנבחר כבקרה לא קיים אינטראקציה חזקה עם mGlu2 ולא שינה את פעילותו.
מדוע זה חשוב להפרעות מוחיות
עבודה זו מראה שקולטנים מסוימים במוח עושים יותר מלהמתין באופן עצמאי למפתחות הכימיה שלהם. באמצעות יצירת בצירופים קטנים, קולטן אחד יכול באופן אלוסטרי, כלומר בעקיפין, לכוונן את התנהגותו של אחר. במקרה של mGlu2 ו‑5‑HT2A, המשמעות היא שקולטני הקשורים לסרוטונין יכולים לעצב איך אותות גלוטמט מעובדים, אפילו כאשר הם עצמם אינם באיתות פעיל. מכיוון ששותפויות קולטן אלה קשורות לסקיזופרניה, למחלת פרקינסון ואולי למצבים אחרים, הן מציעות זווית חדשה ומפתה לעיצוב תרופתי: תרופות שממוקדות על אחד מבני הזוג עשויות להיות מתוכננות כך שישנו בעדינות את פעילותו של האחר, ויאפשרו שליטה עדינה יותר במעגלי מוח מסובכים.
ציטוט: Gai, S., Lin, L., Meng, J. et al. Allosteric activation of the glutamate receptor mGlu2 by the serotonin receptor 5-HT2A. Nat Commun 17, 3303 (2026). https://doi.org/10.1038/s41467-026-69939-3
מילות מפתח: הטמרים הטרומריים של GPCR, קולטן mGlu2, קולטן 5-HT2A, מודולציה אלוסטרית, סקיזופרניה