Clear Sky Science · it
Attivazione allosterica del recettore del glutammato mGlu2 da parte del recettore della serotonina 5-HT2A
Come i guardiani delle cellule cerebrali fanno squadra
Le cellule cerebrali sono rivestite da minuscole proteine “guardiane” che rilevano messaggeri chimici come il glutammato e la serotonina. Questo studio mostra che due di questi guardiani, a lungo collegati alla schizofrenia e al morbo di Parkinson, fanno più che lavorare fianco a fianco: si associano fisicamente in modo che uno potenzi discretamente l’attività dell’altro. Comprendere questa collaborazione potrebbe aiutare gli scienziati a progettare farmaci che modulano i segnali cerebrali con maggiore precisione e meno effetti collaterali.
Segnali sulla superficie cellulare
Molti farmaci di uso comune agiscono su una vasta famiglia di proteine di superficie chiamate recettori accoppiati a proteine G, o GPCR. Ogni GPCR rileva segnali esterni particolari e trasmette il messaggio all’interno della cellula. Poiché una singola cellula nervosa può esporre dozzine di tipi di GPCR contemporaneamente, i ricercatori si sono a lungo chiesti come questi recettori evitino di inviare messaggi confusi. Una proposta è che diversi GPCR si uniscano fisicamente, formando coppie o gruppi più grandi che condividono informazioni. Ma se tali aggregazioni influenzino davvero l’elaborazione dei segnali è stato oggetto di acceso dibattito.
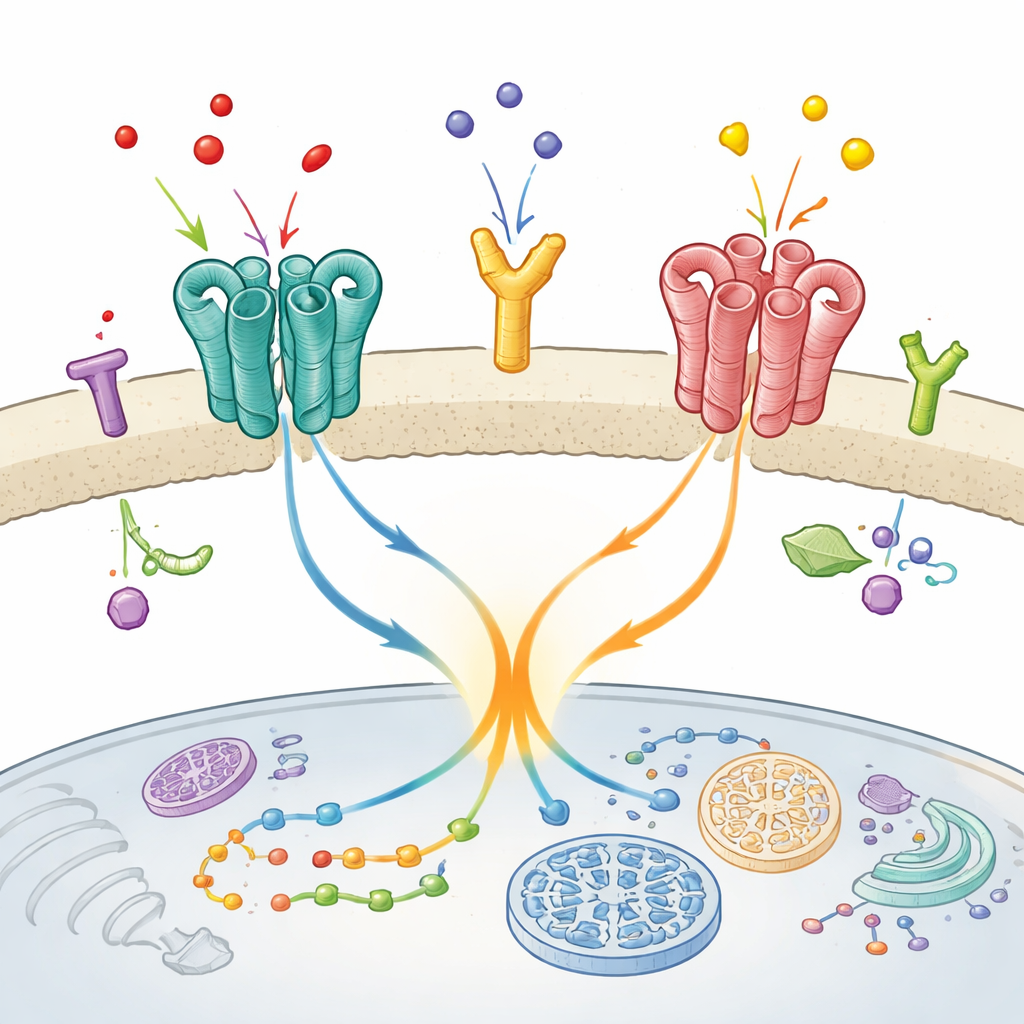
Una sorprendente collaborazione nel cervello
I ricercatori si sono concentrati su un duo specifico presente in regioni cerebrali coinvolte nell’umore, nella percezione e nel movimento: il recettore metabotropico del glutammato mGlu2 e il recettore della serotonina 5-HT2A. Entrambi sono bersagli di farmaci antipsicotici, e lavori precedenti avevano suggerito che formassero una coppia funzionale nei tessuti cerebrali vivi. Qui, il team si è posto due domande chiave: questi recettori si trovano davvero in contatto diretto sulla superficie cellulare e, in caso affermativo, quel contatto fisico altera il comportamento di mGlu2?
Dimostrare che i recettori si toccano
Per verificare se mGlu2 e 5-HT2A si associano realmente, gli autori hanno usato cellule umane coltivate in laboratorio e hanno marcato ciascun recettore con piccoli indicatori fluorescenti. Quando le proteine marcate si avvicinano abbastanza, l’energia può passare da un marcatore all’altro, generando un segnale misurabile. Questi esperimenti hanno mostrato un segnale forte quando entrambi i recettori erano presenti, indicando che si raggruppano sulla superficie cellulare. Il team ha quindi usato un espediente chimico ingegnoso, introducendo “uncini” appositamente posizionati in ciascun recettore così che, quando vicini, potessero essere bloccati insieme. I complessi reticolati risultanti hanno confermato che mGlu2 e 5-HT2A entrano in contatto attraverso sezioni specifiche sepolte nella membrana cellulare.
Un recettore accende discretamente un altro
Successivamente, gli scienziati hanno testato se questo contatto modifica la risposta di mGlu2. Usando sensori fluorescenti sensibili e letture biochimiche, hanno monitorato la conformazione e lo stato di attività di mGlu2. Quando 5-HT2A era presente, anche senza aggiunta di glutammato, un numero maggiore di recettori mGlu2 passava alla loro conformazione “attivata” e mostrava un piccolo ma significativo aumento della segnalazione intracellulare. Bloccare direttamente mGlu2 rimuoveva questo effetto, mentre attivare o spegnere 5-HT2A con i suoi farmaci non lo faceva, e una variante mutante di 5-HT2A incapace di attivare la sua normale via di segnalazione aumentava comunque mGlu2. Ciò significa che 5-HT2A si comporta più come un sostegno di supporto che come un interruttore attivo: la sua semplice presenza, e il contatto fisico, stabilizza la forma attiva di mGlu2.
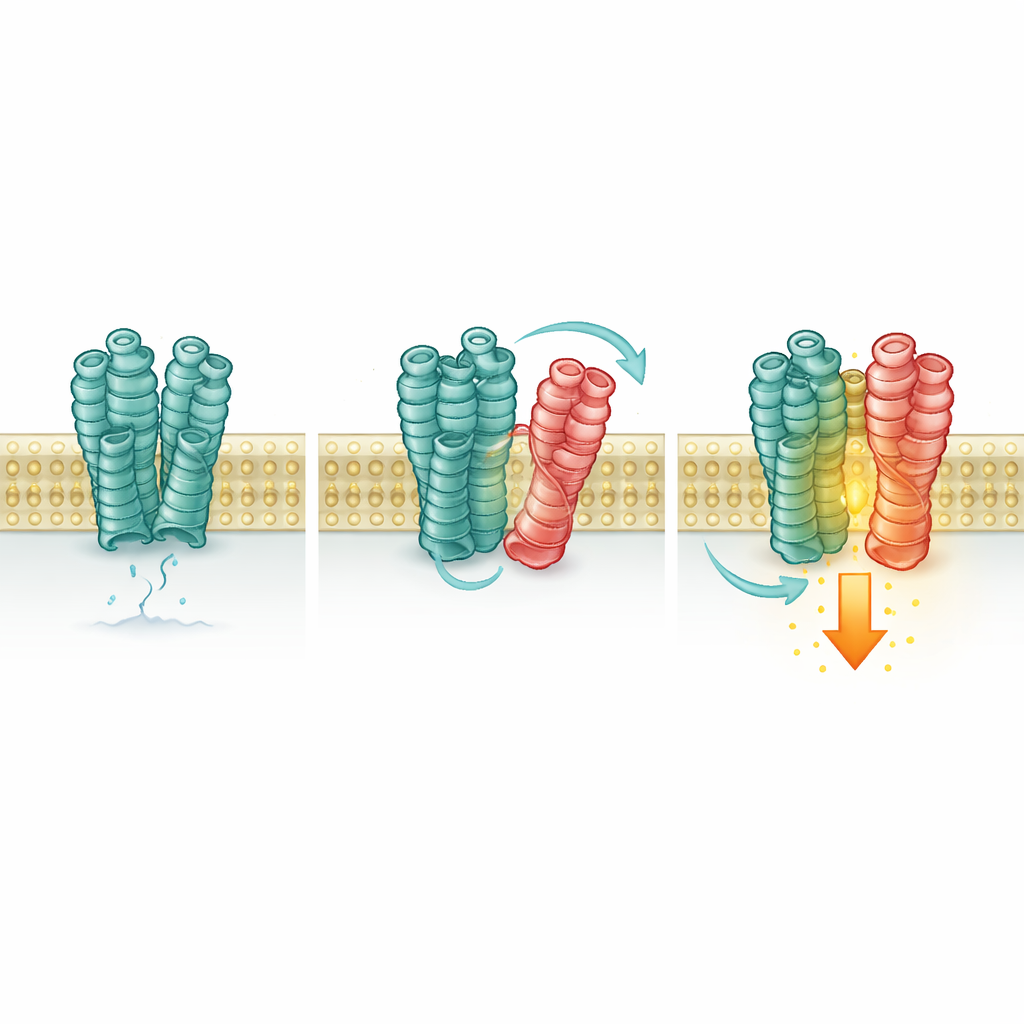
Molti altri partner si uniscono
La storia non finisce con la serotonina. Gli autori hanno esaminato 44 altri GPCR per vedere se potessero influenzare mGlu2 in modo simile. Diversi, inclusi più recettori della dopamina e un altro sottotipo di serotonina, hanno spinto mGlu2 verso il suo stato attivo, mentre altri hanno avuto scarso effetto. Un recettore della dopamina, D1, ha chiaramente aumentato l’attività basale di mGlu2 in assenza di glutammato extra, coerente ancora una volta con una partnership fisica che favorisce la posizione “accesa”. Al contrario, un recettore muscarinico usato come controllo né interagiva fortemente con mGlu2 né ne alterava l’attività.
Perché questo conta per i disturbi cerebrali
Questo lavoro mostra che certi recettori cerebrali fanno più che restare indipendenti in attesa delle loro chiavi chimiche. Formando piccoli assemblaggi, un recettore può allostericamente, cioè indirettamente, modulare il comportamento di un altro. Nel caso di mGlu2 e 5-HT2A, ciò significa che i recettori legati alla serotonina possono modellare il modo in cui i segnali del glutammato vengono elaborati, anche quando non sono essi stessi attivamente attivati. Poiché queste partnership tra recettori sono collegate a schizofrenia, morbo di Parkinson e probabilmente ad altre condizioni, offrono un nuovo e interessante punto di vista per la progettazione di farmaci: farmaci che prendono di mira un membro della coppia potrebbero essere concepiti per modulare l’attività dell’altro, fornendo un controllo più sottile sui circuiti cerebrali complessi.
Citazione: Gai, S., Lin, L., Meng, J. et al. Allosteric activation of the glutamate receptor mGlu2 by the serotonin receptor 5-HT2A. Nat Commun 17, 3303 (2026). https://doi.org/10.1038/s41467-026-69939-3
Parole chiave: eteromeri GPCR, recettore mGlu2, recettore 5-HT2A, modulazione allosterica, schizofrenia