Clear Sky Science · fr
Activation allostérique du récepteur du glutamate mGlu2 par le récepteur de la sérotonine 5‑HT2A
Comment les gardiens des cellules cérébrales font équipe
Les cellules cérébrales sont recouvertes de minuscules protéines « gardiennes » qui détectent des messagers chimiques comme le glutamate et la sérotonine. Cette étude montre que deux de ces gardiennes, longtemps associées à la schizophrénie et à la maladie de Parkinson, font plus que fonctionner côte à côte : elles s’associent physiquement de sorte que l’une augmente discrètement l’activité de l’autre. Comprendre ce partenariat pourrait aider les chercheurs à concevoir des médicaments qui ajustent les signaux cérébraux avec une plus grande précision et moins d’effets secondaires.
Signaux à la surface cellulaire
Beaucoup de médicaments courants agissent sur une vaste famille de protéines de surface appelées récepteurs couplés aux protéines G, ou GPCR. Chaque GPCR détecte des signaux externes particuliers et transmet l’information à l’intérieur de la cellule. Comme une seule cellule nerveuse peut afficher des dizaines de types de GPCR simultanément, les chercheurs se sont longtemps demandé comment ces récepteurs évitent d’envoyer des messages contradictoires. Une hypothèse est que différents GPCR se rejoignent physiquement, formant des paires ou des groupes plus larges qui partagent l’information. Mais la question de savoir si ces assemblages comptent réellement pour le traitement des signaux a été très débattue.
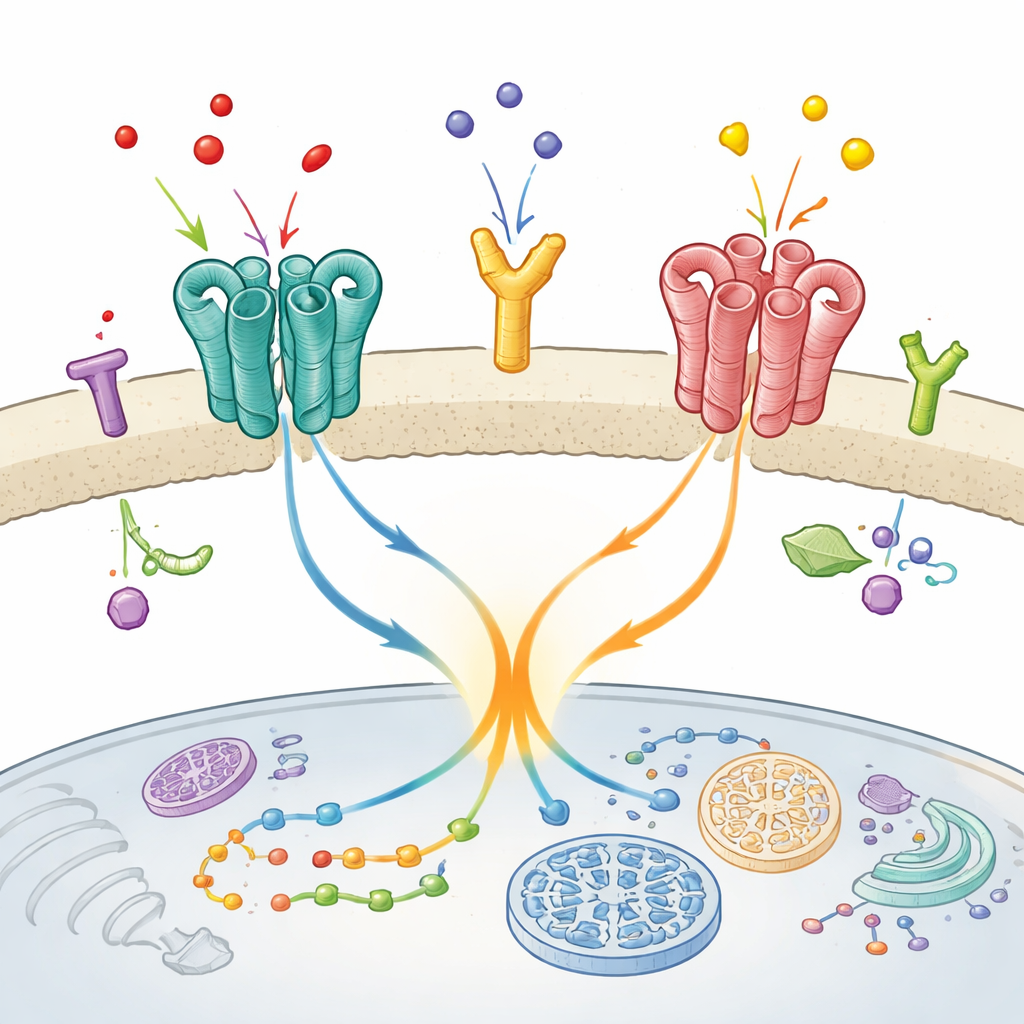
Un partenariat surprenant dans le cerveau
Les chercheurs se sont concentrés sur un duo spécifique présent dans des régions du cerveau impliquées dans l’humeur, la perception et le mouvement : le récepteur métabotropique du glutamate mGlu2 et le récepteur de la sérotonine 5‑HT2A. Les deux sont des cibles d’antipsychotiques, et des travaux antérieurs suggéraient qu’ils forment une paire fonctionnelle dans les tissus cérébraux vivants. Ici, l’équipe a posé deux questions clés : ces récepteurs sont‑ils vraiment en contact direct à la surface cellulaire, et si oui, ce contact physique modifie‑t‑il le comportement de mGlu2 ?
Prouver que les récepteurs se touchent
Pour vérifier si mGlu2 et 5‑HT2A se rapprochent réellement, les auteurs ont utilisé des cellules humaines cultivées en laboratoire et ont marqué chaque récepteur par de petites balises fluorescentes. Lorsque les protéines marquées se trouvent suffisamment proches, l’énergie peut sauter d’une balise à l’autre, générant un signal mesurable. Ces expériences ont révélé un signal fort lorsque les deux récepteurs étaient présents, indiquant qu’ils se regroupent à la surface cellulaire. L’équipe a ensuite utilisé une astuce chimique ingénieuse, introduisant des « crochets » placés spécifiquement dans chaque récepteur afin que, lorsqu’ils sont proches, ils puissent être verrouillés ensemble. Les complexes réticulés obtenus ont confirmé que mGlu2 et 5‑HT2A se contactent via des sections spécifiques enfouies dans la membrane cellulaire.
Un récepteur active discrètement un autre
Ensuite, les scientifiques ont testé si ce contact modifie la réponse de mGlu2. À l’aide de capteurs fluorescents sensibles et de lectures biochimiques, ils ont suivi la conformation et l’état d’activité de mGlu2. En présence de 5‑HT2A, même sans ajout de glutamate, davantage de récepteurs mGlu2 basculaient en conformation « activée » et présentaient une légère mais significative augmentation du signal intracellulaire. Le blocage de mGlu2 lui‑même supprimait cet effet, mais activer ou inhiber 5‑HT2A avec ses propres médicaments ne l’annulait pas, et une variante mutée de 5‑HT2A incapable d’activer sa voie de signalisation habituelle stimulait néanmoins mGlu2. Cela signifie que 5‑HT2A agit plutôt comme une béquille de soutien que comme un interrupteur actif : sa simple présence, et le contact physique, stabilisent la forme active de mGlu2.
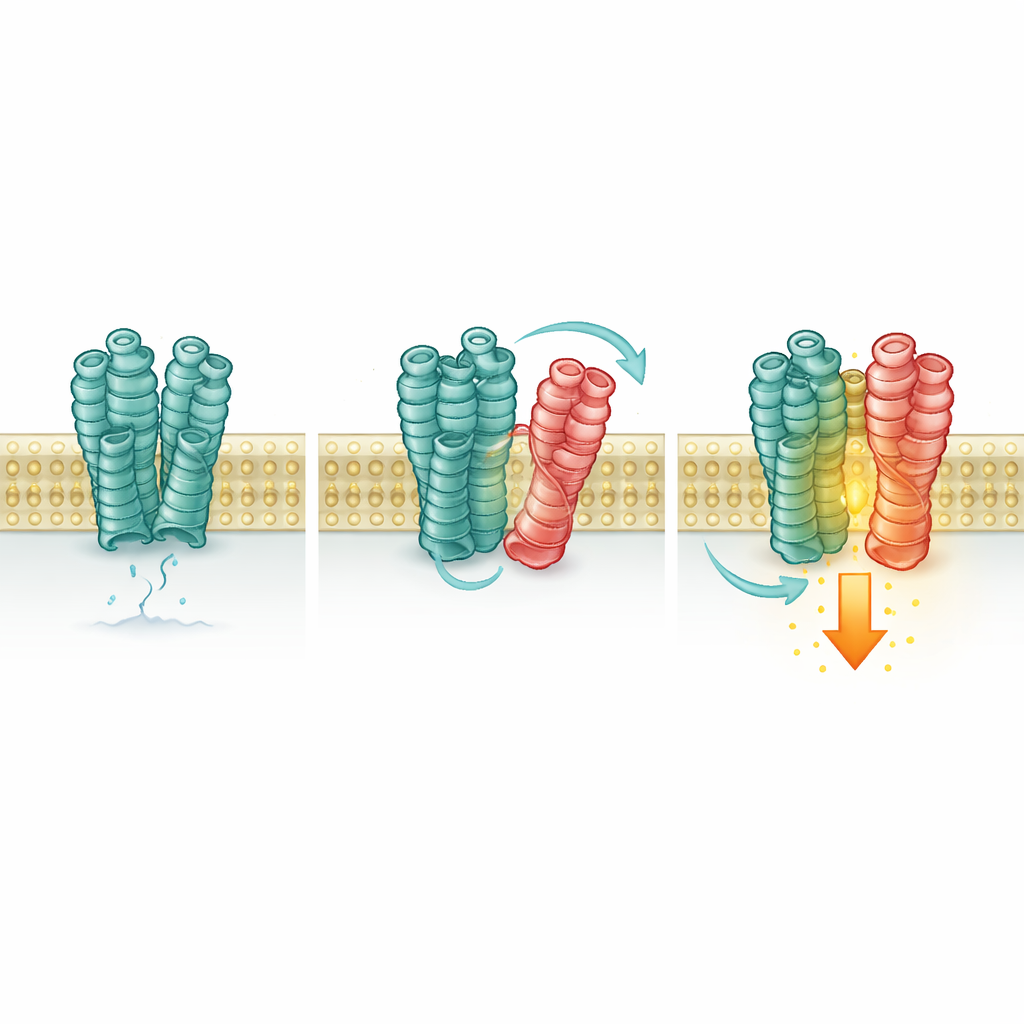
De nombreux autres partenaires s’en mêlent
L’histoire ne s’arrête pas à la sérotonine. Les auteurs ont dépisté 44 autres GPCR pour voir s’ils pouvaient influencer mGlu2 de façon similaire. Plusieurs d’entre eux, y compris plusieurs récepteurs de la dopamine et un autre sous‑type de sérotonine, ont également poussé mGlu2 vers son état actif, tandis que d’autres ont eu peu d’effet. Un récepteur de la dopamine, D1, a clairement augmenté l’activité de base de mGlu2 en l’absence d’apport supplémentaire de glutamate, ce qui est à nouveau cohérent avec un partenariat physique favorisant la position « activée ». En revanche, un récepteur muscarinique utilisé comme témoin n’a ni interagi fortement avec mGlu2 ni modifié son activité.
Pourquoi c’est important pour les troubles cérébraux
Ce travail montre que certains récepteurs cérébraux font plus que rester indépendants en attendant leur clé chimique. En formant de petits assemblages, un récepteur peut allostériquement, c’est‑à‑dire indirectement, régler le comportement d’un autre. Dans le cas de mGlu2 et 5‑HT2A, cela signifie que des récepteurs liés à la sérotonine peuvent façonner la manière dont les signaux du glutamate sont traités, même lorsqu’ils ne signalent pas activement. Étant donné que ces partenariats récepteurs sont associés à la schizophrénie, à la maladie de Parkinson et possiblement à d’autres affections, ils offrent un nouvel angle intéressant pour la conception de médicaments : des traitements ciblant un membre d’une paire pourraient être conçus pour moduler l’activité de l’autre, offrant un contrôle plus subtil des circuits cérébraux complexes.
Citation: Gai, S., Lin, L., Meng, J. et al. Allosteric activation of the glutamate receptor mGlu2 by the serotonin receptor 5-HT2A. Nat Commun 17, 3303 (2026). https://doi.org/10.1038/s41467-026-69939-3
Mots-clés: Hétéromères de GPCR, récepteur mGlu2, récepteur 5‑HT2A, modulation allostérique, schizophrénie