Clear Sky Science · zh
仿生金属-药物配位纳米平台通过能量干扰对抗铜绿假单胞菌的耐药性
为什么耐药性感染关系到我们每个人
抗生素耐药性感染正在使曾经可治的疾病变得更难、也更危险。在医院中,常见细菌正在学会躲避我们最有效的药物,使得原本常见的肺炎或伤口感染变成威胁生命的危机。本研究描述了一种新的方法,通过切断细菌的能量供应来“重新唤醒”一种旧有抗生素对付特别顽固的病原体,而不是完全发明一种新药。
一种对药物不屑一顾的顽固肺部病原
铜绿假单胞菌是一种顽强的细菌,常导致严重的肺部感染,尤其是对那些防御力减弱的人群,如囊性纤维化患者或因化疗而免疫受抑的人。它通过阻止药物通过外膜进入细胞和主动将抗生素泵出细胞来抵抗治疗。与此同时,针对这类革兰氏阴性细菌的新抗生素研发生态已经几十年缺乏活力。因此,研究者将目标放在另一条路径上:通过解除细菌内建的耐药系统,使现有抗生素重新发挥效力。
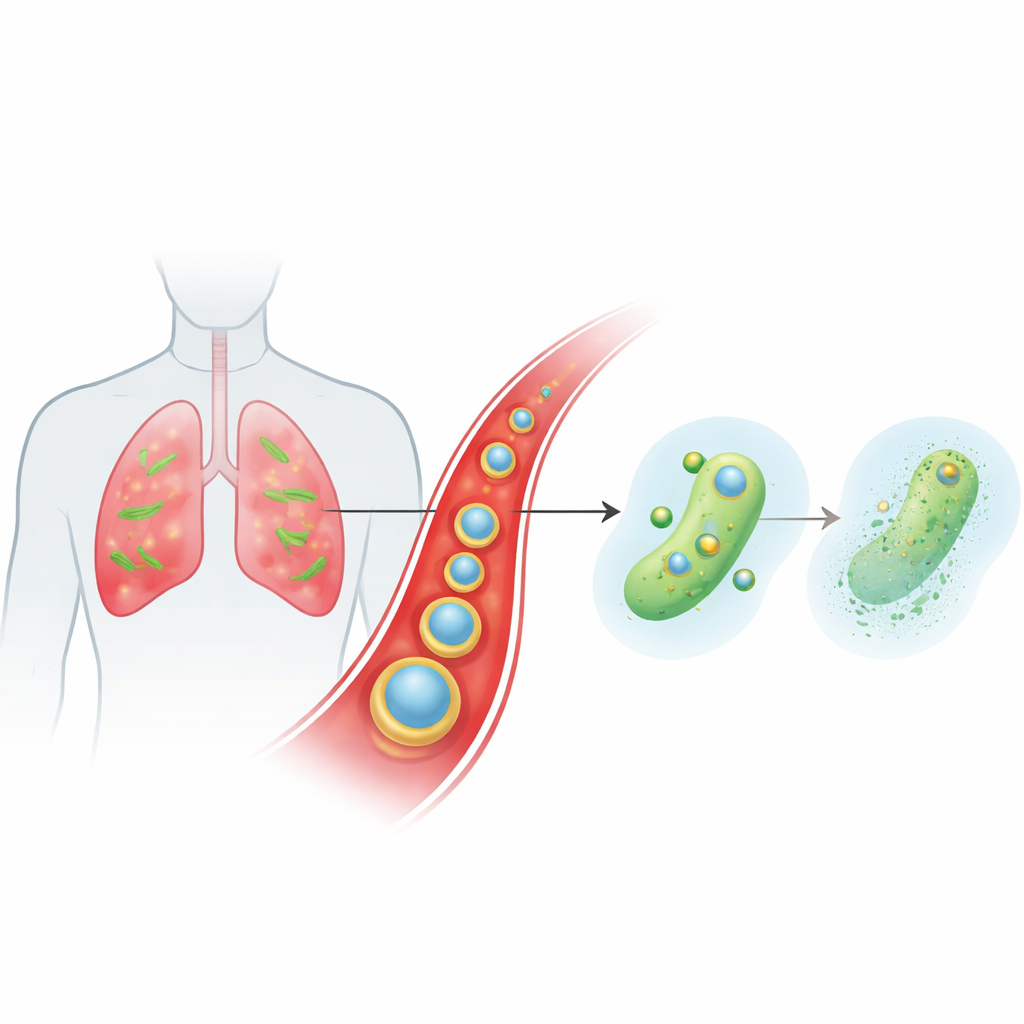
一种聪明的载体在血流中奔向感染部位
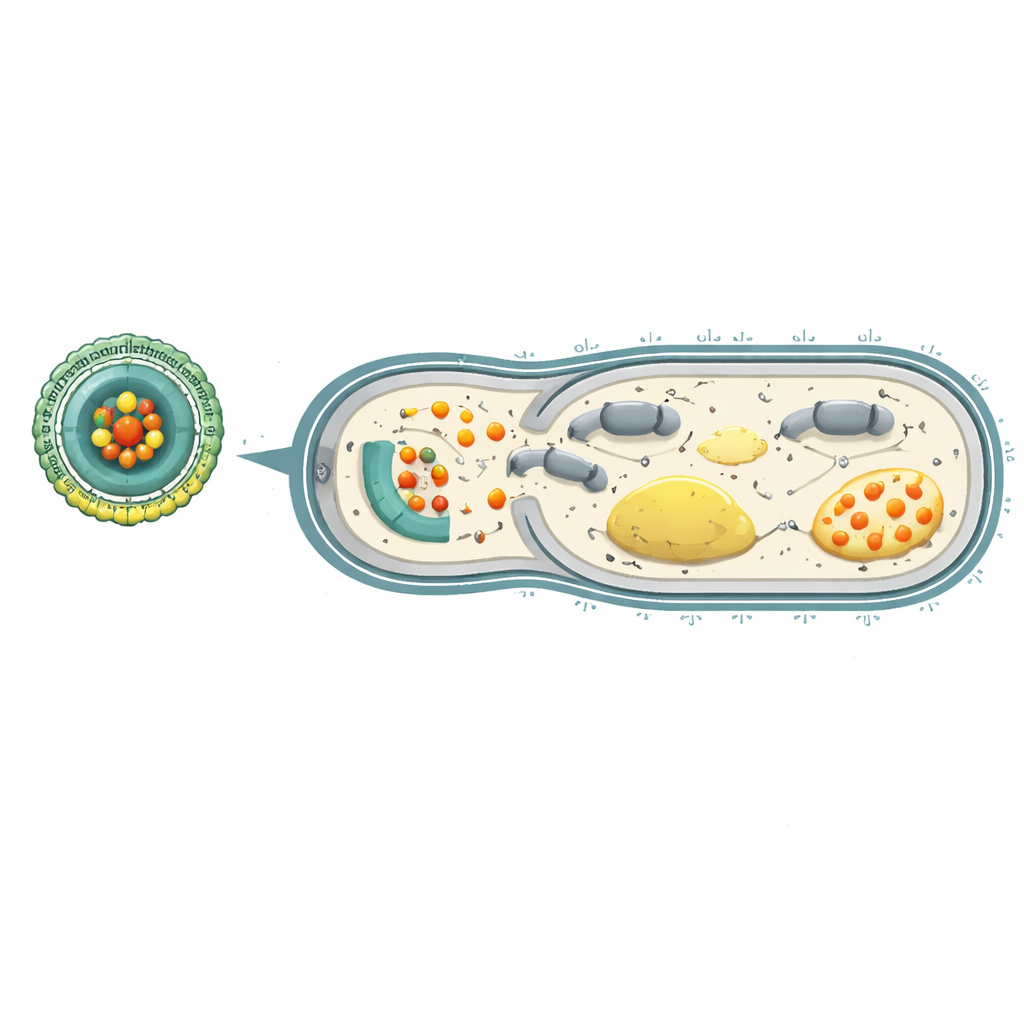
团队设计了一种微小的分层颗粒,称为Ce-Car@EV,用以递送经典的β-内酰胺类抗生素卡苄青霉素(carbenicillin)和具有特殊化学性质的金属离子铈(cerium)。内核是纳米尺度的配位聚合物,卡苄青霉素分子与铈离子相连,形成多孔、高载药量的结构,在弱酸性条件下可解体。该内核随后被从生姜植物提取得到的天然细胞外囊泡包裹。这些植物来源的囊泡有助于颗粒逃避免疫清除,在血液中停留更久,并优先在血管通透性增加、免疫细胞被激活的炎性感染性肺组织中富集。一旦颗粒到达感染的酸性微环境,其结构松散并按需释放卡苄青霉素和铈离子。
通过使细菌断粮来阻止耐药
在细菌细胞内,三磷酸腺苷(ATP)作为通用的能量货币,驱动从细胞壁合成到将抗生素泵出的外排泵等各种过程。铈离子能够分解ATP并扰乱正常生成ATP的反应链。体外实验显示,当耐药的铜绿假单胞菌在类似感染部位的酸性环境中遇到Ce-Car@EV时,纳米颗粒释放出铈和卡苄青霉素,显著降低细菌存活率。铈不仅增强了卡苄青霉素与构建细胞壁的蛋白靶点的结合,还耗竭了ATP并损害细菌呼吸过程中的关键步骤。结果是细菌膜两侧由质子驱动的“电池”崩溃,通常用于移除药物的外排泵失去动力。
逆转耐药并保护肺组织
为了验证该策略是否真的能逆转耐药,研究者在存在游离卡苄青霉素或Ce-Car@EV平台的条件下,将铜绿假单胞菌培养了多代。在仅暴露于抗生素的细菌中,耐药性迅速增强,所需药物浓度增加了256倍。相比之下,反复用Ce-Car@EV处理的细菌所发展出的耐药性要小得多。基因分析显示,接受纳米平台处理的细菌中与能量产生、呼吸和多药外排泵相关的基因表达被下调。在患有严重耐药性铜绿假单胞菌肺炎的小鼠模型中,静脉注射的Ce-Car@EV在受感染的肺部强烈富集,显著降低了肺及其他器官的细菌数量,减少了肺部肿胀和组织损伤,并提高了存活率,同时在血液检测和器官检查中显示出最低限度的毒性。
这对未来治疗可能意味着什么
通过将熟悉的抗生素与金属离子结合并包裹在仿生的递送外壳中,这项工作为在不单靠新药的情况下智胜耐药细菌提供了蓝图。Ce-Car@EV颗粒能靶向炎性肺部,在酸性感染位点崩解,然后关闭细菌的能量和药物外排系统,使卡苄青霉素重新发挥作用。如果在人体中证明此类方法既安全又有效,它们可能延长现有抗生素的可用寿命,并为目前让医生选择有限的多药耐药感染提供新的治疗选项。
引用: Ye, Y., Zhang, K., Wang, Y. et al. Biomimetic metal-drug coordination nanoplatform to counteract drug resistance in Pseudomonas aeruginosa via energy disruption. Nat Commun 17, 2808 (2026). https://doi.org/10.1038/s41467-026-69712-6
关键词: 抗菌素耐药性, 铜绿假单胞菌, 纳米颗粒治疗, 能量代谢, β-内酰胺类抗生素