Clear Sky Science · sv
Biomimetisk metall-läkemedelskoordination nanoplattform för att motverka läkemedelsresistens hos Pseudomonas aeruginosa via energistörning
Varför läkemedelsresistenta infektioner berör oss alla
Antibiotikaresistenta infektioner gör tidigare behandlingsbara sjukdomar svårare och farligare att bota. På sjukhus lär sig vanliga bakterier att undkomma våra bästa läkemedel, vilket förvandlar rutinmässig lunginflammation eller sårinfektioner till livshotande tillstånd. Denna studie beskriver ett nytt sätt att ”återväcka” ett gammalt antibiotikum mot en särskilt envis bakterie genom att stänga av bakteriens energiförsörjning snarare än att uppfinna ett helt nytt läkemedel.
En envis lungsbakterie som avfärdar läkemedel
Pseudomonas aeruginosa är en robust bakterie som ofta orsakar allvarliga lunginfektioner, särskilt hos personer med försvagat försvar, såsom de med cystisk fibros eller immunundertryckning efter kemoterapi. Den undviker behandling genom att blockera läkemedelsinträngning via sitt yttre membran och genom att aktivt pumpa ut antibiotika ur cellen. Samtidigt har den globala pipeline för helt nya antibiotika — särskilt sådana som fungerar mot denna typ av gramnegativa bakterier — varit tunn i årtionden. Forskarna riktade sig därför mot ett annat mål: att göra befintliga antibiotika kraftfulla igen genom att oskadliggöra bakteriens inbyggda resistenssystem.
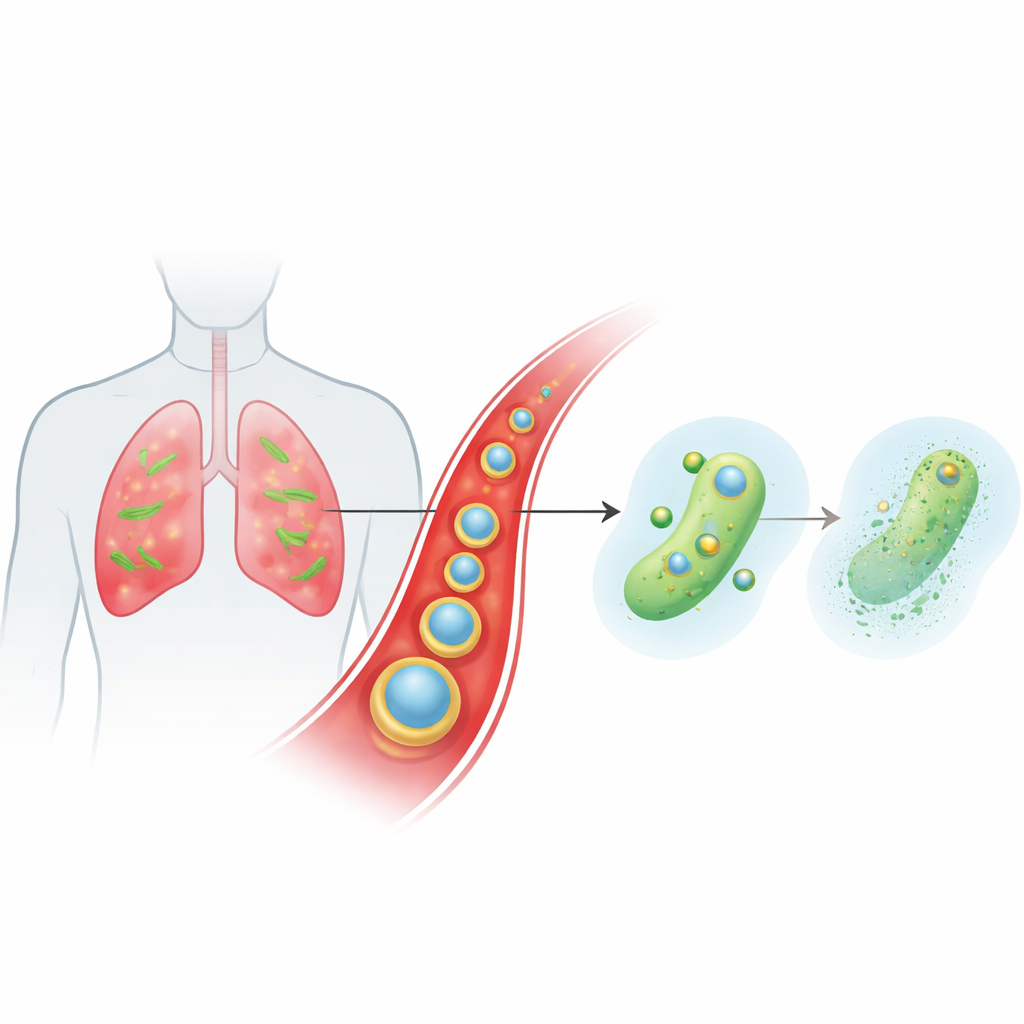
En smart bärare som färdas i blodomloppet till infektionsställen
Teamet designade en liten, lagerbyggd partikel kallad Ce-Car@EV för att leverera ett klassiskt beta-laktamantibiotikum, carbenicillin, tillsammans med cerium, en metalljon med ovanlig kemi. Den inre kärnan är en nanoskalig koordineringspolymer där carbenicillinmolekyler länkar till ceriumjoner och skapar en porös struktur med hög läkemedelslast som bryts ner i svagt sura förhållanden. Denna kärna omsluts sedan av naturliga extracellulära vesiklar hämtade från ingefärsplantor. Dessa växtvesiklar hjälper partiklarna att undvika immunrensning, stanna längre i blodomloppet och ackumuleras i förhöjd grad i inflammerad, infekterad lungvävnad där blodkärlen är läckande och immunceller är aktiverade. När partiklarna når det sura mikroklimatet vid infektion löses de upp och frisätter både carbenicillin och ceriumjoner vid behov.
Att svälta bakterier på energi för att stoppa resistens
I bakterieceller fungerar adenosintrifosfat (ATP) som universell energivaluta och driver allt från cellväggsbygge till de effluxpumpar som spottar ut antibiotika. Ceriumjoner kan bryta ner ATP och störa reaktionskedjan som normalt genererar det. Laboratorietester visade att när resistenta P. aeruginosa mötte Ce-Car@EV i en sur miljö liknande infektionsställen, frigjorde nanopartiklarna cerium och carbenicillin och minskade bakteriers överlevnad kraftigt. Cerium hjälpte inte bara carbenicillin att fästa hårdare vid sitt proteintarget som bygger cellväggen, utan utarmade även ATP och försämrade viktiga steg i bakteriers andning. Som ett resultat kollapsade den protondrivna ”batteripotentialen” över bakteriemembranet och de effluxpumpar som normalt tar bort läkemedel blev strömlösa.
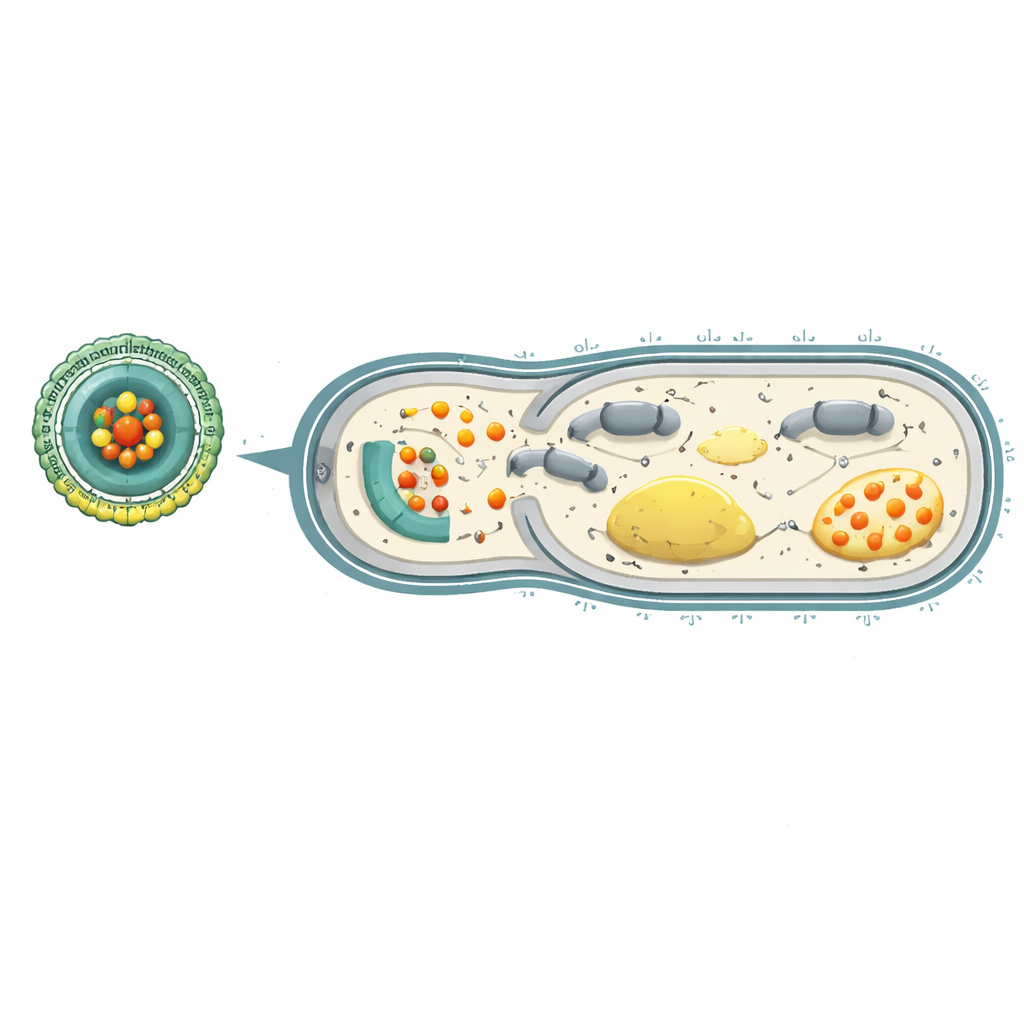
Återvändande av resistens och skydd av lungorna
För att se om denna strategi verkligen vände tillbaka resistensen odlade forskarna P. aeruginosa i många generationer i närvaro av antingen fritt carbenicillin eller Ce-Car@EV-plattformen. Bakterier som utsattes endast för antibiotikumet blev snabbt starkt resistenta och behövde 256 gånger större dos för att kontrolleras. I kontrast utvecklade de som upprepade gånger behandlades med Ce-Car@EV betydligt mindre resistens. Genetiska analyser visade att gener som är involverade i energiproduktion, andning och multidrogseffluxpumpar nedreglerades i bakterier behandlade med nanoplattformen. Hos möss med svår, läkemedelsresistent P. aeruginosa-pneumoni ackumulerade intravenöst tillförd Ce-Car@EV kraftigt i infekterade lungor, sänkte bakterieantalet dramatiskt där och i andra organ, minskade lungsvullnad och vävnadsskada samt förbättrade överlevnaden, samtidigt som minimal toxicitet noterades i blodprov och organundersökningar.
Vad detta kan innebära för framtida behandlingar
Genom att kombinera ett välkänt antibiotikum med en metalljon inuti ett naturinspirerat leveransskal erbjuder detta arbete en ritning för att överlista resistenta bakterier utan att enbart förlita sig på nya läkemedel. Ce-Car@EV-partiklarna söker sig till inflammerade lungor, faller isär i den sura infektionsnischen och stänger sedan ner bakteriens energisystem och läkemedelspumpar så att carbenicillin kan fungera igen. Om liknande metoder visar sig vara säkra och effektiva hos människor kan de förlänga livslängden för befintliga antibiotika och ge nya alternativ mot multiresistenta infektioner som i dag lämnar läkare med få valmöjligheter.
Citering: Ye, Y., Zhang, K., Wang, Y. et al. Biomimetic metal-drug coordination nanoplatform to counteract drug resistance in Pseudomonas aeruginosa via energy disruption. Nat Commun 17, 2808 (2026). https://doi.org/10.1038/s41467-026-69712-6
Nyckelord: antimikrobiell resistens, Pseudomonas aeruginosa, nanopartikelterapi, energimetabolism, beta-laktam antibiotika