Clear Sky Science · ja
バイオミメティック金属–薬物配位ナノプラットフォームによる緑膿菌の薬剤耐性克服:エネルギー撹乱を介して
薬剤耐性感染症が私たち全員にとって重要な理由
抗生物質耐性のある感染症は、かつて治療可能だった病気を治しにくく、危険なものに変えつつあります。病院内では、ありふれた細菌が我々の最良の薬剤を回避する術を学び、日常的な肺炎や創傷感染が生命を脅かす危機に変わることがあります。本研究は、まったく新しい薬を開発するのではなく、細菌のエネルギー供給を断つことで、古い抗生物質を“再び効かせる”新しい方法を示しています。
薬をものともせずしぶとく生き延びる肺の病原体
Pseudomonas aeruginosa(緑膿菌)は頑強な細菌で、特に嚢胞性線維症患者や化学療法による免疫抑制を受けた人など、防御力が低下した人に重篤な肺感染を引き起こすことが多い。外膜で薬の侵入を阻み、さらに薬を細胞外へ能動的に排出するポンプを持つことで治療に抵抗する。同時に、この種のグラム陰性菌に有効な全く新しい抗生物質の開発は何十年も乏しく、研究者らは別の目標に注目しました:既存の抗生物質を再び有力にするため、細菌の持つ耐性機構を無力化することです。
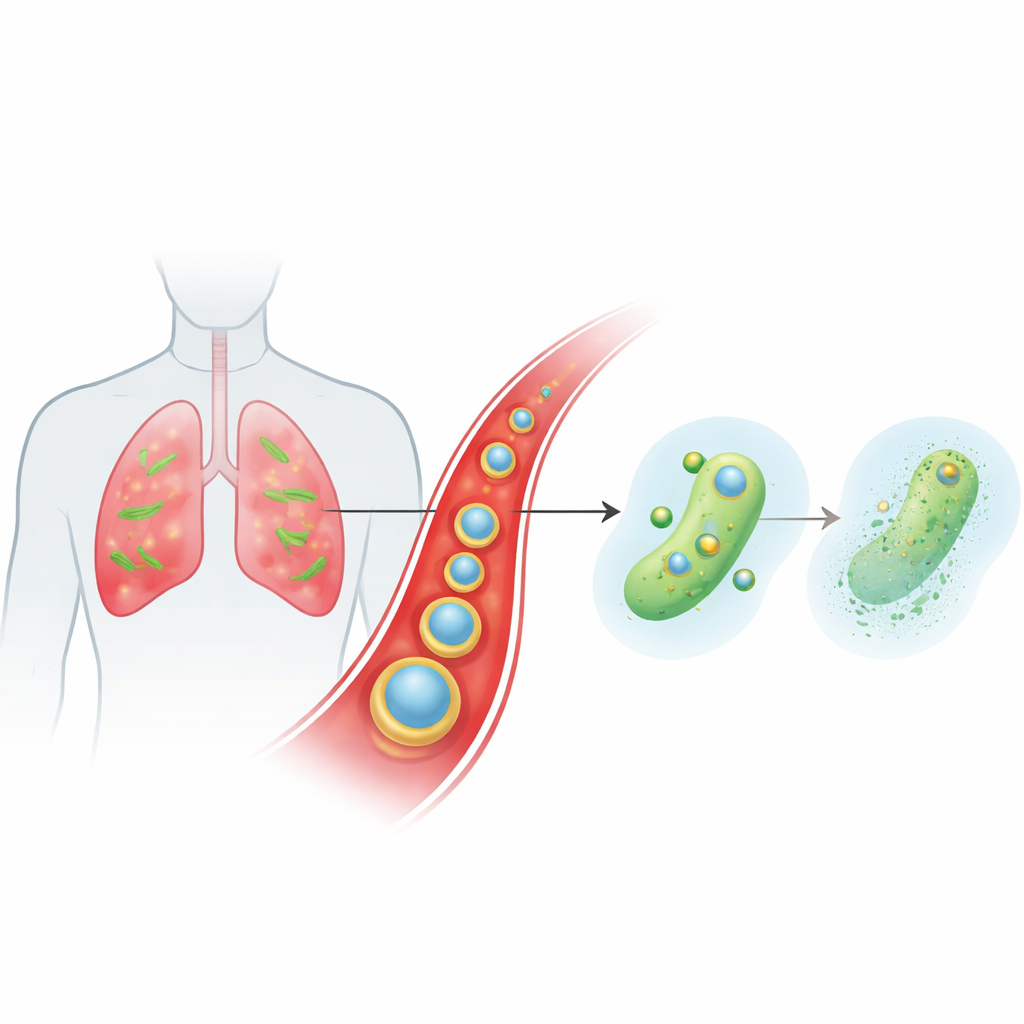
感染部位へと血流を駆ける賢い運搬体
研究チームは、Ce-Car@EVと呼ばれる微小で層状の粒子を設計し、古典的なβ-ラクタム系抗生物質であるカルベニシリンと、特異な化学的性質を持つ金属イオンであるセリウムを同時に届けるようにしました。内部コアは、カルベニシリン分子がセリウムイオンと連結して形成するナノスケールの配位高分子で、薬剤含有量が高く多孔質であり、わずかに酸性の条件で崩壊します。このコアは生姜由来の天然細胞外小胞で包まれており、これらの植物由来小胞は粒子が免疫による排除を回避し、血中滞留時間を延ばし、血管が漏れやすく免疫細胞が活性化している炎症性の感染肺組織に選択的に集積するのを助けます。粒子が酸性の感染微小環境に到達すると構造が緩み、カルベニシリンとセリウムイオンの両方を必要に応じて放出します。
薬剤耐性を止めるために細菌のエネルギーを枯渇させる
細菌内では、アデノシン三リン酸(ATP)が普遍的なエネルギー通貨として働き、細胞壁合成から抗生物質を押し出す排出ポンプに至るまであらゆる過程に動力を供給している。セリウムイオンはATPを分解し、通常それを生み出す一連の反応を乱す能力がある。試験管内での実験では、耐性を持つ緑膿菌が感染部位に類似した酸性環境でCe-Car@EVに遭遇すると、ナノ粒子がセリウムとカルベニシリンを放出して細菌の生存率を鋭く低下させることが示された。セリウムはカルベニシリンが細胞壁合成を担う標的タンパク質により強く結合するのを助けるだけでなく、ATPを枯渇させ、細菌呼吸の重要な段階を損なった。その結果、細菌膜を横切る陽子駆動の“バッテリー”が崩壊し、通常薬を排出する排出ポンプは動力を失った。
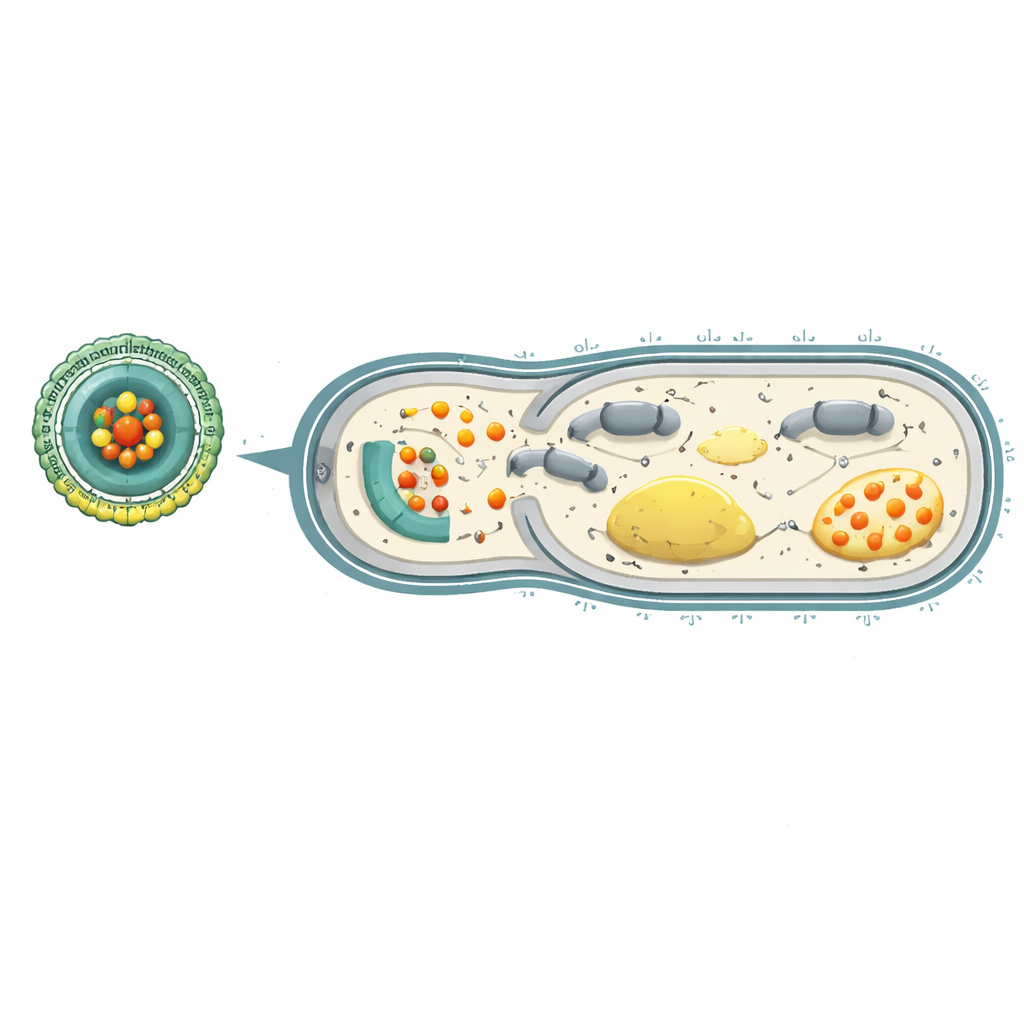
耐性の逆転と肺の保護
この戦略が本当に耐性を覆すかを確かめるため、研究者らは自由なカルベニシリンのみ、あるいはCe-Car@EVプラットフォームの存在下で長期間にわたり緑膿菌を培養した。抗生物質のみを曝露された細菌は速やかに高度な耐性を獲得し、制御に必要な薬剤量が256倍になった。一方、繰り返しCe-Car@EVで処理された菌ははるかに少ない耐性しか発現しなかった。遺伝学的解析は、エネルギー産生、呼吸、および多剤排出ポンプに関与する遺伝子がナノプラットフォームで処理された細菌で抑制されていることを示した。重度の薬剤耐性緑膿菌肺炎を有するマウスでは、静脈内投与されたCe-Car@EVが感染肺に強く蓄積し、肺および他の臓器での細菌数を劇的に低下させ、肺の腫脹や組織損傷を軽減し、生存率を改善した。血液検査や臓器検査での毒性は最小限にとどまった。
今後の治療への含意
馴染みのある抗生物質を金属イオンと結合させ、自然に着想を得た送達シェルで包むことで、この研究は新薬だけに頼らずに耐性菌を出し抜くための設計図を提示します。Ce-Car@EV粒子は炎症を起こした肺に集積し、酸性の感染ニッチで崩壊して細菌のエネルギーと薬物排出システムを遮断し、カルベニシリンが再び効くようにします。同様のアプローチがヒトで安全かつ有効であることが示されれば、既存の抗生物質の有用期間を延ばし、現在医師にほとんど選択肢を残さない多剤耐性感染症に対する新たな選択肢を提供する可能性があります。
引用: Ye, Y., Zhang, K., Wang, Y. et al. Biomimetic metal-drug coordination nanoplatform to counteract drug resistance in Pseudomonas aeruginosa via energy disruption. Nat Commun 17, 2808 (2026). https://doi.org/10.1038/s41467-026-69712-6
キーワード: 抗菌薬耐性, 緑膿菌(Pseudomonas aeruginosa), ナノ粒子治療, エネルギー代謝, β-ラクタム系抗生物質