Clear Sky Science · tr
Enerjiyi bozan biyoilimsel metal-ilaç koordinasyonlu nanoplatform ile Pseudomonas aeruginosa’daki ilaç direncine karşı koyma
Neden ilaç dirençli enfeksiyonlar hepimizi ilgilendirir
Antibiyotiklere dirençli enfeksiyonlar, eskiden kolayca tedavi edilebilen hastalıkları iyice zor ve daha tehlikeli hale getiriyor. Hastanelerde sıradan bakteriler en iyi ilaçlarımızdan kaçınmayı öğrenerek rutin zatürre veya yara enfeksiyonlarını yaşamı tehdit eden krizlere dönüştürüyor. Bu çalışma, tamamen yeni bir ilaç icat etmek yerine bakterinin enerji kaynağını keserek eski bir antibiyotiği yeniden “canlandırmanın” yeni bir yolunu anlatıyor.
İlaçlara aldırış etmeyen inatçı bir akciğer mikrobı
Pseudomonas aeruginosa, özellikle kistik fibrozisli ya da kemoterapi nedeniyle bağışıklığı zayıflamış kişilerde ciddi akciğer enfeksiyonlarına sıkça neden olan dayanıklı bir bakteri türüdür. Dış zarından ilacın girişini engelleyerek ve aynı zamanda antibiyotikleri hücre dışına aktif olarak pompalayarak tedaviyi zorlaştırır. Buna ek olarak, özellikle bu tür Gram-negatif bakterilere etkili tamamen yeni antibiyotiklerin küresel geliştirme hattı on yıllardır zayıf olmuştur. Bu yüzden araştırmacılar farklı bir hedefe odaklandı: mevcut antibiyotikleri bakterinin yerleşik direnç mekanizmalarını etkisiz hâle getirerek tekrar etkili kılmak.
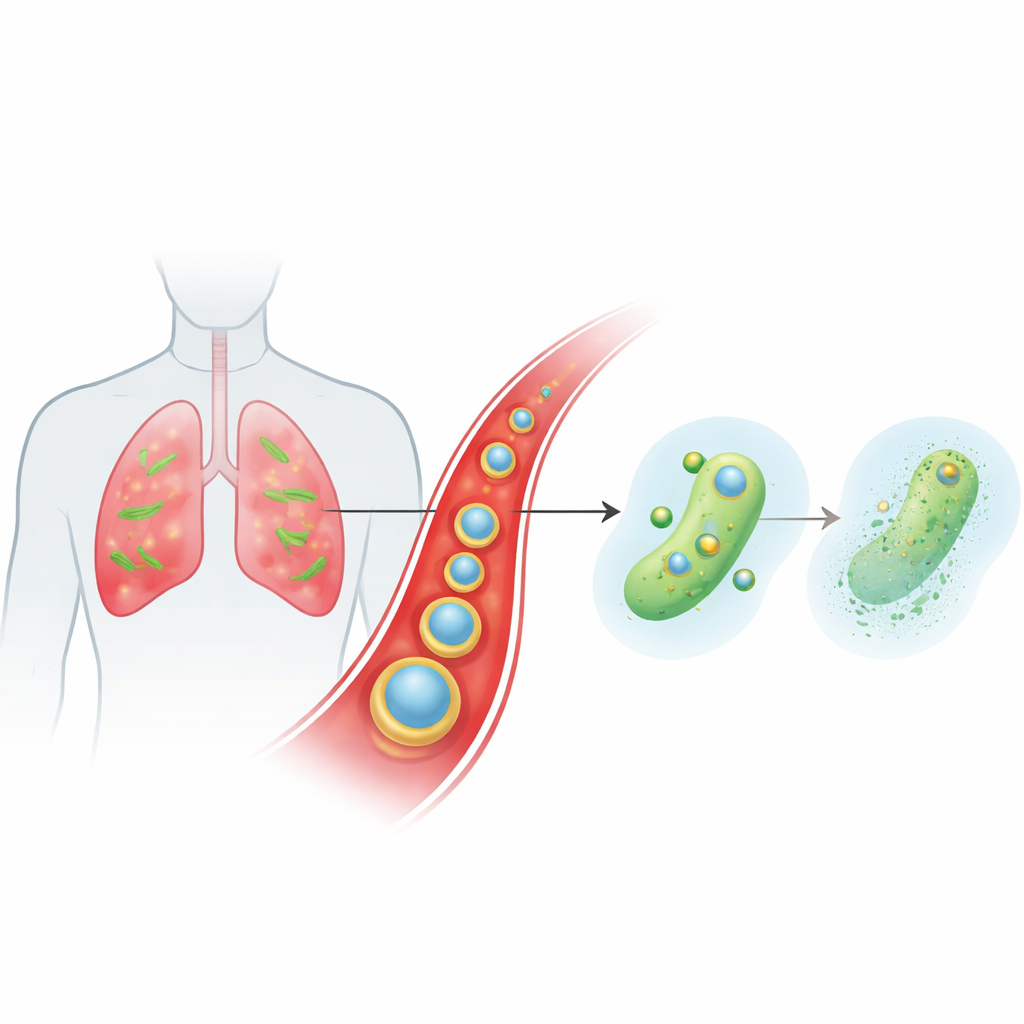
Enfeksiyon bölgelerine kan akışıyla ulaşan akıllı bir taşıyıcı
Ekip, klasik bir beta-laktam antibiyotik olan karbenisillini serbestçe taşıyıp aynı zamanda sıra dışı kimyası olan bir metal iyonu olan seryum ile birlikte iletebilen Ce-Car@EV adında küçük, katmanlı bir partikül tasarladı. İç çekirdek, karbenisillin moleküllerinin seryum iyonlarıyla bağlandığı nanoskaladaki bir koordinasyon polimeridir; gözenekli ve yüksek ilaç yüklü bir yapı oluşturur ve hafif asidik koşullarda parçalanır. Bu çekirdek, zencefil bitkisinden elde edilen doğal ekstraselüler veziküllerle kaplanır. Bu bitkisel veziküller, partiküllerin bağışıklık temizlenmesinden kaçınmasına, kan dolaşımında daha uzun kalmasına ve kan damarlarının sızdığı ve bağışıklık hücrelerinin aktifleştiği iltihaplı, enfekte akciğer dokusunda tercihen birikmesine yardımcı olur. Partiküller enfeksiyonun asidik mikromilieuine ulaştığında yapıları gevşer ve hem karbenisillin hem de seryum iyonlarını talep üzerine serbest bırakır.
İlaç direncini durdurmak için bakteriyi enerji açısından aç bırakmak
Bakteri hücrelerinin içinde adenozin trifosfat (ATP) hücre duvarı yapımından antibiyotikleri dışarı pompalayan effluks pompalarına kadar her şeyi çalıştıran evrensel enerji birimidir. Seryum iyonları ATP’yi parçalayabilir ve normalde ATP’yi üreten reaksiyon zincirini bozabilir. Laboratuvar testleri, dirençli P. aeruginosa bakterileri enfeksiyon bölgelerine benzeyen asidik bir ortamda Ce-Car@EV ile karşılaştığında nanoyapıların seryum ve karbenisilini serbest bıraktığını ve bakteriyel hayatta kalmayı hızla azalttığını gösterdi. Seryum, karbenisillinin hücre duvarını inşa eden protein hedefine daha sıkı bağlanmasına yardımcı olmanın yanı sıra ATP’yi tüketti ve bakteriyel solunumdaki önemli adımları bozdu. Sonuç olarak, bakteriyel zar boyunca proton kaynaklı “pil” çöktü ve ilaçları normalde dışarı atan effluks pompaları enerjisiz kaldı.
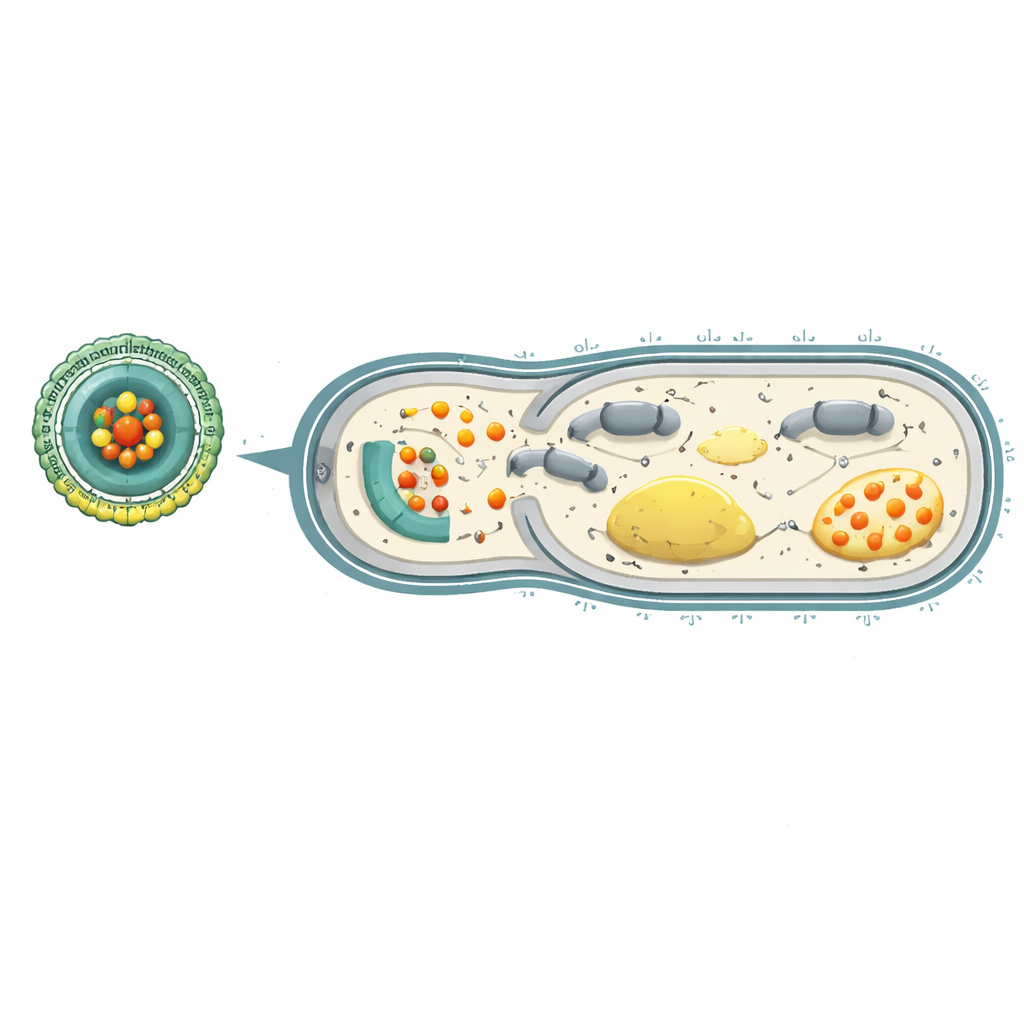
Direncin geri çevrilmesi ve akciğerlerin korunması
Bu stratejinin gerçekten direnci geri çevirip çevirmediğini görmek için araştırmacılar P. aeruginosa’yı ya serbest karbenisiline ya da Ce-Car@EV platformuna maruz bırakarak birçok nesil boyunca büyüttüler. Sadece antibiyotiğe maruz kalan bakteriler hızla yüksek derecede dirençli oldu ve kontrol altına alınmaları için 256 kat daha fazla ilaca ihtiyaç duyuldu. Buna karşılık, yineleyen Ce-Car@EV tedavisi uygulananlar çok daha az direnç geliştirdi. Genetik analizler, nanoplatform ile tedavi edilen bakterilerde enerji üretimi, solunum ve çoklu ilaç effluks pompalarında rol alan genlerin aşağı çekildiğini ortaya koydu. Şiddetli, ilaç dirençli P. aeruginosa pnömonisi olan farelerde intravenöz Ce-Car@EV enfekte akciğerlerde güçlü şekilde birikerek oradaki ve diğer organlardaki bakteri sayılarını dramatik biçimde azalttı, akciğer şişmesini ve doku hasarını azalttı ve hayatta kalmayı iyileştirdi; tüm bunlar kan testleri ve organ incelemelerinde minimal toksisite gösterirken gerçekleşti.
Gelecekteki tedaviler için ne anlama gelebilir
Tanıdık bir antibiyotiki metal iyonu ile doğadan esinlenmiş bir taşıyıcı kabuğun içinde birleştirerek bu çalışma, sadece yeni ilaçlara güvenmeden dirençli bakterileri alt etmenin bir planını sunuyor. Ce-Car@EV partikülleri iltihaplı akciğerlere hedefleniyor, enfeksiyonun asidik nişinde parçalanıyor ve ardından bakterinin enerji ve ilaç pompalama sistemlerini kapatarak karbenisillinin tekrar etkili olmasını sağlıyor. Benzer yaklaşımlar insanlarda güvenli ve etkili bulunursa, mevcut antibiyotiklerin kullanım ömrünü uzatabilir ve şu anda hekimlere az seçenek bırakan çoklu ilaç dirençli enfeksiyonlara karşı yeni seçenekler sağlayabilir.
Atıf: Ye, Y., Zhang, K., Wang, Y. et al. Biomimetic metal-drug coordination nanoplatform to counteract drug resistance in Pseudomonas aeruginosa via energy disruption. Nat Commun 17, 2808 (2026). https://doi.org/10.1038/s41467-026-69712-6
Anahtar kelimeler: antimikrobiyal direnç, Pseudomonas aeruginosa, nanoparçacık terapisi, enerji metabolizması, beta-laktam antibiyotikler