Clear Sky Science · it
Nanoplatforma biomimetica a coordinazione metallo-farmaco per contrastare la resistenza ai farmaci in Pseudomonas aeruginosa tramite l’interruzione dell’energia
Perché le infezioni resistenti ai farmaci ci riguardano tutti
Le infezioni resistenti agli antibiotici rendono malattie un tempo trattabili più difficili e pericolose da curare. Negli ospedali, batteri comuni stanno imparando a eludere i nostri migliori farmaci, trasformando polmoniti o infezioni di ferite di routine in crisi potenzialmente letali. Questo studio descrive un nuovo modo per “risvegliare” un vecchio antibiotico contro un germe particolarmente ostinato tagliando l’alimentazione energetica del batterio invece di inventare un farmaco completamente nuovo.
Un germe polmonare ostinato che ignora i farmaci
Pseudomonas aeruginosa è un batterio resistente che spesso provoca gravi infezioni polmonari, specialmente in persone con difese immunitarie indebolite, come chi ha fibrosi cistica o è immunosoppresso per chemioterapia. Resiste ai trattamenti impedendo l’ingresso dei farmaci attraverso la sua membrana esterna e pompando attivamente gli antibiotici fuori dalla cellula. Allo stesso tempo, la pipeline globale per nuovi antibiotici—soprattutto quelli efficaci contro questo tipo di batterio Gram-negativo—è stata scarsa per decenni. I ricercatori si sono quindi concentrati su un obiettivo diverso: rendere di nuovo potenti gli antibiotici esistenti disattivando i sistemi di resistenza intrinseci del batterio.
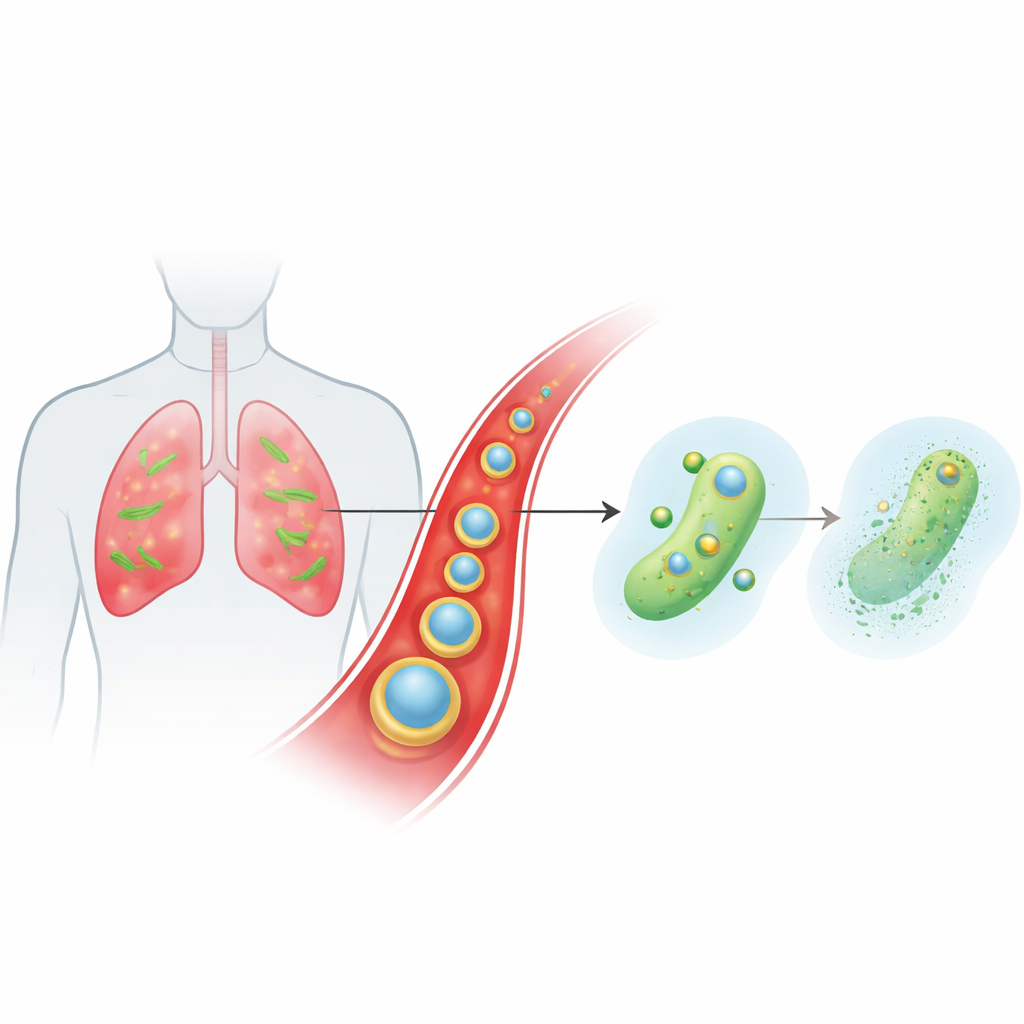
Un vettore intelligente che viaggia nel flusso sanguigno fino al sito dell’infezione
Il team ha progettato una particella nanometrica stratificata chiamata Ce-Car@EV per veicolare un classico antibiotico beta-lattamico, la carbenicillina, insieme al cerio, uno ione metallico con chimica insolita. Il nucleo interno è un polimero di coordinazione su scala nanometrica in cui le molecole di carbenicillina si legano agli ioni di cerio, creando una struttura porosa con alto carico di farmaco che si degrada in condizioni lievemente acide. Questo nucleo è quindi avvolto in vescicole extracellulari naturali ricavate da piante di zenzero. Queste vescicole vegetali aiutano le particelle a sfuggire alla rimozione immunitaria, a rimanere più a lungo nel circolo sanguigno e ad accumularsi preferenzialmente nel tessuto polmonare infiammato e infetto, dove i vasi sanguigni sono più permeabili e le cellule immunitarie sono attivate. Una volta che le particelle raggiungono il microambiente acido dell’infezione, la loro struttura si allenta e rilascia carbenicillina e ioni di cerio su richiesta.
Affamare i batteri di energia per fermare la resistenza ai farmaci
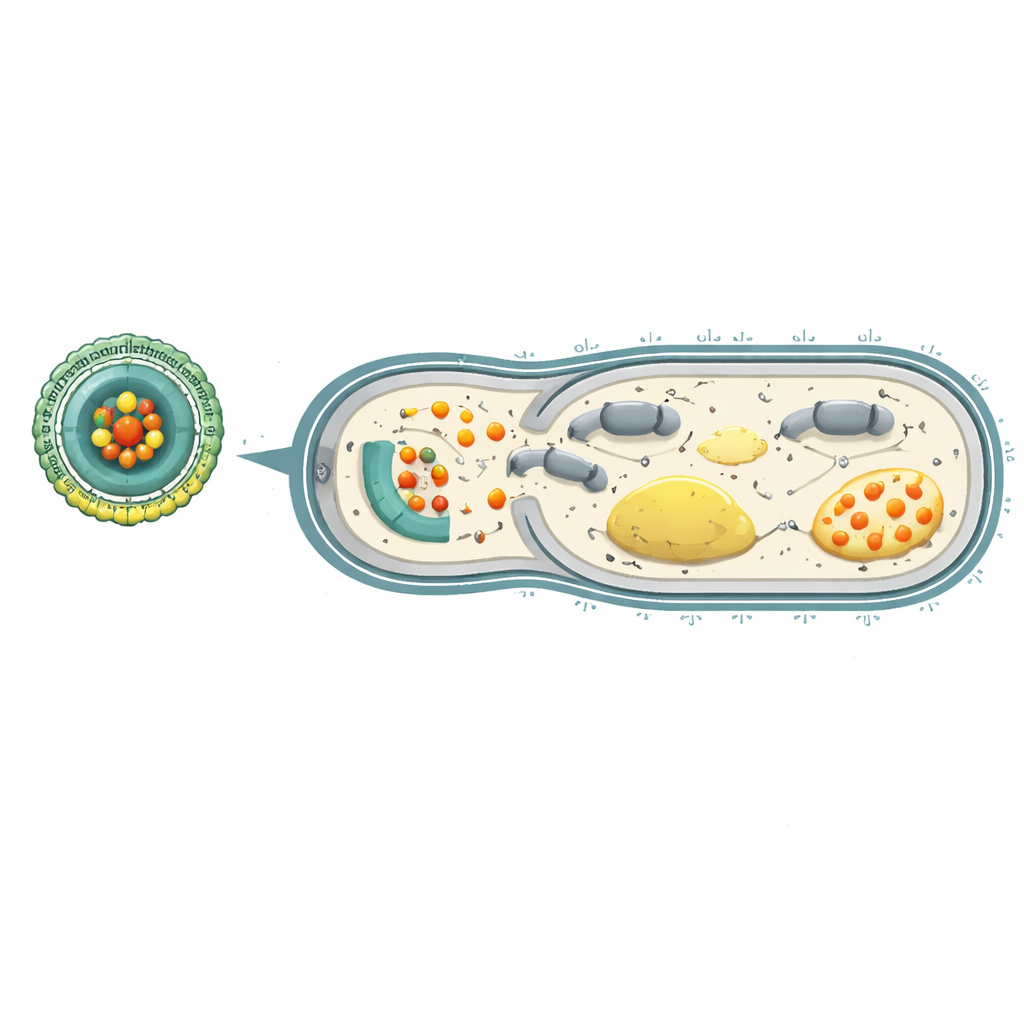
All’interno delle cellule batteriche, l’adenosina trifosfato (ATP) funge da valuta energetica universale, alimentando tutto, dalla sintesi della parete cellulare alle pompe di efflusso che espellono gli antibiotici. Gli ioni di cerio sono in grado di degradare l’ATP e di disturbare la catena di reazioni che lo genera normalmente. I test in laboratorio hanno mostrato che quando P. aeruginosa resistente incontrava Ce-Car@EV in un ambiente acido simile a un sito di infezione, le nanoparticelle rilasciavano cerio e carbenicillina, riducendo drasticamente la sopravvivenza batterica. Il cerio non solo favoriva un legame più stretto della carbenicillina con la proteina bersaglio che costruisce la parete cellulare, ma esauriva anche l’ATP e comprometteva passaggi chiave della respirazione batterica. Di conseguenza, la “batteria” a base di protoni attraverso la membrana batterica collassava e le pompe di efflusso che normalmente rimuovono i farmaci si trovavano prive di energia.
Invertire la resistenza e proteggere i polmoni
Per verificare se questa strategia ribaltasse realmente la resistenza, i ricercatori hanno fatto crescere P. aeruginosa per molte generazioni in presenza di carbenicillina libera o della piattaforma Ce-Car@EV. I batteri esposti solo all’antibiotico sono diventati rapidamente altamente resistenti, necessitando di 256 volte più farmaco per essere controllati. Al contrario, quelli trattati ripetutamente con Ce-Car@EV hanno sviluppato molta meno resistenza. Analisi genetiche hanno rivelato che i geni coinvolti nella produzione di energia, nella respirazione e nelle pompe di efflusso multidroga risultavano downregolati nei batteri trattati con il nanoplatform. In topi con polmonite grave da P. aeruginosa resistente ai farmaci, la somministrazione endovenosa di Ce-Car@EV si è accumulata fortemente nei polmoni infetti, ha ridotto in modo drammatico il carico batterico lì e in altri organi, ha diminuito il gonfiore polmonare e il danno tissutale e ha migliorato la sopravvivenza, mostrando al contempo tossicità minima negli esami del sangue e negli esami degli organi.
Cosa potrebbe significare per i trattamenti futuri
Combinando un antibiotico noto con uno ione metallico all’interno di un involucro ispirato alla natura, questo lavoro offre un modello per superare i batteri resistenti senza fare affidamento esclusivo su nuovi farmaci. Le particelle Ce-Car@EV si dirigono verso i polmoni infiammati, si degradano nella nicchia acida dell’infezione e poi spengono i sistemi energetici e di pompaggio dei farmaci del batterio così che la carbenicillina possa funzionare di nuovo. Se approcci simili si dimostrassero sicuri ed efficaci nell’uomo, potrebbero estendere la vita utile degli antibiotici esistenti e offrire nuove opzioni contro le infezioni multiresistenti che oggi lasciano i medici con poche alternative.
Citazione: Ye, Y., Zhang, K., Wang, Y. et al. Biomimetic metal-drug coordination nanoplatform to counteract drug resistance in Pseudomonas aeruginosa via energy disruption. Nat Commun 17, 2808 (2026). https://doi.org/10.1038/s41467-026-69712-6
Parole chiave: resistenza antimicrobica, Pseudomonas aeruginosa, terapia con nanoparticelle, metabolismo energetico, antibiotici beta-lattamici