Clear Sky Science · de
Biomimetische Metall-Arzneimittel-Koordinations-Nanoplattform zur Bekämpfung von Arzneimittelresistenzen bei Pseudomonas aeruginosa durch Energieunterbrechung
Warum medikamentenresistente Infektionen uns alle betreffen
Antibiotikaresistente Infektionen machen einst gut behandelbare Krankheiten schwerer und gefährlicher zu heilen. In Krankenhäusern lernen häufige Bakterien, unsere besten Arzneien zu umgehen, und verwandeln Routinepneumonien oder Wundinfektionen in lebensbedrohliche Krisen. Diese Studie beschreibt einen neuen Weg, ein altes Antibiotikum gegen einen besonders hartnäckigen Erreger „wiederzubeleben“, indem man dem Bakterium die Energiezufuhr kappt, statt ein völlig neues Medikament zu entwickeln.
Ein hartnäckiger Lungenkeim, der Medikamente abschüttelt
Pseudomonas aeruginosa ist ein widerstandsfähiges Bakterium, das häufig schwere Lungeninfektionen verursacht, besonders bei Menschen mit geschwächter Abwehr, etwa bei Mukoviszidose oder chemotherapiebedingter Immunsuppression. Es widersteht Behandlungen, indem es das Eindringen von Medikamenten durch seine Außenmembran blockiert und Antibiotika aktiv aus der Zelle heraussaugt. Gleichzeitig ist die weltweite Entwicklung neuer Antibiotika — besonders gegen diese Art gramnegativer Bakterien — seit Jahrzehnten dünn. Daher konzentrierten sich die Forscher auf ein anderes Ziel: bestehende Antibiotika wieder wirksam zu machen, indem sie die eingebauten Resistenzmechanismen des Bakteriums außer Kraft setzen.
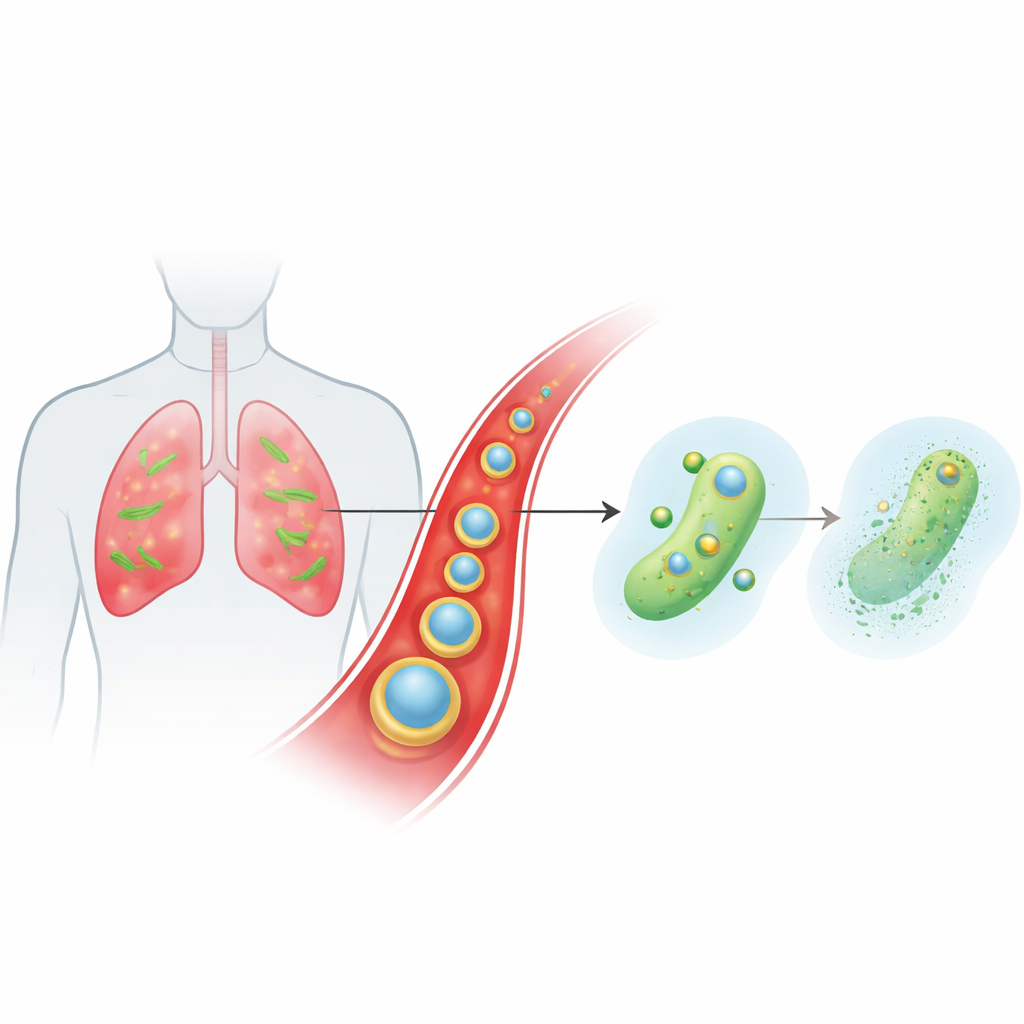
Ein intelligenter Träger, der über den Blutkreislauf zu den Infektionsherden gelangt
Das Team entwarf ein winziges, geschichtetes Partikel namens Ce-Car@EV, um ein klassisches Beta-Lactam-Antibiotikum, Carbenicillin, zusammen mit Cerium, einem Metallion mit ungewöhnlicher Chemie, zu liefern. Der innere Kern ist ein nanoskaliges Koordinationspolymer, in dem Carbenicillin-Moleküle mit Cerium-Ionen verknüpft sind und eine poröse Struktur mit hoher Wirkstoffbeladung bilden, die sich unter milden sauren Bedingungen auflöst. Dieser Kern wird dann in natürliche extrazelluläre Vesikel eingewickelt, die aus Ingwerpflanzen gewonnen wurden. Diese Pflanzenvesikel helfen den Partikeln, der Immunbeseitigung zu entgehen, länger im Blutkreislauf zu verbleiben und bevorzugt in entzündetem, infiziertem Lungengewebe anzureichern, wo Blutgefäße undicht sind und Immunzellen aktiviert sind. Sobald die Partikel in der sauren Mikro-umgebung der Infektion ankommen, lockert sich ihre Struktur und sowohl Carbenicillin als auch Cerium-Ionen werden bedarfsgerecht freigesetzt.
Bakterien der Energie berauben, um Resistenzen zu stoppen
Innerhalb bakterieller Zellen fungiert Adenosintriphosphat (ATP) als universelle Energiewährung und treibt alles an, vom Aufbau der Zellwand bis zu den Efflux-Pumpen, die Antibiotika hinauspumpen. Cerium-Ionen können ATP abbauen und die Reaktionskette stören, die normalerweise seine Erzeugung gewährleistet. Labortests zeigten, dass resistente P. aeruginosa in einer sauren Umgebung, die Infektionsherden ähnelt, bei Kontakt mit Ce-Car@EV Cerium und Carbenicillin freisetzten, wodurch das bakterielle Überleben stark sank. Cerium half nicht nur, dass Carbenicillin sich fester an sein Proteinbindungsziel beteiligt, das die Zellwand aufbaut, sondern es entleerte auch ATP und beeinträchtigte zentrale Schritte der bakteriellen Atmung. In der Folge kollabierte die protonengetriebene «Batterie» über die bakterielle Membran und die Efflux-Pumpen, die normalerweise Medikamente entfernen, waren ohne Energie.
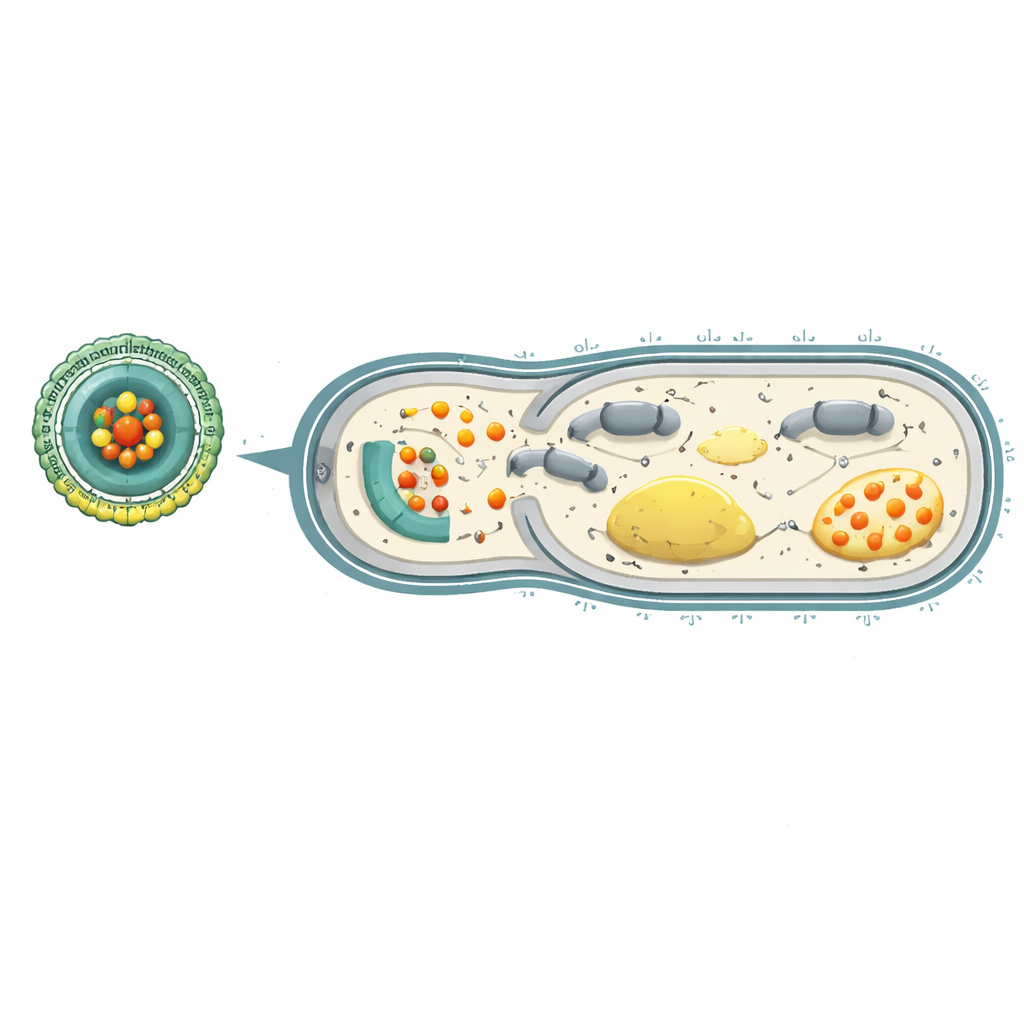
Resistenzen umkehren und die Lunge schützen
Um zu prüfen, ob diese Strategie Resistenzen wirklich zurückdreht, züchteten die Forscher P. aeruginosa über viele Generationen hinweg entweder in Anwesenheit von freiem Carbenicillin oder der Ce-Car@EV-Plattform. Bakterien, die nur dem Antibiotikum ausgesetzt waren, wurden schnell hochresistent und benötigten 256‑mal mehr Wirkstoff zur Kontrolle. Im Gegensatz dazu entwickelten jene, die wiederholt mit Ce-Car@EV behandelt wurden, deutlich geringere Resistenzen. Genetische Analysen zeigten, dass Gene, die an Energieproduktion, Atmung und multidrug Efflux-Pumpen beteiligt sind, in Bakterien, die mit der Nanoplattform behandelt wurden, herunterreguliert waren. Bei Mäusen mit schwerer, medikamentenresistenter P. aeruginosa-Pneumonie reicherte sich intravenös verabreichtes Ce-Car@EV stark in den infizierten Lungen an, senkte dort und in anderen Organen die Bakterienzahlen dramatisch, verringerte Lungenödem und Gewebeschäden und verbesserte das Überleben — und das bei minimaler Toxizität in Bluttests und Organuntersuchungen.
Was das für zukünftige Behandlungen bedeuten könnte
Indem ein bekanntes Antibiotikum mit einem Metallion in einer naturinspirierten Lieferhülle kombiniert wird, liefert diese Arbeit eine Blaupause, um resistente Bakterien auszutricksen, ohne ausschließlich auf neue Medikamente angewiesen zu sein. Die Ce-Car@EV-Partikel konzentrieren sich auf entzündete Lungen, zerfallen in der sauren Infektionsnische und schalten dann die Energie- und Wirkstoffpumpensysteme des Bakteriums aus, sodass Carbenicillin wieder wirken kann. Wenn ähnliche Ansätze beim Menschen sicher und wirksam sind, könnten sie die Nutzungsdauer bestehender Antibiotika verlängern und neue Optionen gegen multiresistente Infektionen bieten, die Ärzten derzeit nur wenige Wahlmöglichkeiten lassen.
Zitation: Ye, Y., Zhang, K., Wang, Y. et al. Biomimetic metal-drug coordination nanoplatform to counteract drug resistance in Pseudomonas aeruginosa via energy disruption. Nat Commun 17, 2808 (2026). https://doi.org/10.1038/s41467-026-69712-6
Schlüsselwörter: antimikrobielle Resistenzen, Pseudomonas aeruginosa, Nanopartikel-Therapie, Energiestoffwechsel, Beta-Lactam-Antibiotika