Clear Sky Science · pl
Biomimetyczna nanoplatforma koordynacji metalu i leku przeciwdziałająca oporności Pseudomonas aeruginosa poprzez zaburzenie dostaw energii
Dlaczego zakażenia odporne na leki dotyczą nas wszystkich
Zakażenia odporne na antybiotyki sprawiają, że kiedyś łatwe do wyleczenia choroby stają się trudniejsze i groźniejsze. W szpitalach pospolite bakterie uczą się omijać nasze najlepsze leki, zmieniając rutynowe zapalenia płuc czy zakażenia ran w zagrażające życiu kryzysy. W tym badaniu opisano nowy sposób „przywrócenia do życia” starego antybiotyku przeciwko szczególnie upartej bakterii poprzez odcięcie jej źródła energii, zamiast wynajdowania całkowicie nowego leku.
Uparta bakteria płucna, która lekceważy leki
Pseudomonas aeruginosa to odporna bakteria, która często powoduje ciężkie zakażenia płuc, zwłaszcza u osób z osłabioną odpornością, na przykład chorych na mukowiscydozę lub po chemioterapii. Opiera się leczeniu, blokując wejście leku przez błonę zewnętrzną i aktywnie wypompowując antybiotyki z komórki. Jednocześnie globalny potok całkowicie nowych antybiotyków — szczególnie tych działających na bakterie Gram-ujemne tego typu — od dziesięcioleci jest słaby. Badacze skupili się zatem na innym celu: przywrócić skuteczność istniejących antybiotyków przez unieszkodliwienie wbudowanych systemów oporności bakterii.
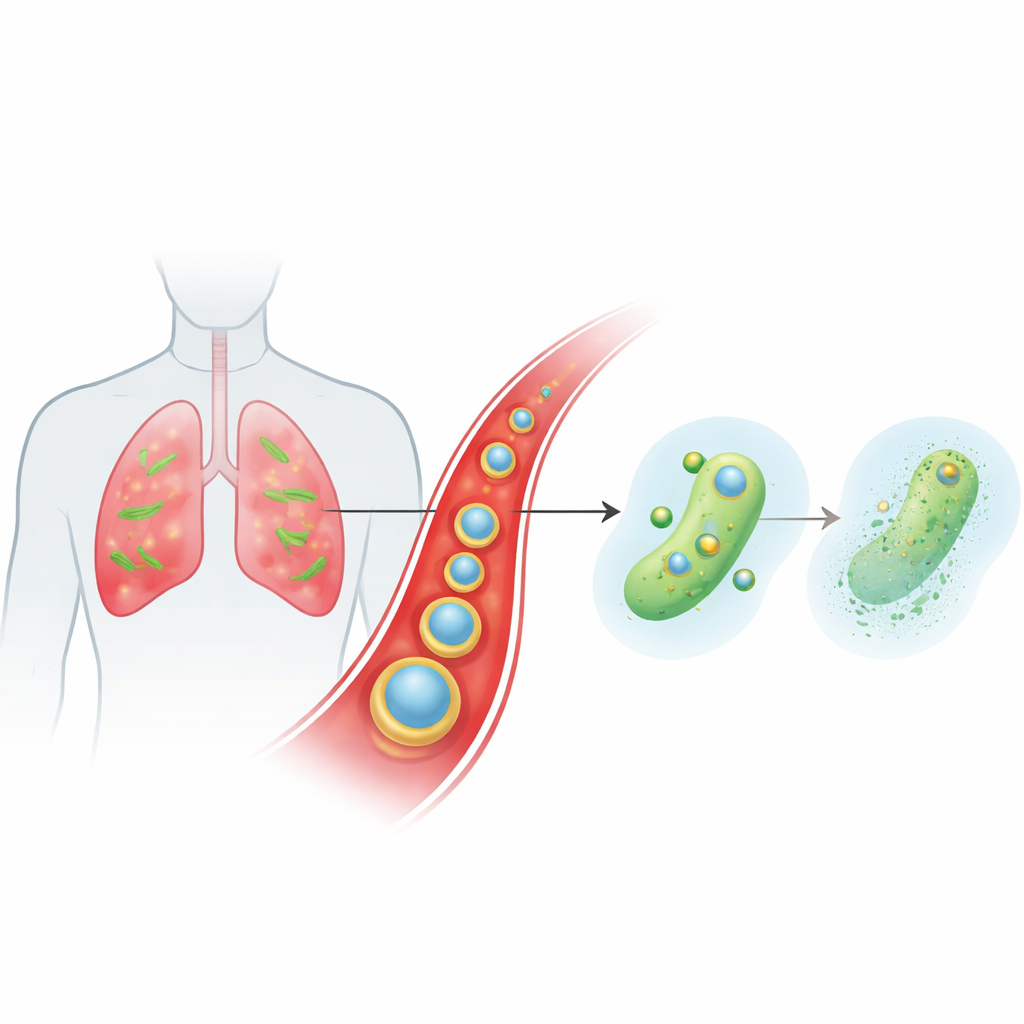
Sprytny nośnik, który dociera krwią do miejsc zakażenia
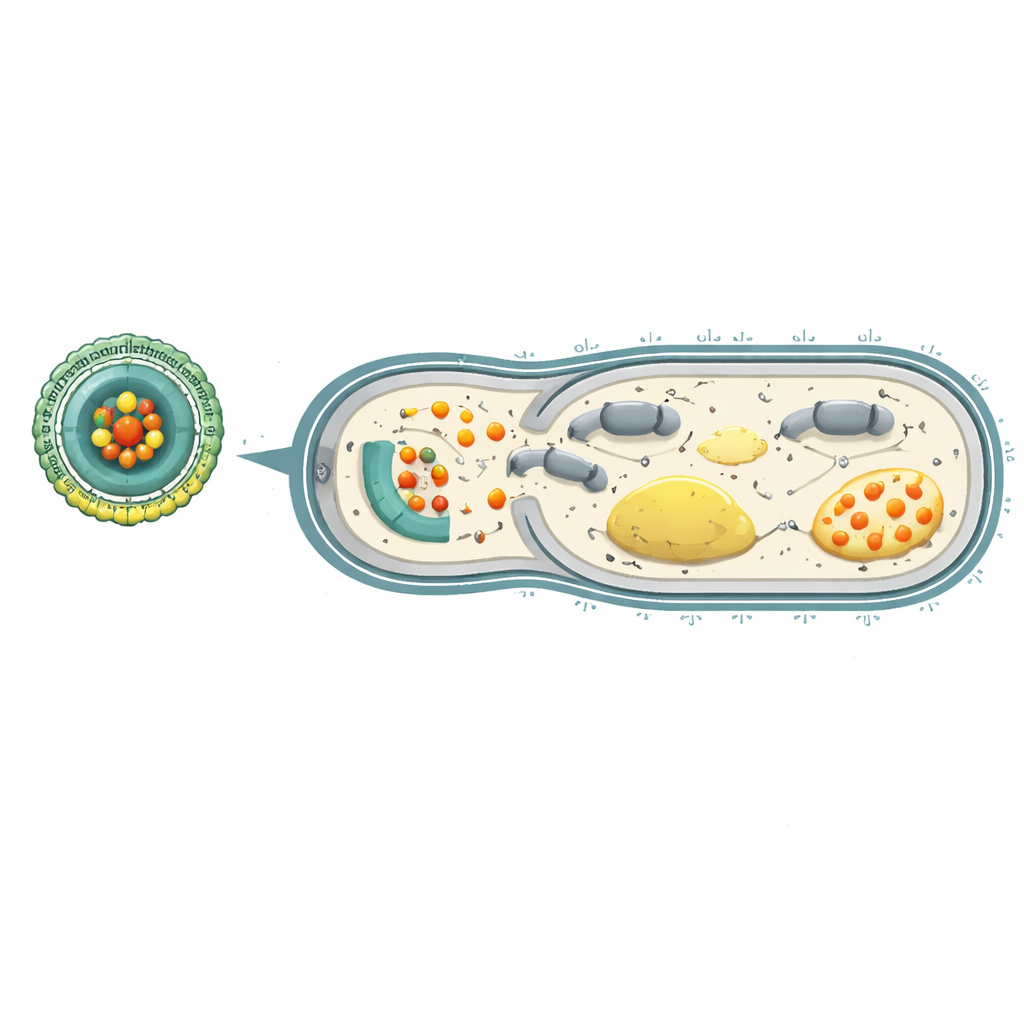
Zespół zaprojektował maleńką, warstwową cząstkę nazwaną Ce-Car@EV do dostarczania klasycznego antybiotyku beta-laktamowego — karbenicyliny — razem z ceremem, kationem metalu o nietypowej chemii. Wewnętrzne jądro to nanoskalowy polimer koordynacyjny, w którym cząsteczki karbenicyliny łączą się z jonami ceru, tworząc porowatą strukturę o dużym ładunku leku, która rozpada się w łagodnie kwaśnych warunkach. To jądro jest następnie otulone naturalnymi pęcherzykami zewnątrzkomórkowymi pozyskanymi z korzenia imbiru. Roślinne pęcherzyki pomagają cząstkom unikać usuwania przez układ odpornościowy, dłużej pozostawać we krwi i preferencyjnie gromadzić się w zapalnej, zakażonej tkance płucnej, gdzie naczynia krwionośne są nieszczelne, a komórki odpornościowe aktywowane. Gdy cząstki dotrą do kwaśnego mikrośrodowiska zakażenia, ich struktura się rozluźnia i uwalnia na żądanie zarówno karbenicylinę, jak i jony ceru.
Głodzenie bakterii z energii, by powstrzymać oporność
W komórkach bakteryjnych adenozynotrójfosforan (ATP) działa jako uniwersalna waluta energetyczna, napędzając wszystko, od budowy ściany komórkowej po pompy wypompowujące antybiotyki. Jony ceru mogą rozkładać ATP i zaburzać łańcuch reakcji, który normalnie go wytwarza. Testy laboratoryjne wykazały, że gdy oporne P. aeruginosa napotkały Ce-Car@EV w kwaśnym środowisku podobnym do miejsca zakażenia, nanocząstki uwalniały cer i karbenicylinę, gwałtownie zmniejszając przeżywalność bakterii. Cer nie tylko pomagał karbenicylinie mocniej wiązać się z białkowym celem odpowiedzialnym za budowę ściany komórkowej, lecz także wyczerpywał ATP i upośledzał kluczowe etapy oddychania bakteryjnego. W rezultacie napędzana protonami „bateria” po obu stronach błony komórkowej załamała się, a pompy wypompowujące, które zwykle usuwają leki, pozostały bez zasilania.
Odwracanie oporności i ochrona płuc
Aby sprawdzić, czy ta strategia faktycznie cofa oporność, badacze hodowali P. aeruginosa przez wiele pokoleń w obecności albo wolnej karbenicyliny, albo platformy Ce-Car@EV. Bakterie wystawione jedynie na antybiotyk szybko stały się wysoce oporne, wymagając 256 razy większej dawki leku, by je kontrolować. Dla porównania, te wielokrotnie traktowane Ce-Car@EV rozwinęły znacznie mniejszą oporność. Analizy genetyczne wykazały, że geny związane z produkcją energii, oddychaniem i wielolekowych pomp wypompowujących były przyciszone u bakterii traktowanych nanoplatformą. U myszy z ciężkim, opornym na leki zapaleniem płuc wywołanym przez P. aeruginosa dożylne podanie Ce-Car@EV silnie kumulowało się w zakażonych płucach, dramatycznie obniżało liczebność bakterii tam i w innych narządach, zmniejszało obrzęk i uszkodzenie tkanki płucnej oraz poprawiało przeżywalność, przy minimalnej toksyczności w badaniach krwi i badaniu narządów.
Co to może znaczyć dla przyszłych terapii
Łącząc znany antybiotyk z jonem metalu wewnątrz inspirowanej naturą otoczki dostarczającej, ta praca przedstawia schemat obejścia opornych bakterii bez polegania wyłącznie na nowych lekach. Cząstki Ce-Car@EV kierują się do zapalnych płuc, rozpadają w kwaśnej niszy zakażenia, a następnie wyłączają systemy energetyczne i wypompowujące leki bakterii, tak że karbenicylina znów może działać. Jeśli podobne podejścia okażą się bezpieczne i skuteczne u ludzi, mogą wydłużyć użyteczność istniejących antybiotyków i zapewnić nowe opcje przeciw zakażeniom wielolekowo opornym, które obecnie pozostawiają lekarzom niewiele możliwości.
Cytowanie: Ye, Y., Zhang, K., Wang, Y. et al. Biomimetic metal-drug coordination nanoplatform to counteract drug resistance in Pseudomonas aeruginosa via energy disruption. Nat Commun 17, 2808 (2026). https://doi.org/10.1038/s41467-026-69712-6
Słowa kluczowe: oporność na środki przeciwbakteryjne, Pseudomonas aeruginosa, terapia nanopartykularna, metabolizm energetyczny, antybiotyki beta-laktamowe