Clear Sky Science · fr
Nanoplates-forme biomimétique métal-médicament pour contrer la résistance aux antibiotiques chez Pseudomonas aeruginosa via la perturbation de l’énergie
Pourquoi les infections résistantes aux médicaments nous concernent tous
Les infections résistantes aux antibiotiques rendent des maladies autrefois faciles à traiter plus difficiles et plus dangereuses à guérir. Dans les hôpitaux, des bactéries courantes apprennent à échapper à nos meilleurs médicaments, transformant des pneumonies ou des infections de plaies de routine en crises potentiellement mortelles. Cette étude décrit une nouvelle façon de « réactiver » un ancien antibiotique contre un germe particulièrement tenace en coupant l’approvisionnement énergétique de la bactérie plutôt qu’en inventant un médicament entièrement nouveau.
Un germe pulmonaire tenace qui se moque des antibiotiques
Pseudomonas aeruginosa est une bactérie robuste qui provoque souvent des infections pulmonaires graves, en particulier chez les personnes dont les défenses sont affaiblies, comme celles atteintes de mucoviscidose ou sous chimiothérapie. Elle résiste aux traitements en bloquant l’entrée des médicaments par sa membrane externe et en expulsant activement les antibiotiques hors de la cellule. Parallèlement, le développement mondial de nouveaux antibiotiques — surtout ceux efficaces contre ce type de bactérie à Gram négatif — a été maigre pendant des décennies. Les chercheurs se sont donc concentrés sur un objectif différent : rendre les antibiotiques existants à nouveau puissants en désarmant les systèmes de résistance intrinsèques de la bactérie.
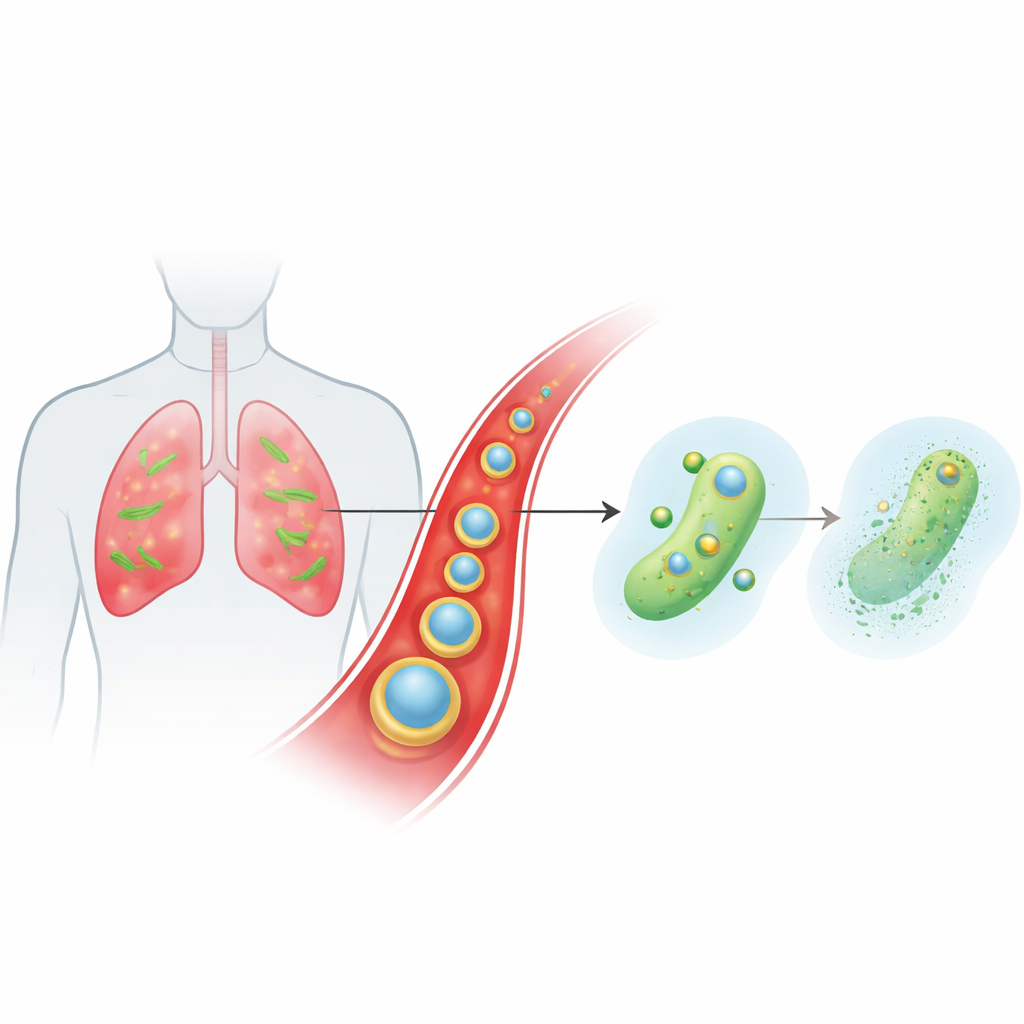
Un transporteur intelligent qui rejoint la circulation jusqu’aux foyers d’infection
L’équipe a conçu une particule minuscule et stratifiée appelée Ce‑Car@EV pour délivrer une bêta‑lactamine classique, la carbénicilline, conjointement au cérium, un ion métallique à chimie singulière. Le cœur interne est un polymère de coordination à l’échelle nanométrique dans lequel les molécules de carbénicilline se lient aux ions cérium, créant une structure poreuse à forte charge en médicament qui se désagrège en conditions légèrement acides. Ce cœur est ensuite enveloppé dans des vésicules extracellulaires naturelles issues de plantes de gingembre. Ces vésicules végétales aident les particules à échapper à l’élimination par le système immunitaire, à rester plus longtemps dans la circulation et à s’accumuler préférentiellement dans les tissus pulmonaires enflammés et infectés où les vaisseaux sanguins sont perméables et les cellules immunitaires activées. Une fois arrivées dans le microenvironnement acide de l’infection, les particules se déstructurent et libèrent à la demande à la fois la carbénicilline et les ions cérium.
Priver les bactéries d’énergie pour arrêter la résistance aux médicaments
À l’intérieur des cellules bactériennes, l’adénosine triphosphate (ATP) sert de monnaie énergétique universelle, alimentant tout, de la construction de la paroi cellulaire aux pompes d’efflux qui expulsent les antibiotiques. Les ions cérium peuvent décomposer l’ATP et perturber la chaîne de réactions qui la produit normalement. Les tests en laboratoire ont montré que lorsque des P. aeruginosa résistantes rencontraient Ce‑Car@EV dans un environnement acide similaire à celui des foyers d’infection, les nanoparticules libéraient du cérium et de la carbénicilline, réduisant fortement la survie bactérienne. Le cérium aidait non seulement la carbénicilline à se lier plus fermement à sa cible protéique impliquée dans la construction de la paroi, mais épuisait aussi l’ATP et altérait des étapes clés de la respiration bactérienne. En conséquence, la « batterie » protonique à travers la membrane bactérienne s’effondra et les pompes d’efflux qui éliminent normalement les médicaments se retrouvèrent sans puissance.
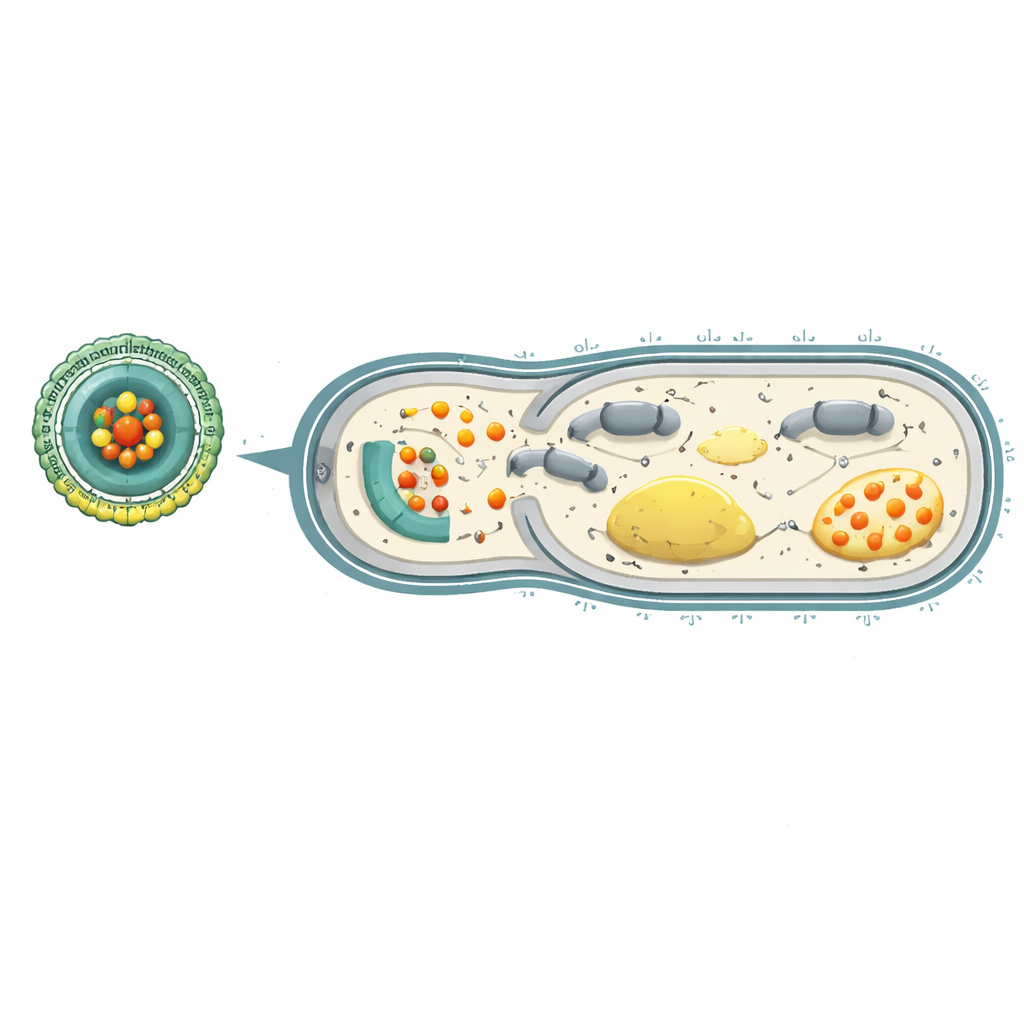
Renverser la résistance et protéger les poumons
Pour vérifier si cette stratégie inversait réellement la résistance, les chercheurs ont cultivé P. aeruginosa pendant de nombreuses générations en présence soit de carbénicilline libre soit de la plateforme Ce‑Car@EV. Les bactéries exposées uniquement à l’antibiotique sont rapidement devenues fortement résistantes, nécessitant 256 fois plus de médicament pour être contrôlées. En revanche, celles traitées à plusieurs reprises avec Ce‑Car@EV développèrent beaucoup moins de résistance. Des analyses génétiques ont révélé que les gènes impliqués dans la production d’énergie, la respiration et les pompes d’efflux multirésistantes étaient réduits chez les bactéries traitées avec la nanoplatforme. Chez des souris atteintes d’une pneumonie sévère à P. aeruginosa résistante aux médicaments, l’administration intraveineuse de Ce‑Car@EV s’est fortement accumulée dans les poumons infectés, a réduit de façon spectaculaire le nombre de bactéries là‑bas et dans d’autres organes, a diminué l’œdème et les dommages tissulaires pulmonaires et a amélioré la survie, tout en montrant une toxicité minimale dans les analyses sanguines et les examens des organes.
Ce que cela pourrait signifier pour les traitements futurs
En combinant un antibiotique bien connu avec un ion métallique à l’intérieur d’une enveloppe d’inspiration naturelle, ce travail propose une feuille de route pour déjouer les bactéries résistantes sans compter uniquement sur de nouveaux médicaments. Les particules Ce‑Car@EV ciblent les poumons enflammés, se désagrègent dans la niche d’infection acide, puis désactivent les systèmes énergétiques et d’efflux de la bactérie pour que la carbénicilline puisse à nouveau agir. Si des approches similaires s’avèrent sûres et efficaces chez l’humain, elles pourraient prolonger la durée d’utilité des antibiotiques existants et offrir de nouvelles options contre les infections multirésistantes qui laissent actuellement peu de choix aux médecins.
Citation: Ye, Y., Zhang, K., Wang, Y. et al. Biomimetic metal-drug coordination nanoplatform to counteract drug resistance in Pseudomonas aeruginosa via energy disruption. Nat Commun 17, 2808 (2026). https://doi.org/10.1038/s41467-026-69712-6
Mots-clés: résistance antimicrobienne, Pseudomonas aeruginosa, thérapie par nanoparticules, métabolisme énergétique, antibiotiques bêta‑lactamines