Clear Sky Science · pt
Nanoplataforma biomimética de coordenação metal-fármaco para combater a resistência medicamentosa em Pseudomonas aeruginosa por meio da interrupção de energia
Por que infecções resistentes a medicamentos nos importam a todos
Infecções resistentes a antibióticos estão tornando doenças antes tratáveis mais difíceis e perigosas de curar. Em hospitais, bactérias comuns aprendem a escapar dos nossos melhores remédios, transformando uma pneumonia rotineira ou uma infecção de ferida em crises potencialmente fatais. Este estudo descreve uma nova forma de “reacordar” um antibiótico antigo contra um microrganismo particularmente persistente ao cortar o suprimento de energia da bactéria em vez de inventar um fármaco totalmente novo.
Um germe pulmonar persistente que ignora medicamentos
Pseudomonas aeruginosa é uma bactéria resistente que frequentemente causa infecções pulmonares graves, especialmente em pessoas com defesas enfraquecidas, como portadores de fibrose cística ou pacientes com imunossupressão por quimioterapia. Ela resiste ao tratamento bloqueando a entrada do fármaco através da membrana externa e bombeando ativamente os antibióticos para fora da célula. Ao mesmo tempo, a linha de desenvolvimento global de antibióticos novos — especialmente os eficazes contra esse tipo de bactéria Gram-negativa — tem sido escassa por décadas. Os pesquisadores, portanto, focaram em um objetivo diferente: tornar antibióticos existentes eficazes novamente neutralizando os sistemas de resistência embutidos na bactéria.
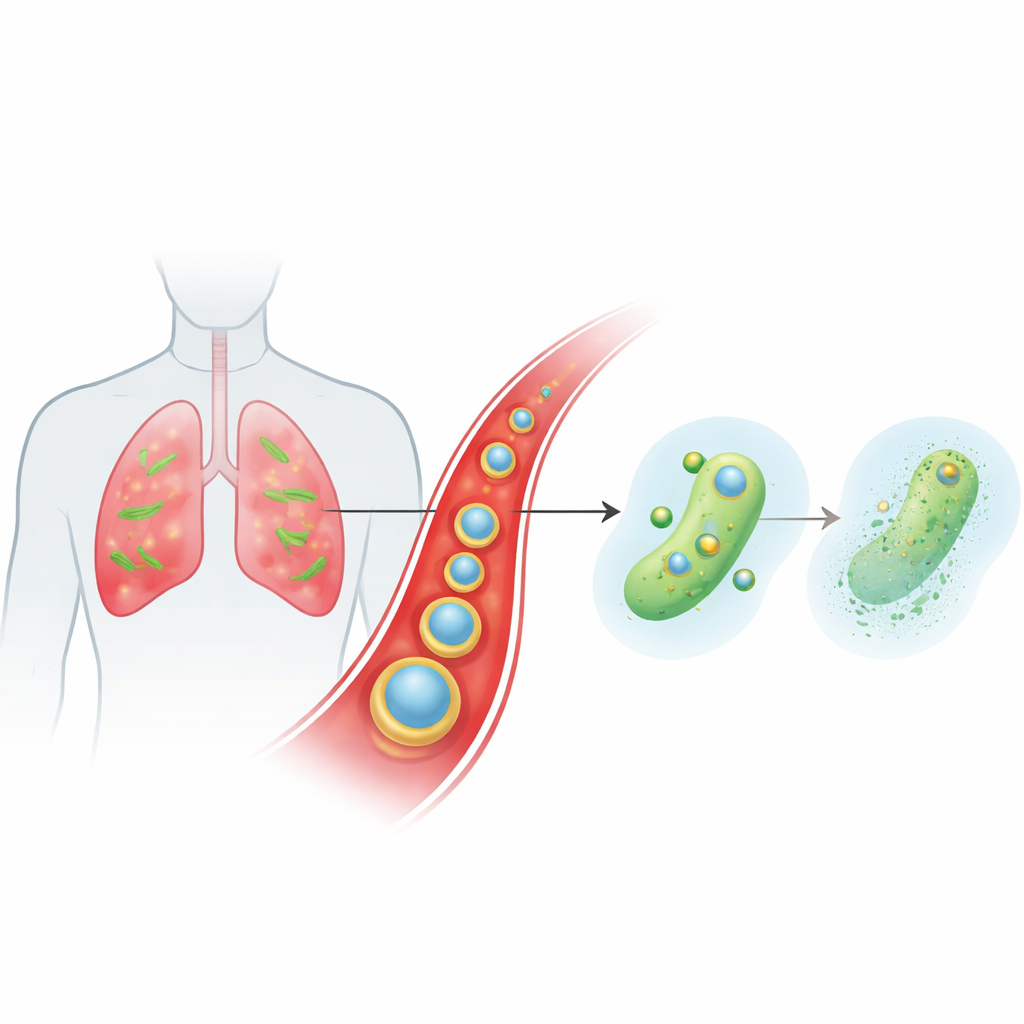
Um transportador inteligente que percorre a corrente sanguínea até os locais da infecção
A equipe projetou uma partícula minúscula e em camadas chamada Ce-Car@EV para entregar um antibiótico beta-lactâmico clássico, a carbenicilina, juntamente com cério, um íon metálico de química incomum. O núcleo interno é um polímero de coordenação em escala nanométrica no qual moléculas de carbenicilina se ligam a íons de cério, criando uma estrutura porosa com alta carga de fármaco que se desfaz em condições levemente ácidas. Esse núcleo é então revestido por vesículas extracelulares naturais colhidas de plantas de gengibre. Essas vesículas vegetais ajudam as partículas a escapar da depuração imune, permanecerem mais tempo na corrente sanguínea e se acumularem preferencialmente no tecido pulmonar inflamado e infectado, onde os vasos sanguíneos estão mais permeáveis e as células imunes ativadas. Quando as partículas chegam ao microambiente ácido da infecção, sua estrutura se afrouxa e libera sob demanda tanto a carbenicilina quanto os íons de cério.
Privar bactérias de energia para interromper a resistência a medicamentos
Dentro das células bacterianas, o trifosfato de adenosina (ATP) atua como a moeda energética universal, alimentando tudo, desde a construção da parede celular até as bombas de efluxo que expulsam antibióticos. Íons de cério são capazes de degradar ATP e perturbar a cadeia de reações que normalmente o gera. Testes laboratoriais mostraram que, quando P. aeruginosa resistente encontrou Ce-Car@EV em um ambiente ácido similar ao dos sítios de infecção, as nanopartículas liberaram cério e carbenicilina, reduzindo drasticamente a sobrevivência bacteriana. O cério não apenas ajudou a carbenicilina a se ligar mais fortemente ao seu alvo proteico responsável pela construção da parede celular, mas também esgotou o ATP e prejudicou etapas-chave da respiração bacteriana. Como resultado, a “bateria” movida por prótons através da membrana bacteriana colapsou e as bombas de efluxo que normalmente removem os fármacos ficaram sem energia.
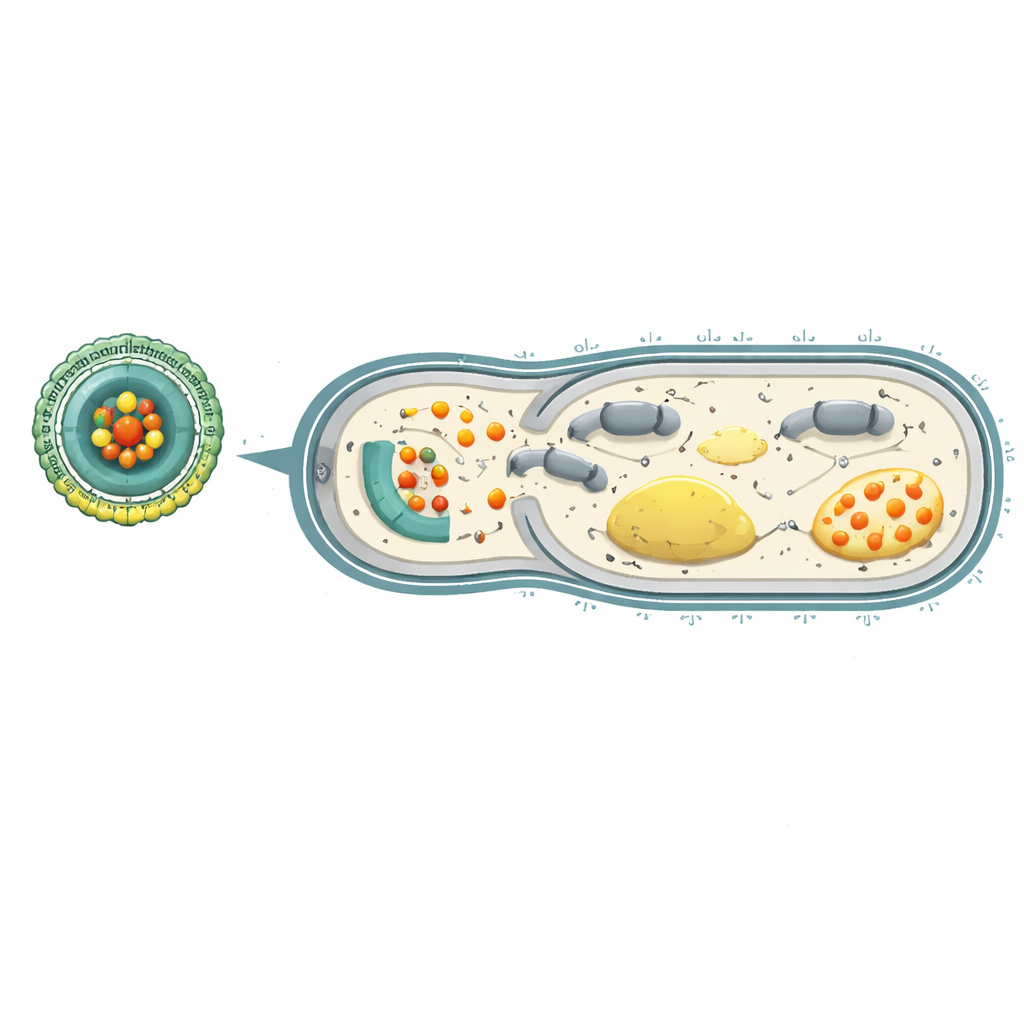
Reverter a resistência e proteger os pulmões
Para verificar se essa estratégia realmente reverteu a resistência, os pesquisadores cultivaram P. aeruginosa por muitas gerações na presença de carbenicilina livre ou da plataforma Ce-Car@EV. Bactérias expostas apenas ao antibiótico rapidamente se tornaram altamente resistentes, precisando de 256 vezes mais fármaco para serem controladas. Em contraste, aquelas tratadas repetidamente com Ce-Car@EV desenvolveram bem menos resistência. Análises genéticas revelaram que genes envolvidos na produção de energia, na respiração e nas bombas de efluxo multirresistentes foram reduzidos em bactérias tratadas com a nanoplataforma. Em camundongos com pneumonia grave por P. aeruginosa resistente a medicamentos, a administração intravenosa de Ce-Car@EV se acumulou fortemente nos pulmões infectados, reduziu dramaticamente as contagens bacterianas lá e em outros órgãos, diminuiu o inchaço e danos teciduais pulmonares e melhorou a sobrevivência, tudo isso exibindo toxicidade mínima em exames de sangue e de órgãos.
O que isso pode significar para tratamentos futuros
Ao combinar um antibiótico conhecido com um íon metálico dentro de um invólucro de entrega inspirado na natureza, este trabalho oferece um modelo para superar bactérias resistentes sem depender apenas de novos fármacos. As partículas Ce-Car@EV se dirigem a pulmões inflamados, se desfazem no nicho ácido da infecção e então desligam os sistemas de energia e de bombeamento de fármacos da bactéria para que a carbenicilina volte a ser eficaz. Se abordagens semelhantes se mostrarem seguras e eficazes em humanos, elas podem estender a vida útil de antibióticos existentes e fornecer novas opções contra infecções multirresistentes que hoje deixam os médicos com poucas alternativas.
Citação: Ye, Y., Zhang, K., Wang, Y. et al. Biomimetic metal-drug coordination nanoplatform to counteract drug resistance in Pseudomonas aeruginosa via energy disruption. Nat Commun 17, 2808 (2026). https://doi.org/10.1038/s41467-026-69712-6
Palavras-chave: resistência antimicrobiana, Pseudomonas aeruginosa, terapia com nanopartículas, metabolismo energético, antibióticos beta-lactâmicos