Clear Sky Science · ar
نانومنصة تنسيق معدن-دواء مستوحاة من الطبيعة لمواجهة مقاومة الأدوية في Pseudomonas aeruginosa عبر تعطيل الطاقة
لماذا تهمنا العدوى المقاومة للأدوية جميعًا
تجعل العدوى المقاومة للمضادات الحيوية أمراضًا كانت قابلة للعلاج سابقًا أصعب وأكثر خطورة في الشفاء. في المستشفيات، تتعلم البكتيريا الشائعة كيفية التحايل على أفضل أدوية لدينا، مما يحول الالتهاب الرئوي الروتيني أو التهابات الجروح إلى أزمات مهددة للحياة. تصف هذه الدراسة طريقة جديدة «لإعادة تنشيط» مضاد حيوي قديم ضد جرثوم عنيد بشكل خاص عن طريق قطع إمداد الطاقة للبكتيريا بدلًا من اختراع دواء جديد كليًا.
جرثوم رئوي عنيد يتجاهل الأدوية
تعد Pseudomonas aeruginosa بكتيريا متينة غالبًا ما تسبب إصابات رئوية خطيرة، خاصة لدى الأشخاص ذوي الدفاعات الضعيفة، مثل مرضى التليف الكيسي أو المصابين بقمع المناعة الناتج عن العلاج الكيميائي. تقاوم العلاج عن طريق منع دخول الدواء عبر غشائها الخارجي وبضخ المضادات الحيوية خارج الخلية بنشاط. في الوقت نفسه، كان خط إنتاج المضادات الحيوية الجديدة عالميًا—وخاصة تلك الفعالة ضد هذا النوع من البكتيريا سالبة الغرام—شحيحًا لعقود. لذا ركز الباحثون على هدف مختلف: إعادة قوة المضادات الحيوية الحالية عن طريق تعطيل نظم المقاومة المدمجة في البكتيريا.
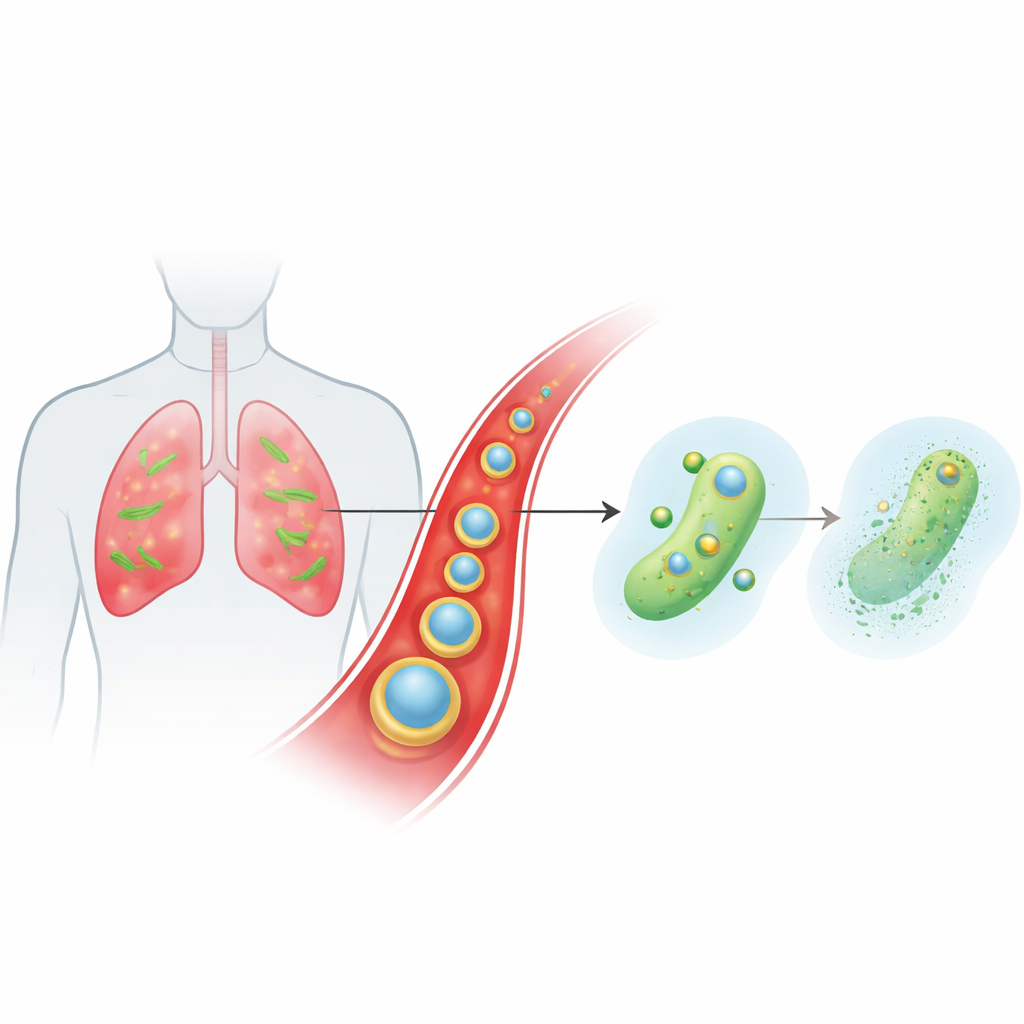
حامل ذكي يركب مجرى الدم إلى مواقع العدوى
صمم الفريق جسيمًا صغيرًا مُصفًفًا يُسمى Ce-Car@EV ليحمل مضادًا بيتا‑لاكتاميًا كلاسيكيًا، الكاربينيسلِين، مع عنصر السيرِيوم، أيون فلزي بخصائص كيميائية غير عادية. النواة الداخلية عبارة عن بوليمر تنسيقي بحجم النانو ترتبط فيه جزيئات الكاربينيسلِين بأيونات السيرِيوم، مكونة بنية مسامِيَّة ذات تحميل دوائي عالٍ تتفكك في ظروف حمضية خفيفة. تُلف هذه النواة بحويصلات خارج خلوية طبيعية مُستخرجة من نبات الزنجبيل. تساعد هذه الحويصلات النباتية الجسيمات على التملص من الإزالة المناعية، والبقاء فترة أطول في مجرى الدم، والتراكم تفضيليًا في نسيج الرئة الملتهب والمصاب حيث تكون الأوعية الدموية متسربة والخلايا المناعية منشطة. بمجرد وصول الجسيمات إلى البيئة الميكروحمضية للعدوى، تترقق بنيتها وتُطلق كلًا من الكاربينيسلِين وأيونات السيرِيوم حسب الحاجة.
تجويع البكتيريا من الطاقة لإيقاف المقاومة الدوائية
داخل الخلايا البكتيرية، يعمل الأدينوسين ثلاثي الفوسفات (ATP) كعملة طاقة شاملة، ويزود كل شيء بالطاقة من بناء جدار الخلية إلى مضخات الطرد التي تطرد المضادات الحيوية. تستطيع أيونات السيرِيوم تكسير ATP وإرباك سلسلة التفاعلات التي تُنتجه عادة. أظهرت الاختبارات المخبرية أنه عندما واجهت P. aeruginosa المقاومة Ce-Car@EV في بيئة حمضية مشابهة لمواقع العدوى، أطلقت الجسيمات النانوية السيرِيوم والكاربينيسلِين، مما قلّل بحدة من بقاء البكتيريا. لم يساعد السيرِيوم الكاربينيسلِين فحسب على الارتباط بقوة أكبر بمستهدفه البروتيني المسؤول عن بناء جدار الخلية، بل استنزف أيضًا ATP وأعاق خطوات رئيسية في تنفس البكتيريا. ونتيجة لذلك، انهارت «البطارية» المدفوعة بالبروتون عبر غشاء البكتيريا وفقدت مضخات الطرد التي تزيل الأدوية مصدر طاقتها.
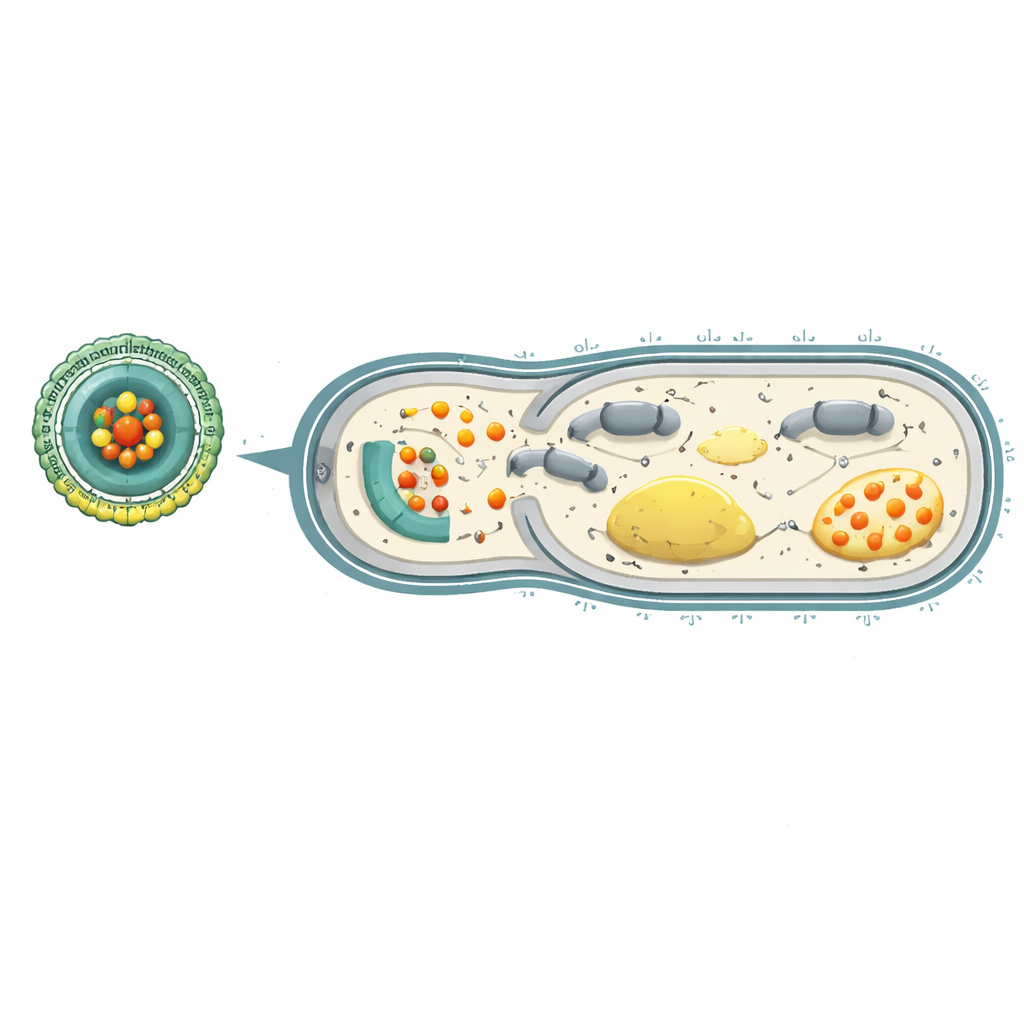
عكس المقاومة وحماية الرئتين
ليروا ما إذا كانت هذه الاستراتيجية قد أعادت المقاومة فعلاً إلى الخلف، نما الباحثون P. aeruginosa لعدة أجيال في حضور إما الكاربينيسلِين الحر أو منصة Ce-Car@EV. أصبحت البكتيريا المعرضة للمضاد الحيوي وحده مقاومة بسرعة كبيرة، حيث احتاجت إلى جرعة تزيد 256 مرة للسيطرة عليها. بالمقابل، طورت البكتيريا المعالجة مرارًا وتكرارًا بـ Ce-Car@EV مقاومة أقل بكثير. كشفت التحليلات الوراثية أن الجينات المشاركة في إنتاج الطاقة والتنفس ومضخات الطرد متعددة الأدوية قد تم خفض نشاطها في البكتيريا المعالجة بالمنصة النانوية. في فئران تعاني من التهاب رئوي شديد بموجِب P. aeruginosa المقاومة للأدوية، تراكم Ce-Car@EV وريدياً بقوة في الرئتين المصابتين، وخفّض بشكل دراماتيكي أعداد البكتيريا هناك وفي أعضاء أخرى، وقلّل من التورم وتلف أنسجة الرئة، وحسّن البقاء على قيد الحياة، كل ذلك مع إظهار سميّة قليلة في اختبارات الدم وفحوصات الأعضاء.
ماذا قد يعني هذا للعلاجات المستقبلية
بجمع مضاد حيوي مألوف مع أيون فلزي داخل غلاف توصيل مستوحى من الطبيعة، تقدم هذه الدراسة مخططًا ذكيًا للتغلب على البكتيريا المقاومة دون الاعتماد حصريًا على أدوية جديدة. تستهدف جسيمات Ce-Car@EV الرئتين الملتهبتين، وتتفتت في المكان الحمضي للعدوى، ثم تغلق أنظمة طاقة البكتيريا ومضخات الطرد حتى يتمكن الكاربينيسلِين من العمل مجددًا. إذا أثبتت مقاربات مماثلة أمانها وفعاليتها في البشر، فقد تطيل العمر المفيد للمضادات الحيوية الحالية وتوفر خيارات جديدة ضد العدوى متعددة المقاومة التي تترك الأطباء حاليًا مع خيارات قليلة.
الاستشهاد: Ye, Y., Zhang, K., Wang, Y. et al. Biomimetic metal-drug coordination nanoplatform to counteract drug resistance in Pseudomonas aeruginosa via energy disruption. Nat Commun 17, 2808 (2026). https://doi.org/10.1038/s41467-026-69712-6
الكلمات المفتاحية: مقاومة المضادات الحيوية, Pseudomonas aeruginosa, علاج بالجسيمات النانوية, استقلاب الطاقة, مضادات بيتا-لاكتام