Clear Sky Science · es
Nanoplataforma biomimética de coordinación metal-fármaco para contrarrestar la resistencia a fármacos en Pseudomonas aeruginosa mediante la interrupción energética
Por qué las infecciones resistentes a fármacos nos importan a todos
Las infecciones resistentes a los antibióticos están convirtiendo enfermedades que antes eran tratables en padecimientos más difíciles y peligrosos de curar. En los hospitales, bacterias comunes aprenden a evadir nuestros mejores medicamentos, transformando una neumonía rutinaria o una infección de herida en una crisis potencialmente mortal. Este estudio describe una nueva forma de “reactivar” un antibiótico antiguo frente a un germen particularmente tenaz cortando el suministro de energía de la bacteria en lugar de inventar un fármaco completamente nuevo.
Un germen pulmonar tenaz que ignora los fármacos
Pseudomonas aeruginosa es una bacteria resistente que con frecuencia causa infecciones pulmonares graves, especialmente en personas con defensas debilitadas, como quienes padecen fibrosis quística o tienen supresión inmune por quimioterapia. Se defiende de los tratamientos bloqueando la entrada de fármacos a través de su membrana externa y bombeando activamente los antibióticos fuera de la célula. Al mismo tiempo, la canalización global de antibióticos totalmente nuevos —especialmente los efectivos contra este tipo de bacterias Gram negativas— ha sido escasa durante décadas. Por eso los investigadores se centraron en un objetivo diferente: devolver potencia a los antibióticos existentes desactivando los sistemas de resistencia incorporados en la bacteria.
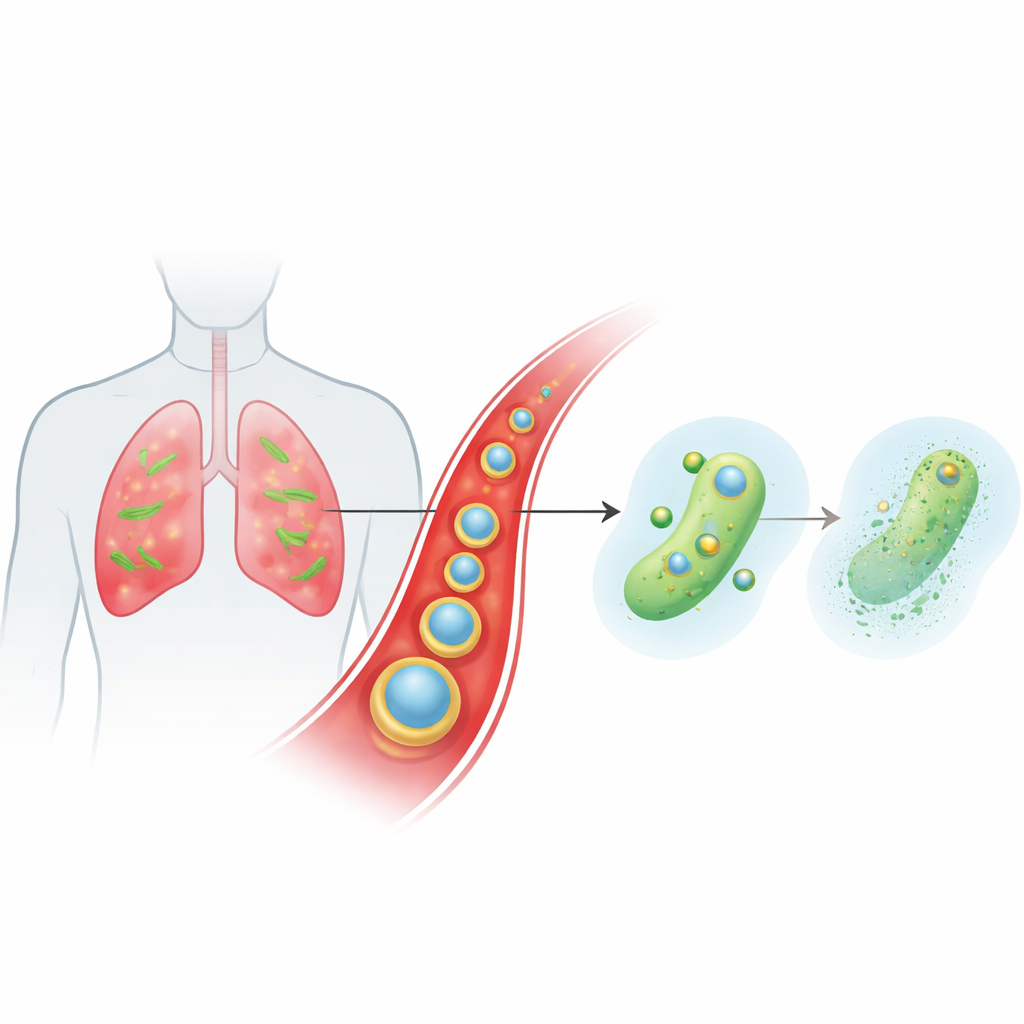
Un portador inteligente que viaja por la sangre hasta los sitios de infección
El equipo diseñó una partícula diminuta y estratificada llamada Ce-Car@EV para administrar un antibiótico beta-lactámico clásico, carbenicilina, junto con cerio, un ion metálico de química inusual. El núcleo interno es un polímero de coordinación a escala nanométrica en el que las moléculas de carbenicilina se enlazan con iones de cerio, creando una estructura porosa con alta carga de fármaco que se descompone en condiciones ligeramente ácidas. Este núcleo se recubre con vesículas extracelulares naturales obtenidas de plantas de jengibre. Estas vesículas vegetales ayudan a las partículas a eludir la eliminación inmunitaria, permanecer más tiempo en el torrente sanguíneo y acumularse preferentemente en el tejido pulmonar inflamado e infectado, donde los vasos sanguíneos son permeables y las células inmunitarias están activadas. Cuando las partículas llegan al microambiente ácido de la infección, su estructura se afloja y libera carbenicilina e iones de cerio según se necesite.
Privar a las bacterias de energía para detener la resistencia a fármacos
Dentro de las células bacterianas, el trifosfato de adenosina (ATP) actúa como la moneda energética universal, alimentando desde la construcción de la pared celular hasta las bombas de eflujo que expulsan antibióticos. Los iones de cerio son capaces de descomponer el ATP y alterar la cadena de reacciones que normalmente lo genera. Pruebas de laboratorio mostraron que cuando P. aeruginosa resistente se encontró con Ce-Car@EV en un entorno ácido similar al de los sitios de infección, las nanopartículas liberaron cerio y carbenicilina, reduciendo drásticamente la supervivencia bacteriana. El cerio no solo ayudó a que la carbenicilina se uniera con más firmeza a su objetivo proteico que construye la pared celular, sino que también agotó el ATP e impidió pasos clave en la respiración bacteriana. Como resultado, la “batería” impulsada por protones a través de la membrana bacteriana colapsó y las bombas de eflujo que normalmente eliminan los fármacos se quedaron sin energía.
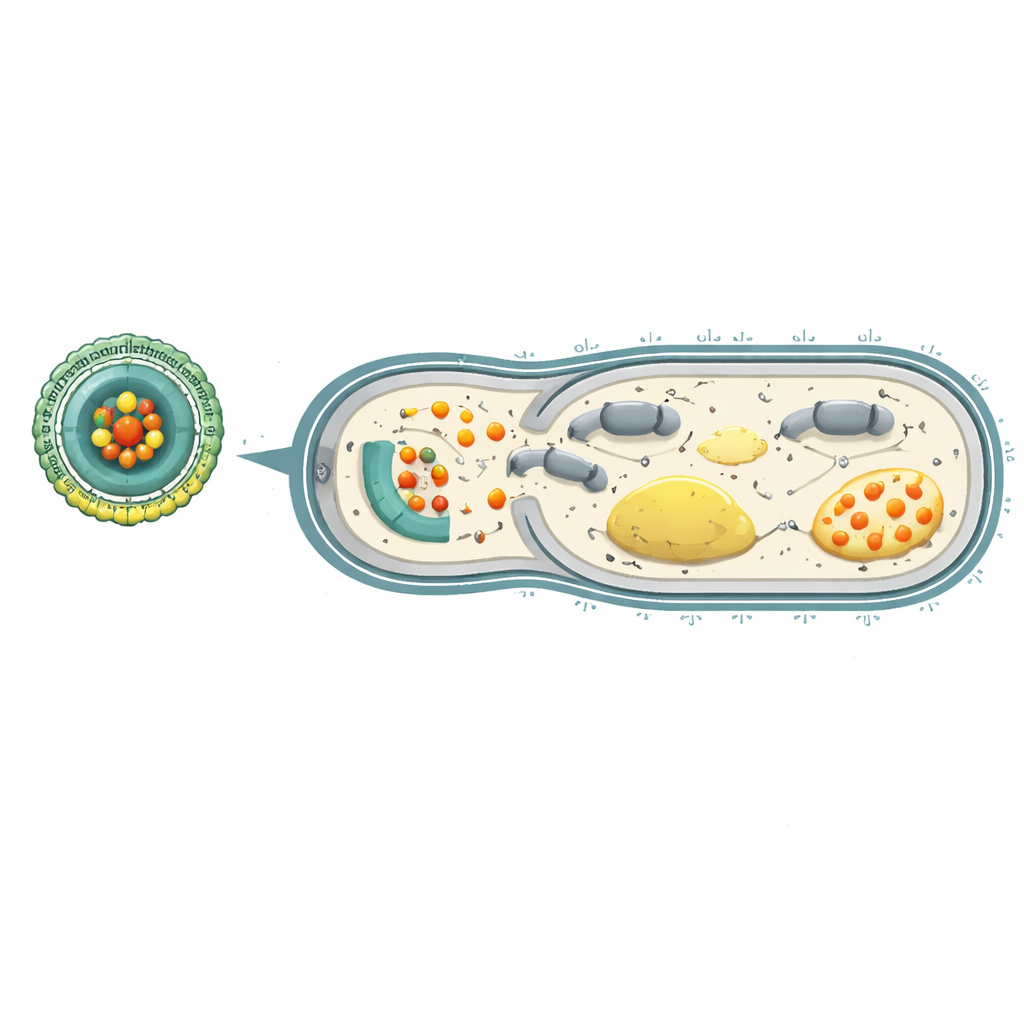
Revirtiendo la resistencia y protegiendo los pulmones
Para comprobar si esta estrategia realmente revertía la resistencia, los investigadores cultivaron P. aeruginosa durante muchas generaciones en presencia de carbenicilina libre o de la plataforma Ce-Car@EV. Las bacterias expuestas solo al antibiótico desarrollaron resistencia rápidamente, necesitando 256 veces más fármaco para controlarse. En contraste, las tratadas repetidamente con Ce-Car@EV desarrollaron mucha menos resistencia. Los análisis genéticos revelaron que en las bacterias tratadas con la nanoplataforma se redujo la expresión de genes implicados en la producción de energía, la respiración y las bombas de eflujo multidroga. En ratones con neumonía grave por P. aeruginosa resistente a fármacos, la administración intravenosa de Ce-Car@EV se acumuló fuertemente en los pulmones infectados, redujo drásticamente los recuentos bacterianos allí y en otros órganos, disminuyó la inflamación y el daño tisular pulmonar, y mejoró la supervivencia, todo ello mostrando una toxicidad mínima en análisis de sangre y exámenes de órganos.
Qué podría significar esto para tratamientos futuros
Al combinar un antibiótico conocido con un ion metálico dentro de una cubierta de administración inspirada en la naturaleza, este trabajo ofrece un plan para burlar a las bacterias resistentes sin depender únicamente de fármacos nuevos. Las partículas Ce-Car@EV se dirigen a los pulmones inflamados, se descomponen en el nicho ácido de la infección y luego apagan los sistemas energéticos y de bombeo de drogas de la bacteria para que la carbenicilina pueda volver a actuar. Si enfoques similares demuestran ser seguros y eficaces en humanos, podrían prolongar la vida útil de los antibióticos existentes y ofrecer nuevas opciones frente a infecciones multirresistentes que actualmente dejan a los médicos con pocas alternativas.
Cita: Ye, Y., Zhang, K., Wang, Y. et al. Biomimetic metal-drug coordination nanoplatform to counteract drug resistance in Pseudomonas aeruginosa via energy disruption. Nat Commun 17, 2808 (2026). https://doi.org/10.1038/s41467-026-69712-6
Palabras clave: resistencia antimicrobiana, Pseudomonas aeruginosa, terapia con nanopartículas, metabolismo energético, antibióticos beta-lactámicos