Clear Sky Science · nl
Biomimetisch metaal‑geneesmiddel coördinatie-nanoplatform om geneesmiddelresistentie bij Pseudomonas aeruginosa te bestrijden via energieontregeling
Waarom door geneesmiddelen resistente infecties ons allemaal aangaan
Antibioticaresistente infecties maken ziektes die vroeger behandelbaar waren steeds moeilijker en gevaarlijker te genezen. In ziekenhuizen leren veelvoorkomende bacteriën onze beste medicijnen te ontlopen, waardoor routinematige longontstekingen of wondinfecties levensbedreigende crises kunnen worden. Deze studie beschrijft een nieuwe manier om een ouder antibioticum weer “te wekken” tegen een bijzonder hardnekkig microbe door de energievoorziening van de bacterie af te knijpen in plaats van volledig nieuwe geneesmiddelen te ontwikkelen.
Een hardnekkige longbacterie die middelen afschudt
Pseudomonas aeruginosa is een taaie bacterie die vaak ernstige longinfecties veroorzaakt, vooral bij mensen met verzwakte afweer, zoals patiënten met cystische fibrose of chemotherapie‑gerelateerde immuunsuppressie. Ze weerstaat behandeling door de opname van medicijnen via het buitenmembraan te blokkeren en door actief antibiotica uit de cel te pompen. Tegelijkertijd is de mondiale pijplijn voor volledig nieuwe antibiotica—vooral tegen dit type Gram‑negatieve bacteriën—al decennialang dun. De onderzoekers richtten zich daarom op een andere aanpak: bestaande antibiotica weer krachtig maken door de ingebouwde resistentiesystemen van de bacterie uit te schakelen.
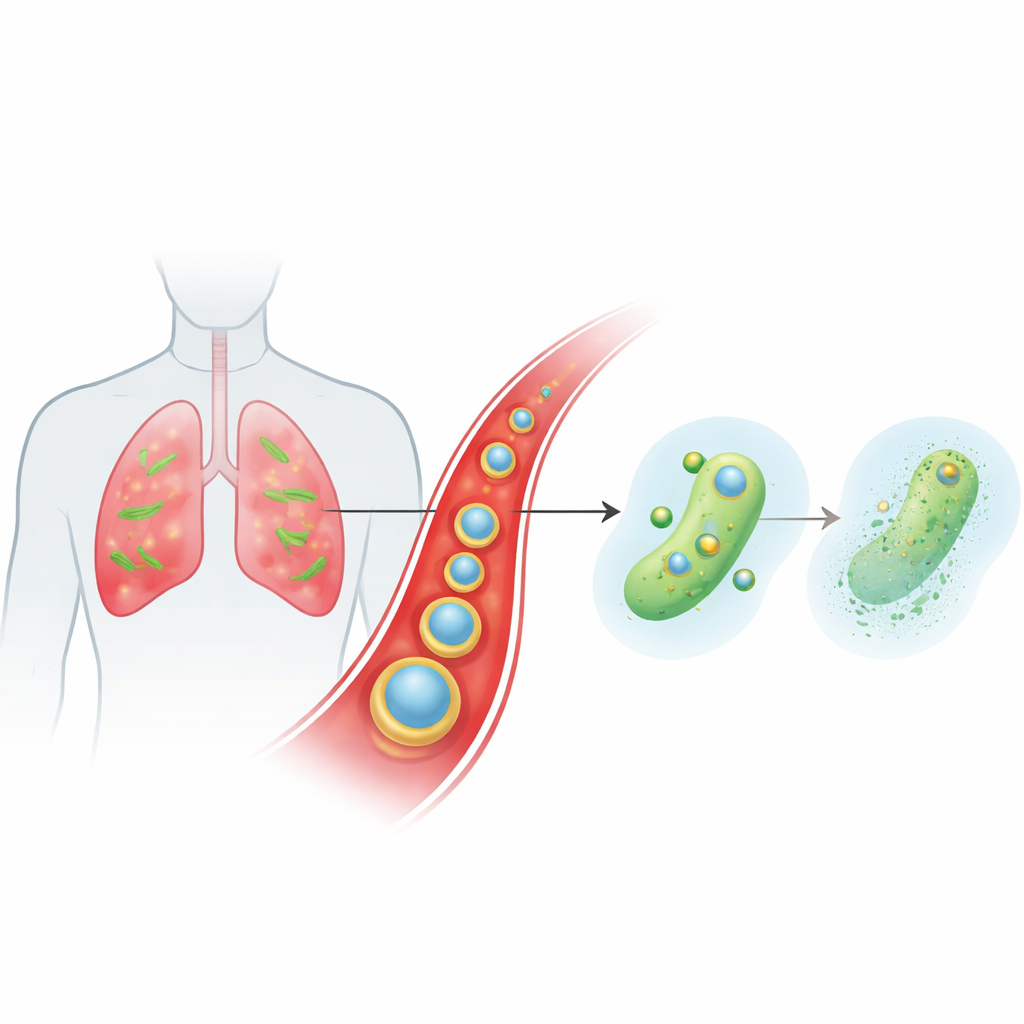
Een slimme drager die via de bloedbaan naar infectiehaarden rijdt
Het team ontwierp een minuscuul, gelaagd deeltje genaamd Ce‑Car@EV om een klassiek beta‑lactamantibioticum, carbenicilline, samen met cerium, een metaalion met ongewone chemie, af te leveren. De binnenkern is een nanoschaal coördinatiepolymeer waarin carbenicillinemoleculen zich binden aan ceriumionen, wat een poreuze structuur met hoge geneesmiddellading oplevert die uiteenvalt onder licht zure omstandigheden. Deze kern wordt vervolgens omhuld met natuurlijke extracellulaire vesikels gewonnen uit gemberplanten. Deze plantaardige vesikels helpen de deeltjes immuunonttrekking te ontwijken, langer in de bloedbaan te blijven en zich bij voorkeur op te hopen in ontstoken, geïnfecteerd longweefsel waar bloedvaten lek zijn en immuuncellen geactiveerd zijn. Zodra de deeltjes in de zure micro‑omgeving van de infectie aankomen, verslappen ze en geven ze op verzoek zowel carbenicilline als ceriumionen vrij.
Bacteriën van energie beroven om resistentie te stoppen
Binnen bacteriële cellen fungeert adenosinetrifosfaat (ATP) als de universele energievaluta en voedt alles, van de opbouw van de celwand tot de effluxpompen die antibiotica uitspuwen. Ceriumionen kunnen ATP afbreken en verstoren de keten van reacties die het normaal aanmaakt. Laboratoriumtests toonden aan dat wanneer resistente P. aeruginosa Ce‑Car@EV tegenkwam in een zure omgeving vergelijkbaar met infectieplaatsen, de nanodeeltjes cerium en carbenicilline vrijgaven en de bacteriële overleving sterk terugdrongen. Cerium hielp niet alleen dat carbenicilline steviger bindt aan zijn proteïnedoel dat de celwand bouwt, maar raakte ook ATP uitgeput en verstoorde sleutelstappen in de bacteriële ademhaling. Daardoor stortte de protongedreven “batterij” over het bacteriële membraan in en raakten de effluxpompen die gewoonlijk geneesmiddelen verwijderen zonder energie.
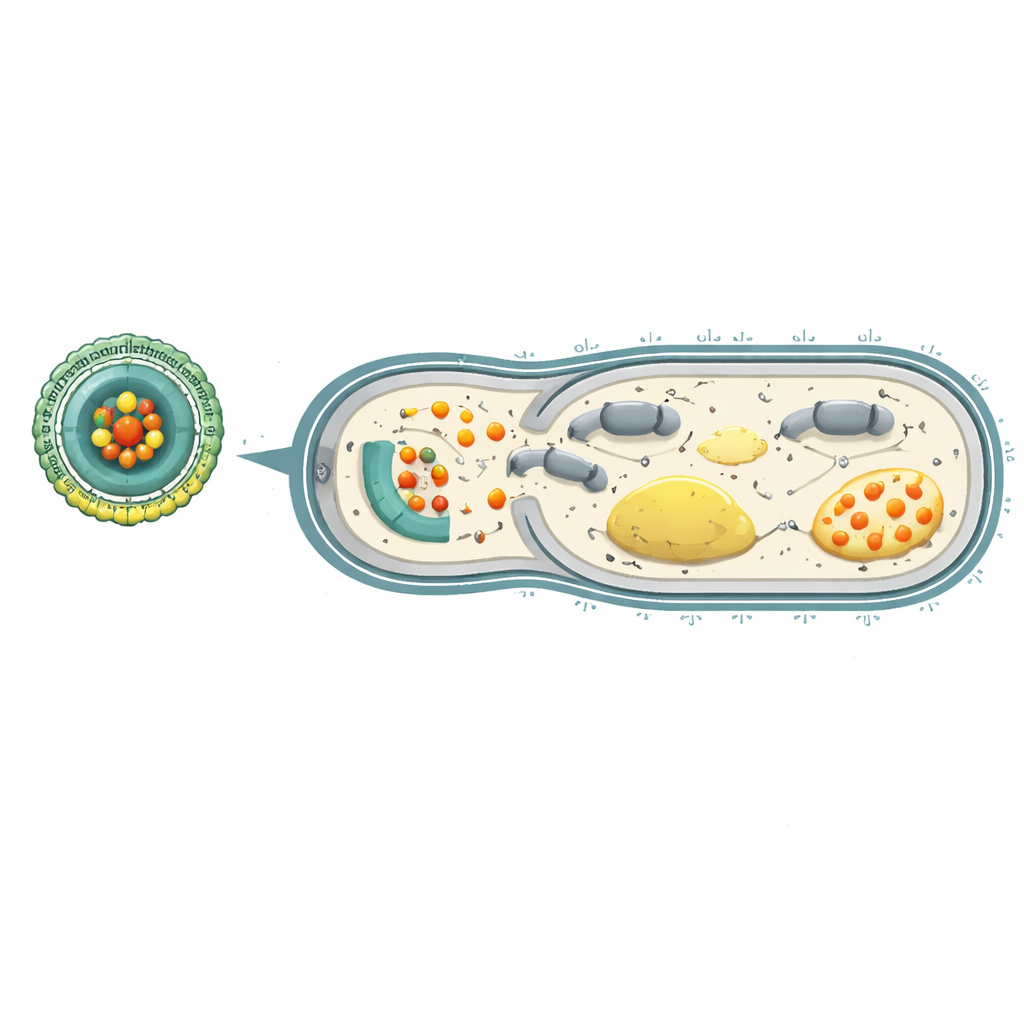
Resistentie terugdraaien en de longen beschermen
Om te onderzoeken of deze strategie de resistentie daadwerkelijk terugdraaide, lieten de onderzoekers P. aeruginosa vele generaties groeien in aanwezigheid van ofwel vrije carbenicilline ofwel het Ce‑Car@EV‑platform. Bacteriën die alleen aan het antibioticum werden blootgesteld, werden snel zeer resistent en hadden 256 keer meer geneesmiddel nodig om onder controle te blijven. Daarentegen ontwikkelden bacteriën die herhaaldelijk met Ce‑Car@EV werden behandeld veel minder resistentie. Genetische analyses toonden aan dat genen betrokken bij energieproductie, ademhaling en multidrug‑effluxpompen werden uitgeschakeld in bacteriën behandeld met het nanoplatform. Bij muizen met ernstige, geneesmiddelresistente P. aeruginosa‑pneumonie stapelde intraveneus toegediend Ce‑Car@EV zich sterk op in de geïnfecteerde longen, verlaagde daar en in andere organen de bacterietellingen dramatisch, verminderde longzwelling en weefselschade en verbeterde de overleving, terwijl in bloedtests en orgaanonderzoeken minimale toxiciteit werd waargenomen.
Wat dit kan betekenen voor toekomstige behandelingen
Door een bekend antibioticum te combineren met een metaalion in een door de natuur geïnspireerde afleveromhulling, biedt dit werk een blauwdruk om resistente bacteriën te slim af te zijn zonder uitsluitend op nieuwe geneesmiddelen te vertrouwen. De Ce‑Car@EV‑deeltjes richten zich op ontstoken longen, vallen uiteen in het zure infectieniche en schakelen vervolgens de energie‑ en geneesmiddelpompsystemen van de bacterie uit, zodat carbenicilline weer kan werken. Als soortgelijke benaderingen veilig en effectief blijken bij mensen, zouden ze de bruikbare levensduur van bestaande antibiotica kunnen verlengen en nieuwe opties kunnen bieden tegen multiresistente infecties waarvoor artsen nu weinig keuzes hebben.
Bronvermelding: Ye, Y., Zhang, K., Wang, Y. et al. Biomimetic metal-drug coordination nanoplatform to counteract drug resistance in Pseudomonas aeruginosa via energy disruption. Nat Commun 17, 2808 (2026). https://doi.org/10.1038/s41467-026-69712-6
Trefwoorden: antimicrobiële resistentie, Pseudomonas aeruginosa, nanodeeltjestherapie, energiewisseling, beta-lactamantibiotica