Clear Sky Science · ru
Биомиметическая наноплатформа координации металла и лекарства для противодействия лекарственной устойчивости Pseudomonas aeruginosa через нарушение энергообеспечения
Почему инфекции, устойчивые к препаратам, важны для каждого из нас
Инфекции, устойчивые к антибиотикам, делают ранее излечимые болезни более трудными и опасными для лечения. В больницах обычные бактерии учатся обходить наши лучшие лекарства, превращая рутинную пневмонию или инфицирование ран в угрожающие жизни кризисы. В этом исследовании описан новый способ «оживить» старый антибиотик против особенно упорного микроорганизма — не создавая полностью новый препарат, а лишая бактерию источников энергии.
Упрямый легочный возбудитель, который отмахивается от лекарств
Pseudomonas aeruginosa — выносливая бактерия, часто вызывающая тяжелые инфекции легких, особенно у людей с ослабленным иммунитетом, например при муковисцидозе или иммунодефиците после химиотерапии. Она сопротивляется лечению, блокируя проникновение препаратов через внешнюю мембрану и активно выкачивая антибиотики из клетки. В то же время глобальная разработка принципиально новых антибиотиков — особенно тех, что действуют на такие грамотрицательные бактерии — в течение десятилетий была скудной. Поэтому исследователи сосредоточились на другой задаче: вернуть силу существующим антибиотикам, обезоружив встроенные в бактерию механизмы резистентности.
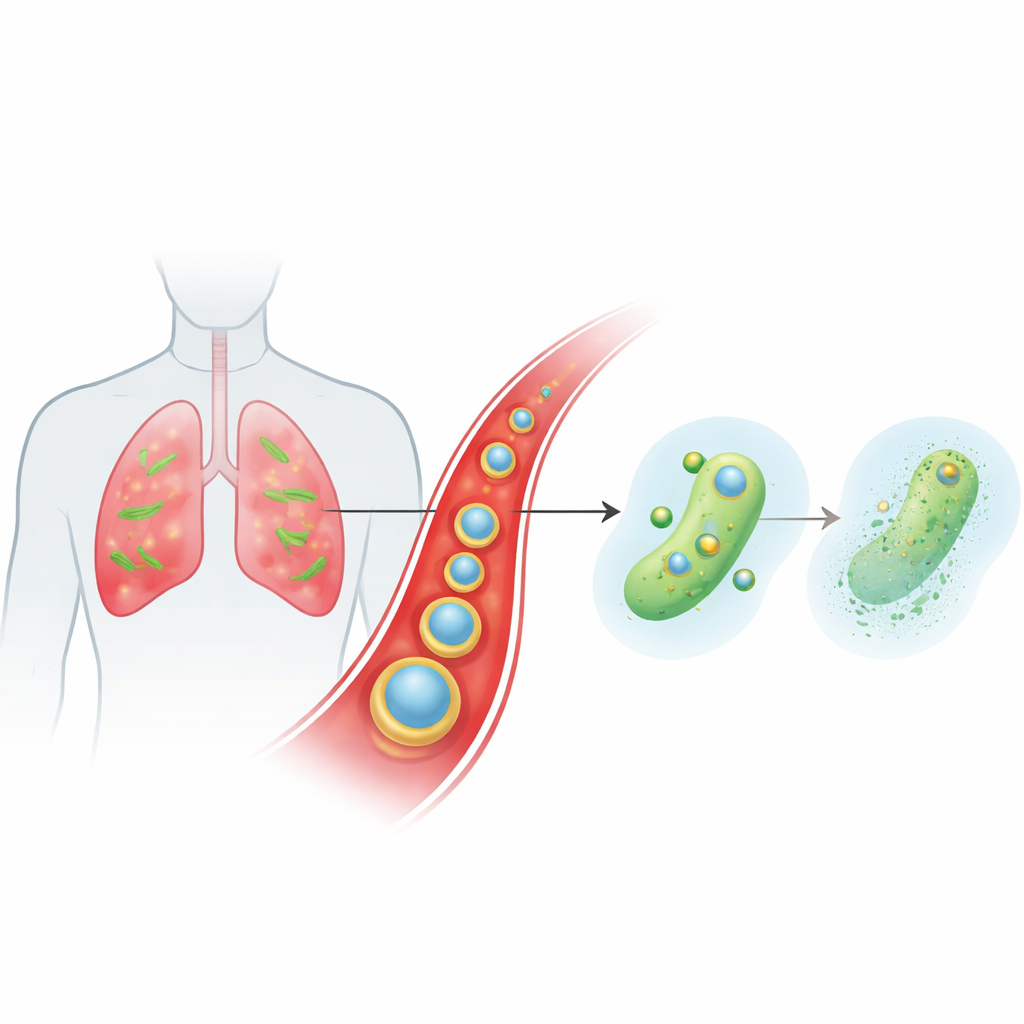
Умный носитель, который доставляет груз кровотоком к очагам инфекции
Команда разработала крошечную многослойную частицу под названием Ce-Car@EV для доставки классического бета-лактамного антибиотика карбенициллина вместе с церием — ионом металла с необычной химией. Внутреннее ядро представляет собой наномасштабный координационный полимер, в котором молекулы карбенициллина связаны ионами церия, образуя пористую структуру с высоким содержанием лекарства, разрушающуюся в слабо кислотных условиях. Это ядро затем покрывают натуральными внеклеточными везикулами, полученными из имбиря. Растительные везикулы помогают частицам избегать удаления иммунной системой, дольше циркулировать в крови и преимущественно накапливаться в воспаленной, инфицированной ткани легких, где сосуды проницаемы, а иммунные клетки активны. Попав в кислую микроокружение инфекции, частицы раскрываются и по требованию высвобождают и карбенициллин, и ионы церия.
Лишение бактерий энергии, чтобы подавить резистентность
Внутри бактериальных клеток аденозинтрифосфат (АТФ) действует как универсальная энергетическая валюта, обеспечивая всё — от синтеза клеточной стенки до работы насосов вывода антибиотиков. Ионы церия способны разрушать АТФ и нарушать цепочку реакций, которые его генерируют. Лабораторные испытания показали, что когда устойчивые штаммы P. aeruginosa сталкивались с Ce-Car@EV в кислой среде, похожей на очаги инфекции, наночастицы высвобождали церий и карбенициллин, резко снижая выживаемость бактерий. Церий не только усиливал связывание карбенициллина с его белковым мишенью, участвующим в построении стенки, но и истощал АТФ и нарушал ключевые этапы бактериального дыхания. В результате исчезла протонная «батарея» через бактериальную мембрану, и насосы вывода, обычно удаляющие лекарства, остались без энергии.
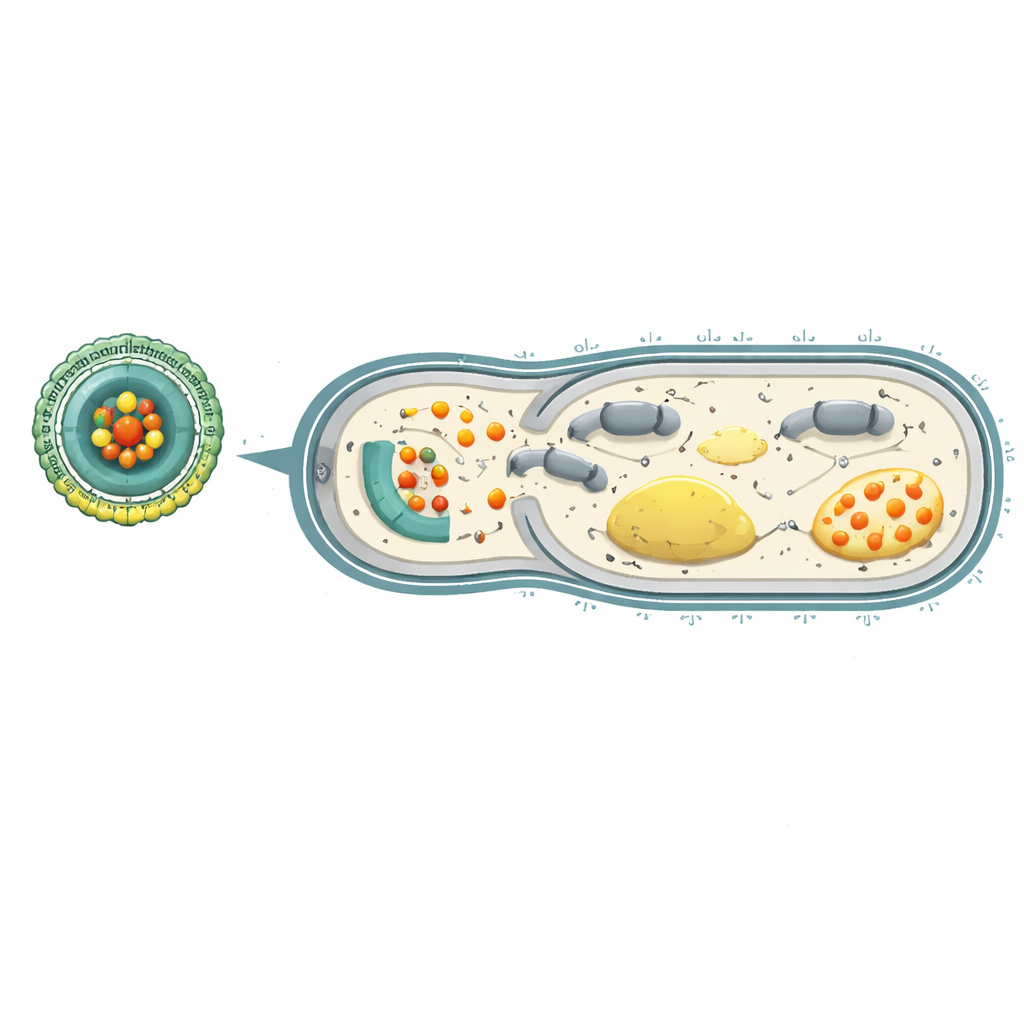
Обратный разворот резистентности и защита легких
Чтобы проверить, действительно ли эта стратегия обращает резистентность вспять, исследователи культивировали P. aeruginosa в течение многих поколений в присутствии либо свободного карбенициллина, либо платформы Ce-Car@EV. Бактерии, подвергшиеся воздействию только антибиотика, быстро становились высоко устойчивыми и требовали в 256 раз больше препарата для контроля. Напротив, те, что многократно лечились Ce-Car@EV, развили значительно меньшую степень резистентности. Генетический анализ показал, что у бактерий, обработанных наноплатформой, снижалась экспрессия генов, вовлеченных в производство энергии, дыхание и многокомпонентные насосы вывода лекарств. У мышей с тяжелой, устойчивой к препаратам пневмонией, вызванной P. aeruginosa, внутривенное введение Ce-Car@EV сильно накапливалось в инфицированных легких, драматически снижало число бактерий там и в других органах, уменьшало отек и повреждение ткани легких и повышало выживаемость, при этом показывая минимальную токсичность по результатам анализов крови и исследований органов.
Что это может значить для будущего лечения
Объединив знакомый антибиотик с ионом металла внутри натуралистичной доставляющей оболочки, эта работа предлагает план действий по перехитриванию устойчивых бактерий без полной зависимости от новых препаратов. Частицы Ce-Car@EV нацеливаются на воспаленные легкие, распадаются в кислой нише инфекции и затем отключают энергетические и «выпускающие» системы бактерии, чтобы карбенициллин снова мог подействовать. Если аналогичные подходы окажутся безопасными и эффективными у людей, они могут продлить срок полезного использования существующих антибиотиков и предоставить новые варианты против мультирезистентных инфекций, при которых врачи сейчас часто сталкиваются с ограниченным выбором.
Цитирование: Ye, Y., Zhang, K., Wang, Y. et al. Biomimetic metal-drug coordination nanoplatform to counteract drug resistance in Pseudomonas aeruginosa via energy disruption. Nat Commun 17, 2808 (2026). https://doi.org/10.1038/s41467-026-69712-6
Ключевые слова: антибактериальная резистентность, Pseudomonas aeruginosa, наночастичная терапия, энергетический метаболизм, бета-лактамные антибиотики