Clear Sky Science · zh
3-脱氧科林诺酮 B 的合成及其降低阿尔茨海默相关错误折叠蛋白的能力
用新的视角看阿尔茨海默病
阿尔茨海默病部分由错误折叠蛋白的团块驱动,这些团块会逐渐损害大脑,但现有治疗很少能清除这些有害沉积物。本研究介绍了一种实验室合成的、来源于罕见天然化合物的近亲,它能够更有效地到达大脑并同时直接作用于两种主要致病蛋白。通过将先进的化学合成、人工智能和动物实验相结合,研究人员展示了这种小分子如何瓦解有毒蛋白聚集体并在阿尔茨海默小鼠模型中改善记忆。
有局限性的天然分子
科学家此前发现了一种来自细菌的天然产物——科林内酯(collinolactone),它可以拆解由淀粉样β和 tau 形成的蛋白团块——这两种是阿尔茨海默病的标志性蛋白。然而,科林内酯难以从微生物来源中大量提取,并且对某些大脑区域(尤其是皮层,这是阿尔茨海默病受损严重的部位)的渗透性差。这些缺点使其难以作为实用药物开发。研究团队因此着手设计并合成一种相关分子,以保留科林内酯的有益活性,同时改善其稳定性和穿透大脑的能力。
构建更聪明的分子
研究人员利用现代有机合成方法构建了一种名为3-脱氧科林诺酮 B 的新化合物。他们将三种较简单的化学构件组装起来,然后诱导发生一种罕见的环化反应,该反应模拟了被认为在自然界中发生的一步。详尽的计算机计算解释了为何该反应有利于形成一种特定的三环构型,该构型比其他可能结构更稳定。所得分子相较原始天然产物稍微更偏亲脂,这一性质有助于其穿过血–脑屏障。重要的是,合成路线具有可放大性,这意味着在实验室里可以可靠地生产克级数量,便于广泛的生物学测试和未来优化。 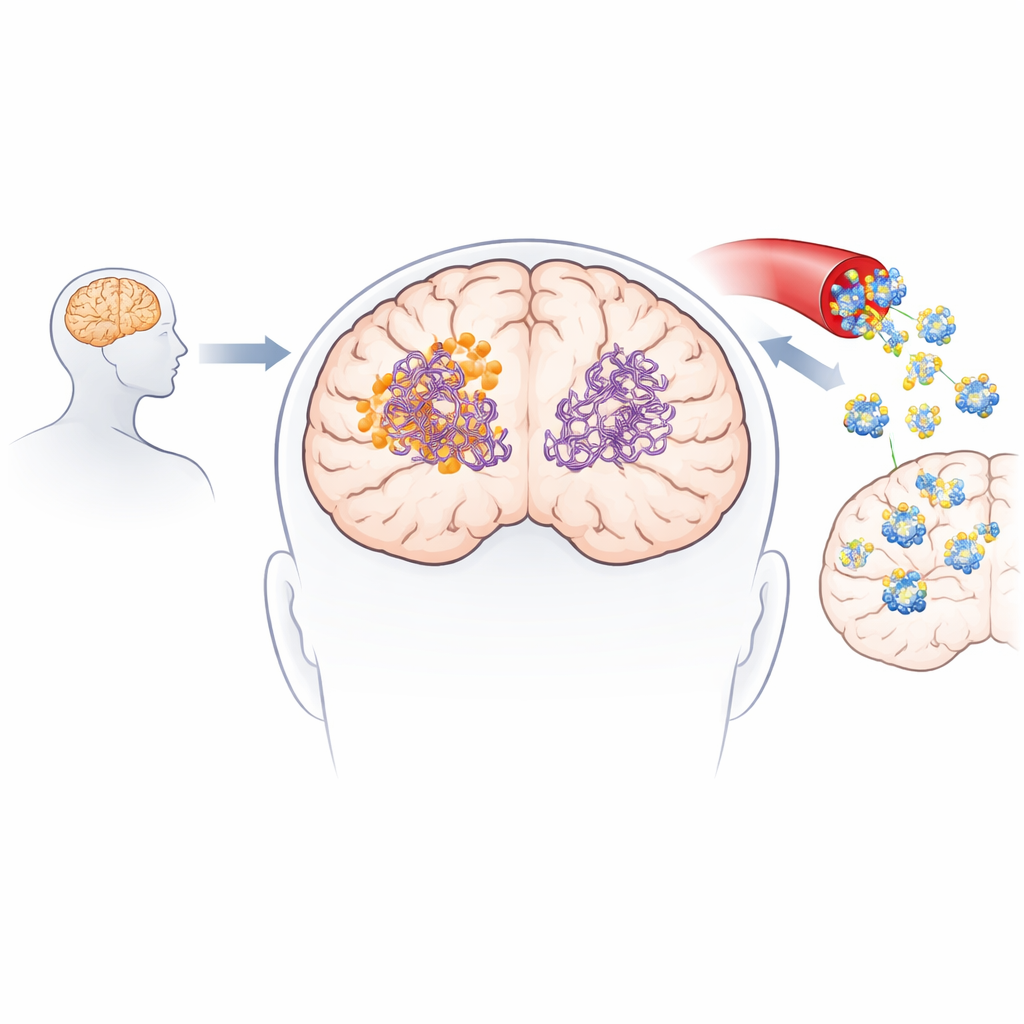
模拟揭示它如何抓握有毒纤维
为了理解新分子可能如何与致病蛋白相互作用,团队借助人工智能和分子模拟。他们使用最先进的对接模型探索该化合物与预先形成的淀粉样β和 tau 纤维结合的数千种方式。计算结果一致显示,3-脱氧科林诺酮 B 比科林内酯与两类纤维结合更紧密,它填入疏水(憎水)口袋并形成稳定的接触,如氢键和盐桥。随后分子动力学模拟追踪了纤维随时间的变化,显示一旦结合,该化合物会增加局部柔性并削弱蛋白链之间的关键接触,推动纤维朝结构崩解的方向发展。
从试管到小鼠大脑
实验室实验证实,3-脱氧科林诺酮 B 不仅能减缓新生淀粉样β和 tau 纤维的形成,还能主动破坏已有的纤维和较小的、高度毒性的寡聚体。在无细胞试验中,它显著减少了淀粉样β 纤维和寡聚体,并对与缠结形成相关的 tau 片段表现出更强的作用。该分子能穿透人工及生物学模型的血–脑屏障,并在静脉注射和口服给药后在小鼠脑内被检测到。在两种不同的类阿尔茨海默小鼠模型中,短期和较长期的治疗降低了淀粉样斑块和可溶性淀粉样物质的水平,减少了脑炎性标志物,部分恢复了突触蛋白,并在 Y 迷宫和新奇物体识别等记忆与学习任务中改善了行为表现。 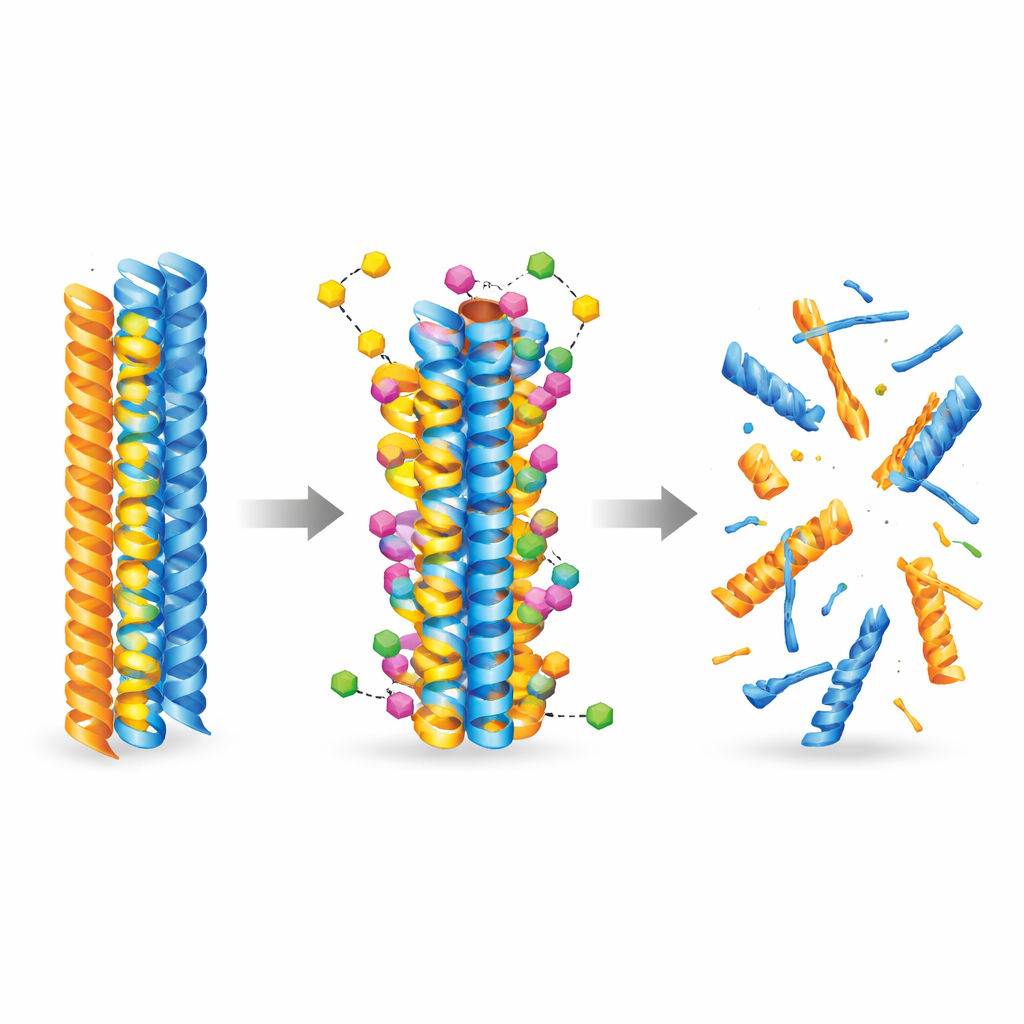
前景与下一步
总体而言,该研究表明3-脱氧科林诺酮 B 是一种双重作用的小分子,能够进入大脑、强烈结合淀粉样β 和 tau 聚集体并促进其解体,从而在小鼠中带来可测的认知益处。对非专业读者来说,这意味着该化合物有点像对两类关键阿尔茨海默相关蛋白团块起作用的分子“溶剂”,而不是仅仅掩盖症状。尽管该分子在体内清除相对较快,需要进一步修饰以延长血液中的滞留时间,但其可放大合成、脑穿透性以及对错误折叠蛋白的广谱活性,使其成为开发更易获得且更具成本效益的、从根本上应对阿尔茨海默病治疗的有希望的起点。
引用: Heo, S., Cha, M., Zhung, W. et al. Synthesis of 3-desoxycollinoketone B and its ability to reduce Alzheimer-associated misfolded proteins. Nat Commun 17, 3288 (2026). https://doi.org/10.1038/s41467-026-69662-z
关键词: 阿尔茨海默病, 淀粉样β蛋白, tau 蛋白, 小分子疗法, 蛋白质聚集体