Clear Sky Science · pl
Synteza 3-desoksycollinoketonu B i jego zdolność do redukcji zlepów białek związanych z chorobą Alzheimera
Nowe spojrzenie na Alzheimera
Choroba Alzheimera jest częściowo napędzana przez skupiska nieprawidłowo sfałdowanych białek, które stopniowo uszkadzają mózg, jednak dzisiejsze terapie niewiele robią, by usunąć te szkodliwe depozyty. W tym badaniu przedstawiono laboratoryjnego kuzyna rzadkiego związku naturalnego, który może skuteczniej docierać do mózgu i bezpośrednio atakować jednocześnie dwa główne problematyczne białka. Łącząc zaawansowaną chemię, sztuczną inteligencję i badania na zwierzętach, badacze pokazują, jak ta mała cząsteczka rozkłada toksyczne agregaty białkowe i poprawia pamięć u modeli mysich choroby Alzheimera.
Naturalna cząsteczka z ograniczeniami
Naukowcy wcześniej odkryli bakteryjny produkt naturalny zwany collinolactone, który potrafi rozmontowywać skupiska białek tworzone przez amyloid-beta i tau — dwa charakterystyczne białka choroby Alzheimera. Jednak collinolactone jest trudny do pozyskania w użytecznych ilościach z jego źródła mikrobiologicznego i ma słaby dostęp do niektórych obszarów mózgu, zwłaszcza kory, gdzie występuje duża część uszkodzeń w Alzheimerze. Te wady utrudniają jego rozwój jako praktycznego leku. Zespół postanowił zaprojektować i zsyntezować pokrewną cząsteczkę, która zachowa korzystne działanie collinolactone, jednocześnie poprawiając jej stabilność i zdolność przenikania do mózgu.
Budowanie „mądrzejszej” cząsteczki
Wykorzystując nowoczesną syntezę organiczną, badacze skonstruowali nowy związek nazwany 3-desoksycollinoketonem B. Złożyli go z trzech prostszych bloków chemicznych, a następnie wywołali rzadką reakcję tworzenia pierścienia, która imituje krok przypuszczalnie zachodzący w naturze. Szczegółowe obliczenia komputerowe wyjaśniły, dlaczego ta reakcja faworyzuje specyficzny trójpierścieniowy kształt, bardziej stabilny niż alternatywne struktury. Powstała cząsteczka jest nieco bardziej lipofilna niż oryginalny produkt naturalny, co powinno ułatwić jej przenikanie przez barierę krew–mózg. Co istotne, ścieżka syntezy jest skalowalna, co oznacza, że można niezawodnie wytwarzać gramowe ilości w laboratorium do szeroko zakrojonych testów biologicznych i przyszłej optymalizacji. 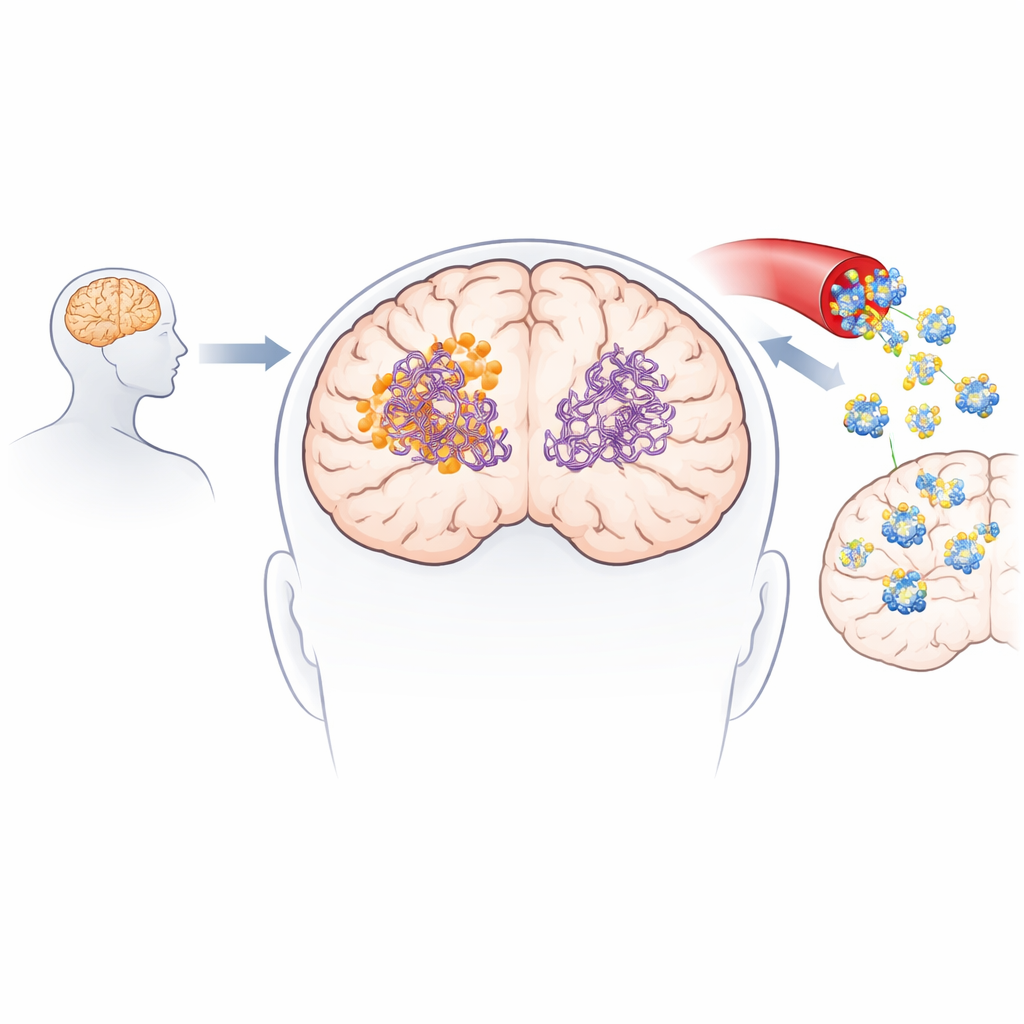
Symulacje ujawniają, jak chwyta toksyczne włókna
Aby zrozumieć, jak nowa cząsteczka może oddziaływać z białkami powodującymi chorobę, zespół sięgnął po sztuczną inteligencję i symulacje molekularne. Użyli najnowocześniejszych modeli dokowania, aby zbadać tysiące sposobów, w jakie związek może przyłączać się do już uformowanych włókien amyloid-beta i tau. Obliczenia konsekwentnie pokazały, że 3-desoksycollinoketon B wiąże się silniej z oboma typami włókien niż collinolactone, wciskając się w hydrofobowe (odpychające wodę) kieszenie i tworząc stabilizujące kontakty, takie jak wiązania wodorowe i mostki solne. Symulacje dynamiki molekularnej śledziły następnie włókna w czasie i wykazały, że po związaniu związek zwiększa lokalną elastyczność i osłabia krytyczne kontakty między niciami białkowymi, skłaniając włókna ku rozpadowi strukturalnemu.
Od probówek do mózgów myszy
Eksperymenty laboratoryjne potwierdziły, że 3-desoksycollinoketon B nie tylko spowalnia tworzenie nowych włókien amyloid-beta i tau, ale także aktywnie rozrywa istniejące włókna oraz mniejsze, wysoce toksyczne oligomery. W testach bezkomórkowych zmniejszał ilość włókien i oligomerów amyloid-beta w znacznym stopniu, a jego efekty na fragmenty tau kluczowe dla tworzenia się splątków były jeszcze silniejsze. Cząsteczka przenikała przez sztuczne i biologiczne modele bariery krew–mózg i była wykrywalna w mózgach myszy po podaniu dożylnym i doustnym. W dwóch różnych modelach mysich przypominających Alzheimera krótkotrwałe i dłuższe leczenie obniżało poziomy blaszek amyloidowych i rozpuszczalnych form amyloidu, zmniejszało markery zapalenia mózgu, częściowo przywracało białka synaptyczne oraz poprawiało wyniki w zadaniach pamięci i uczenia się, takich jak labirynt typu Y i rozpoznawanie nowego obiektu. 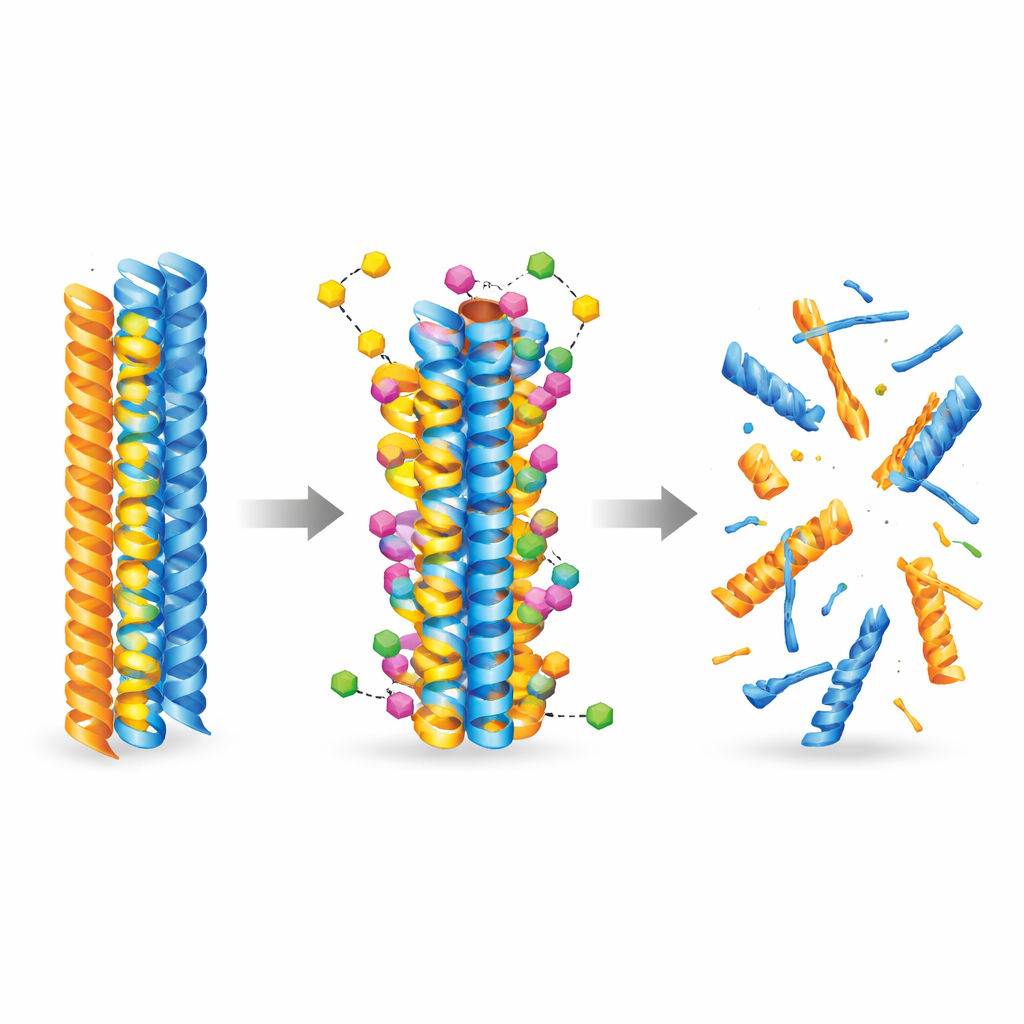
Obietnica i kolejne kroki
Podsumowując, badanie pokazuje, że 3-desoksycollinoketon B jest dwukierunkowo działającą małą cząsteczką, która może wejść do mózgu, silnie wiązać się zarówno z agregatami amyloid-beta, jak i tau, oraz sprzyjać ich rozpadowi, co prowadzi do mierzalnych korzyści poznawczych u myszy. Dla laika oznacza to, że związek działa trochę jak molekularny rozpuszczalnik dla dwóch kluczowych typów zlepów białkowych związanych z Alzheimerem, zamiast jedynie maskować objawy. Chociaż cząsteczka jest relatywnie szybko usuwana z organizmu i wymaga dalszych modyfikacji, by dłużej utrzymywać się we krwi, jej skalowalna synteza, przenikanie do mózgu i szerokie działanie przeciwko nieprawidłowo sfałdowanym białkom czynią ją obiecującym punktem wyjścia do opracowania bardziej dostępnych i opłacalnych terapii atakujących chorobę Alzheimera u jej źródła.
Cytowanie: Heo, S., Cha, M., Zhung, W. et al. Synthesis of 3-desoxycollinoketone B and its ability to reduce Alzheimer-associated misfolded proteins. Nat Commun 17, 3288 (2026). https://doi.org/10.1038/s41467-026-69662-z
Słowa kluczowe: choroba Alzheimera, amyloid-beta, białko tau, terapia małocząsteczkowa, agregaty białkowe