Clear Sky Science · nl
Synthese van 3-desoxycollinoketone B en het vermogen ervan om aan Alzheimer gerelateerde verkeerd gevouwen eiwitten te verminderen
Een nieuwe invalshoek op Alzheimer
De ziekte van Alzheimer wordt deels aangedreven door hopen verkeerd gevouwen eiwitten die de hersenen geleidelijk beschadigen, maar de huidige behandelingen doen weinig om deze schadelijke afzettingen te verwijderen. Deze studie introduceert een in het laboratorium gemaakte neef van een zeldzaam natuurlijk verbinding die de hersenen effectiever kan bereiken en twee belangrijke probleem-eiwitten tegelijk rechtstreeks kan aanvallen. Door geavanceerde chemie, kunstmatige intelligentie en dierstudies te combineren, laten de onderzoekers zien hoe dit klein molecuul toxische eiwitaggregaten afbreekt en het geheugen verbetert in muismodellen van Alzheimer.
Een natuurlijk molecuul met beperkingen
Onderzoekers ontdekten eerder een bacterieel natuurlijk product genaamd collinolacton dat eiwitklonters gevormd door amyloïde-beta en tau—twee kenmerkende eiwitten van de ziekte van Alzheimer—kan afbreken. Collinolacton is echter moeilijk in bruikbare hoeveelheden uit zijn microbiele bron te isoleren en heeft beperkte toegang tot bepaalde hersengebieden, met name de cortex, waar veel van de schade bij Alzheimer optreedt. Deze nadelen bemoeilijken de ontwikkeling tot een praktisch geneesmiddel. Het team stelde zich daarom ten doel een verwant molecuul te ontwerpen en te synthetiseren dat de gunstige activiteit van collinolacton behoudt terwijl het stabiliteit en de capaciteit om de hersenen binnen te dringen verbetert.
Het bouwen van een slimmer molecuul
Met moderne organische synthese bouwden de onderzoekers een nieuwe verbinding genaamd 3-desoxycollinoketone B. Ze zetten drie eenvoudigere chemische bouwstenen in elkaar en veroorzaakten vervolgens een zeldzame ringvormende reactie die een stap nabootst waarvan men denkt dat die in de natuur plaatsvindt. Gedetailleerde computercalculaties legden uit waarom deze reactie een specifieke driedubbele ringvorm bevoordeelt die stabieler is dan alternatieve structuren. Het resulterende molecuul is iets lipofieler dan het oorspronkelijke natuurlijke product, een eigenschap waarvan verwacht wordt dat die helpt bij het passeren van de bloed-hersenbarrière. Belangrijk is dat de synthetische route schaalbaar is, wat betekent dat gramhoeveelheden betrouwbaar in het lab kunnen worden geproduceerd voor uitgebreide biologische tests en toekomstige optimalisatie. 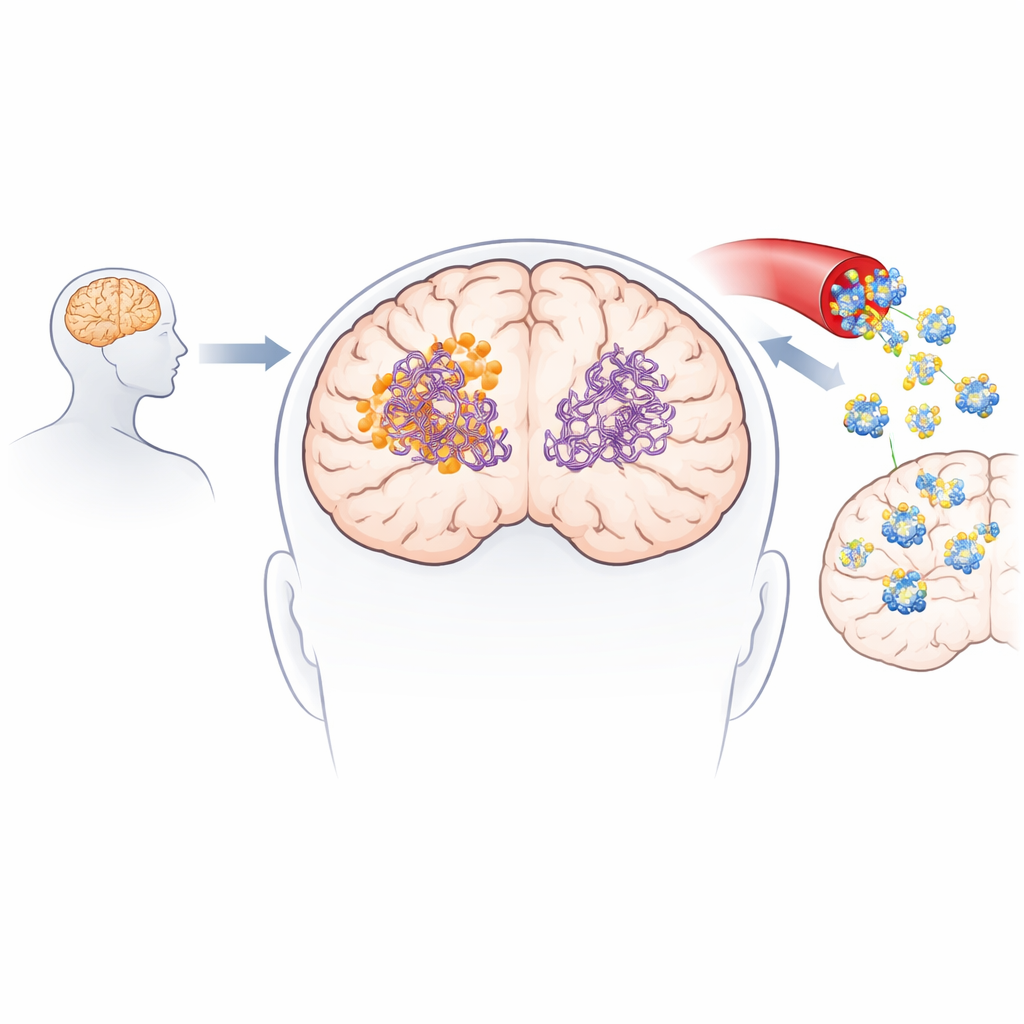
Simulaties onthullen hoe het toxische vezels omklemt
Om te begrijpen hoe het nieuwe molecuul mogelijk met ziekmakende eiwitten interageert, gebruikte het team kunstmatige intelligentie en moleculaire simulaties. Ze pasten geavanceerde dockingmodellen toe om duizenden manieren te verkennen waarop het verbinding zich aan vooraf gevormde amyloïde-beta- en tau-vezels zou kunnen hechten. De berekeningen toonden consequent aan dat 3-desoxycollinoketone B sterker bindt aan beide types vezels dan collinolacton, door zich in hydrofobe (waterafstotende) pockets te nestelen en stabiliserende contacten te vormen zoals waterstofbruggen en zoutbruggen. Moleculaire dynamica-simulaties volgden vervolgens de vezels in de tijd en lieten zien dat, eenmaal gebonden, het verbinding de lokale flexibiliteit verhoogt en kritieke contacten tussen eiwitstrengen verzwakt, waardoor de vezels richting structurele afbraak worden geduwd.
Van reageerbuis naar muizenhersenen
Laboratoriumexperimenten bevestigden dat 3-desoxycollinoketone B niet alleen de vorming van nieuwe amyloïde-beta- en tau-vezels vertraagt, maar ook actief bestaande vezels en kleinere, sterk toxische oligomeren uiteenrijt. In celvrije assays verminderde het amyloïde-beta-vezels en oligomeren in significante mate, en toonde het nog sterkere effecten op tau-fragmenten die centraal staan in de vorming van neurofibrillaire knopen. Het molecuul passeerde kunstmatige en biologische modellen van de bloed-hersenbarrière en was detecteerbaar in de hersenen van muizen na zowel intraveneuze als orale toediening. In twee verschillende Alzheimerachtige muismodellen verlaagde korte- en langere termijnbehandeling niveaus van amyloïdeplaques en oplosbare amyloïde-species, verminderde markers van hersenontsteking, herstelde deels synaptische eiwitten en verbeterde de prestaties bij geheugen- en leertaken zoals Y-maze en herkenning van nieuwe objecten. 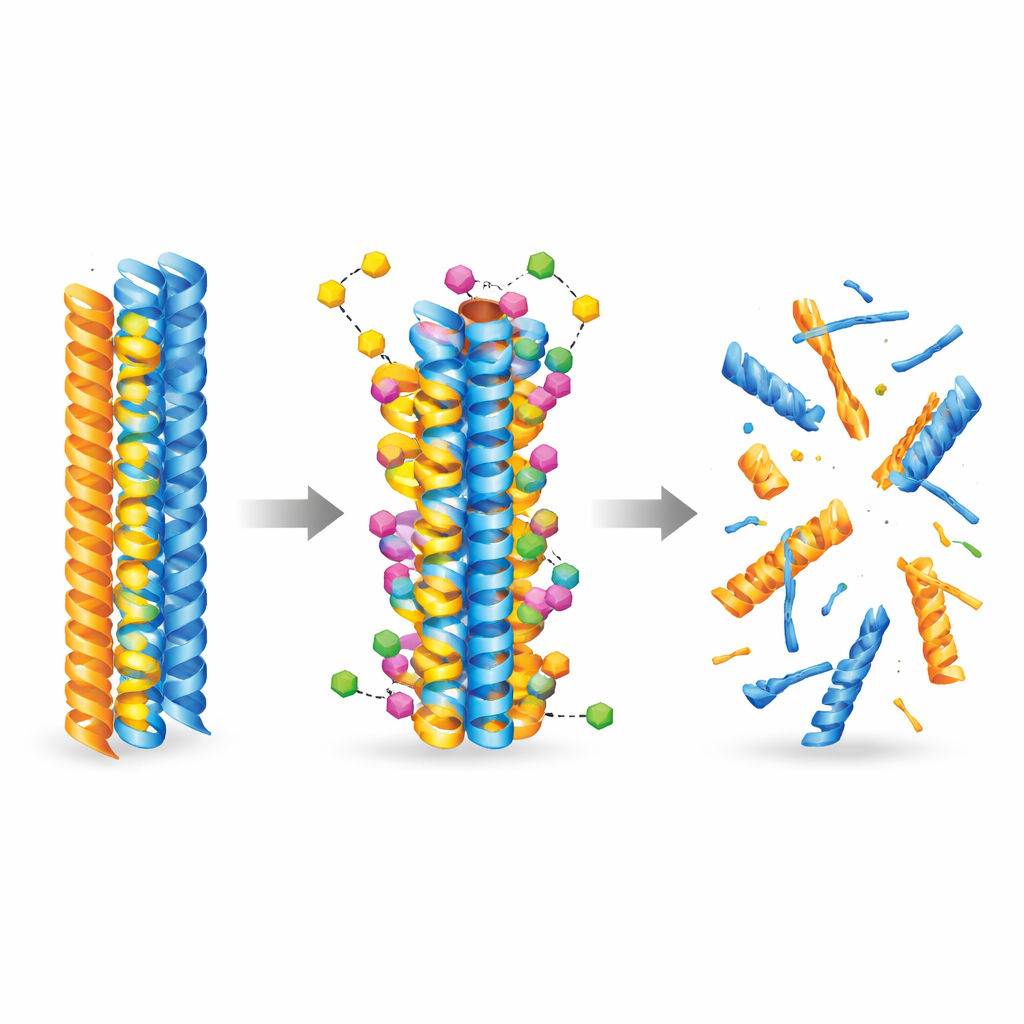
Belofte en volgende stappen
Alles bij elkaar laat de studie zien dat 3-desoxycollinoketone B een dubbelwerkend klein molecuul is dat de hersenen kan binnendringen, sterk bindt aan zowel amyloïde-beta- als tau-aggregaten en hun afbraak bevordert, wat leidt tot meetbare cognitieve voordelen bij muizen. Voor een leek betekent dit dat de verbinding enigszins werkt als een moleculaire oplosmiddel voor twee sleuteltypen eiwitklonters die met Alzheimer geassocieerd zijn, in plaats van slechts symptomen te maskeren. Hoewel het molecuul relatief snel uit het lichaam wordt verwijderd en verder aangepast moet worden om langer in de bloedbaan te blijven, maken de schaalbare synthese, hersenpenetratie en brede activiteit tegen verkeerd gevouwen eiwitten het tot een veelbelovende vertrekpunt voor de ontwikkeling van toegankelijkere en kosteneffectievere behandelingen die Alzheimer bij de kern aanpakken.
Bronvermelding: Heo, S., Cha, M., Zhung, W. et al. Synthesis of 3-desoxycollinoketone B and its ability to reduce Alzheimer-associated misfolded proteins. Nat Commun 17, 3288 (2026). https://doi.org/10.1038/s41467-026-69662-z
Trefwoorden: Ziekte van Alzheimer, amyloïde-beta, tau-eiwit, klein-molecuultherapie, proteïne-aggregaten