Clear Sky Science · ru
Синтез 3-дезоксиколлинокетона B и его способность уменьшать белки с неверной укладкой, связанные с болезнью Альцгеймера
Новый подход к Альцгеймеру
Болезнь Альцгеймера отчасти вызывается скоплениями неправильно свернутых белков, которые постепенно повреждают мозг, тогда как современные лечения мало что делают для удаления этих вредных отложений. В этом исследовании представлен синтетический родственник редкого природного соединения, который лучше проникает в мозг и напрямую атакует одновременно две ключевые проблемные белковые мишени. Объединив современные методы синтеза, искусственный интеллект и животные модели, авторы показывают, как эта малая молекула разрушает токсичные белковые агрегаты и улучшает память у мышей с моделями болезни Альцгеймера.
Природная молекула с ограничениями
Ранее учёные обнаружили бактериальный природный продукт коллинолактон, способный разрушать белковые скопления, образуемые амилоид-бета и тау — двумя характерными белками при болезни Альцгеймера. Однако коллинолактон трудно выделять из микробного источника в полезных количествах, и он плохо попадает в некоторые области мозга, особенно в кору, где происходит значительная часть повреждений при Альцгеймере. Эти недостатки затрудняют его развитие как практического лекарства. Исследователи поставили задачу разработать и синтезировать родственную молекулу, сохраняющую полезную активность коллинолактона, но обладающую большей стабильностью и лучшей способностью проникать в мозг.
Создание более умной молекулы
С помощью современных методов органического синтеза исследователи получили новое соединение под названием 3-дезоксиколлинокетон B. Они собрали три более простых химических блока и затем инициировали редкую реакцию формирования кольца, имитирующую шаг, который, как считают, происходит в природе. Подробные вычисления объяснили, почему эта реакция даёт преимущество определённой трёхкольцевой форме, более стабильной по сравнению с альтернативными структурами. Получившаяся молекула стала слегка более липофильной по сравнению с природным продуктом, что, как ожидается, поможет ей проникать через гематоэнцефалический барьер. Важно, что синтетический путь масштабируем — это значит, что граммовые количества можно надёжно получать в лаборатории для обширных биологических испытаний и дальнейшей оптимизации. 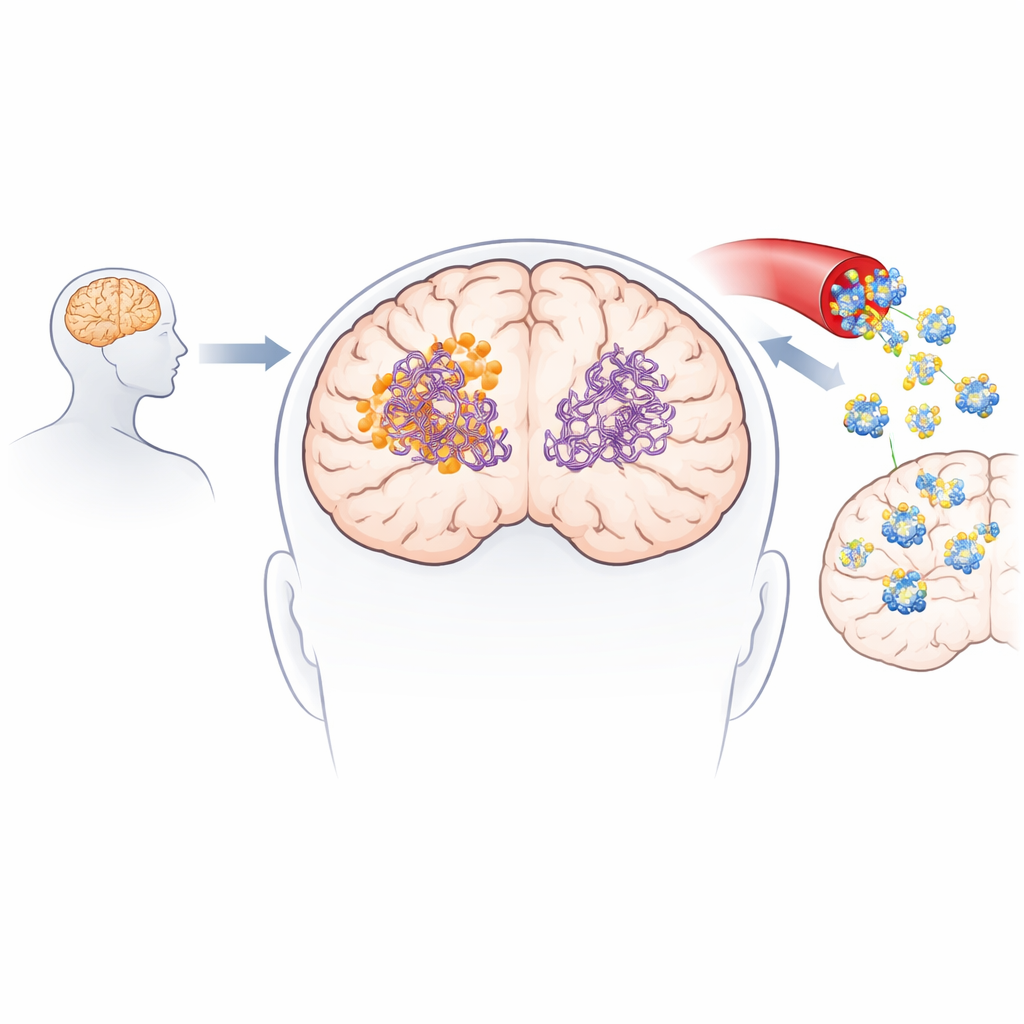
Симуляции показывают, как она захватывает токсичные фибриллы
Чтобы понять, как новая молекула может взаимодействовать с вызывающими заболевание белками, команда привлекла искусственный интеллект и молекулярные симуляции. Они использовали передовые модели докинга, чтобы исследовать тысячи способов, которыми соединение могло бы прикрепляться к уже сформированным фибриллам амилоид-бета и тау. Расчёты последовательно показали, что 3-дезоксиколлинокетон B связывается прочнее с обоими типами фибрилл, чем коллинолактон, западая в гидрофобные (отталкивающие воду) карманы и образуя стабилизирующие контакты, такие как водородные связи и сольвные мосты. Молекулярно-динамические симуляции затем отслеживали фибриллы во времени и показали, что после связывания соединение увеличивает локальную гибкость и ослабляет ключевые контакты между белковыми цепями, подталкивая фибриллы к структурному распаду.
От пробирок до мозга мыши
Лабораторные эксперименты подтвердили, что 3-дезоксиколлинокетон B не только замедляет образование новых фибрилл амилоид-бета и тау, но и активно расщепляет уже существующие фибриллы и более мелкие, высокотоксичные олигомеры. В бесклеточных тестах он существенно сокращал количество фибрилл и олигомеров амилоид-бета и демонстрировал ещё более выраженные эффекты на фрагменты тау, центральные для образования нейрофибриллярных клубков. Молекула проникала через искусственные и биологические модели гематоэнцефалического барьера и обнаруживалась в мозгах мышей как после внутривенного, так и после перорального введения. В двух различных моделях, имитирующих болезнь Альцгеймера, краткосрочное и более длительное лечение снижало уровни амилоидных бляшек и растворимых форм амилоида, уменьшало маркёры воспаления мозга, частично восстанавливало синаптические белки и улучшало показатели памяти и обучения в тестах, таких как Y-лабиринт и распознавание нового объекта. 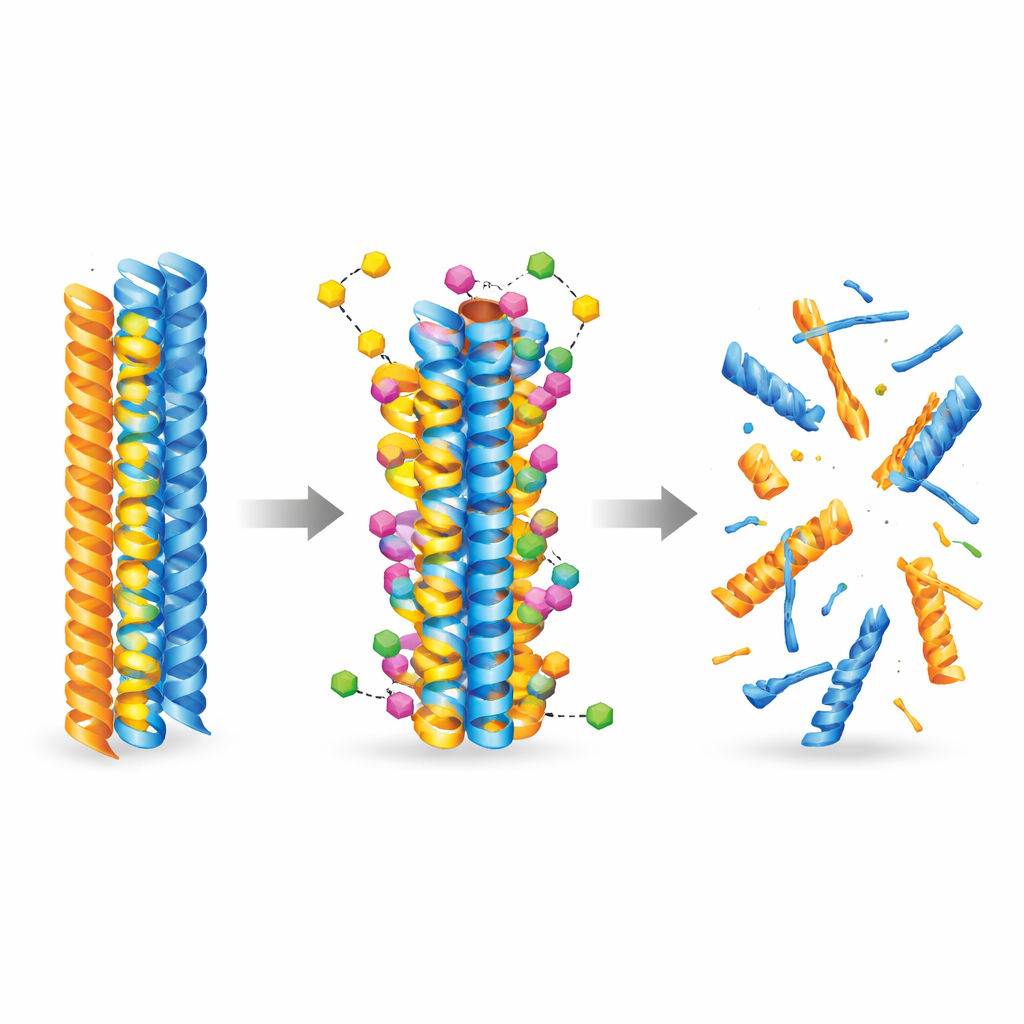
Перспективы и следующие шаги
В целом исследование демонстрирует, что 3-дезоксиколлинокетон B — это двухцелевое маломолекулярное средство, способное проникать в мозг, прочно связываться как с агрегатами амилоид-бета, так и тау и способствовать их разрушению, что приводит к измеримым когнитивным улучшениям у мышей. Для неспециалиста это означает, что соединение действует подобно молекулярному растворителю для двух ключевых типов белковых скоплений, связанных с Альцгеймером, а не просто маскирует симптомы. Хотя молекула относительно быстро выводится из организма и потребует доработки, чтобы дольше сохраняться в кровотоке, её масштабируемый синтез, проникновение в мозг и широкая активность против неправильно свернутых белков делают её перспективной отправной точкой для разработки более доступных и экономичных терапий, направленных на коренные причины болезни Альцгеймера.
Цитирование: Heo, S., Cha, M., Zhung, W. et al. Synthesis of 3-desoxycollinoketone B and its ability to reduce Alzheimer-associated misfolded proteins. Nat Commun 17, 3288 (2026). https://doi.org/10.1038/s41467-026-69662-z
Ключевые слова: Болезнь Альцгеймера, амилоид-бета, белок тау, терапия малыми молекулами, белковые агрегаты