Clear Sky Science · he
סינתזה של 3-דזוקסי־קולינוקטון B ויכולתו להפחית חלבונים מקופלים שקשורים לאלצהיימר
זוית חדשה על אלצהיימר
מחלת האלצהיימר מונעת במידה מסוימת על ידי צברים של חלבונים מקופלים בצורה חריגה שפוגעים בהדרגה במוח, אך הטיפולים הקיימים היום עושים מעט מאוד כדי להסיר את ההצטברויות המזיקות הללו. המחקר הזה מציג קרוב מעבדתי של תרכובת טבעית נדירה היכול להגיע למוח ביעילות רבה יותר ולתקוף ישירות שתי חלבונים בעייתיים מרכזיים בו זמנית. באמצעות שילוב של כימיה מתקדמת, בינה מלאכותית וניסויים בחיות, החוקרים מראים כיצד מולקולה קטנה זו מפוררת צברי חלבון רעילים ומשפרת זיכרון במודלים עכבריים של אלצהיימר.
מולקולה טבעית עם מגבלות
מדענים גילו בעבר מוצר טבעי חיידקי שנקרא קולינולקטון שיכול לפרק צברי חלבון שנוצרים על ידי עימילואיד-בטא וטאו — שני חלבונים מאפיינים של מחלת האלצהיימר. עם זאת, קולינולקטון קשה לחילוץ בכמויות שימושיות ממקורו המיקרוביאלי ויש לו חדירה לקויה לאזורים מסוימים במוח, במיוחד לקורטקס, שבו מרבית הנזק באלצהיימר מתרחש. חסרונות אלה מקשים על פיתוחו כתרופה מעשית. הצוות יצא לתכנן ולסנתז מולקולה קרובה ששומרת על הפעילות המועילה של קולינולקטון תוך שיפור היציבות ויכולת החדירה שלה למוח.
בניית מולקולה חכמה יותר
באמצעות סינתזה אורגנית מודרנית, החוקרים בנו תרכובת חדשה שנקראת 3-דזוקסי־קולינוקטון B. הם הרכיבו שלושה גושי בנייה כימיים פשוטים ואז יזמו תגובת סגירת טבעת נדירה שמדמה שלב שנחשב שמתרחש בטבע. חישובים ממוחשבים מפורטים הסבירו מדוע תגובה זו מעדיפה צורה תלת־טבעתית ספציפית שהיא יציבה יותר מאשר מבנים חלופיים. המולקולה המתקבלת הידרופובית במעט יותר מהמוצר הטבעי המקורי — תכונה שמצופה שתעזור לה לעבור את מחסום הדם־מוח. חשוב לציין כי המסלול הסינתטי ניתן להקנה בכמויות, כלומר ניתן לייצר reliably כמויות גרמיות במעבדה למבחני ביולוגיה נרחבים ואופטימיזציה עתידית. 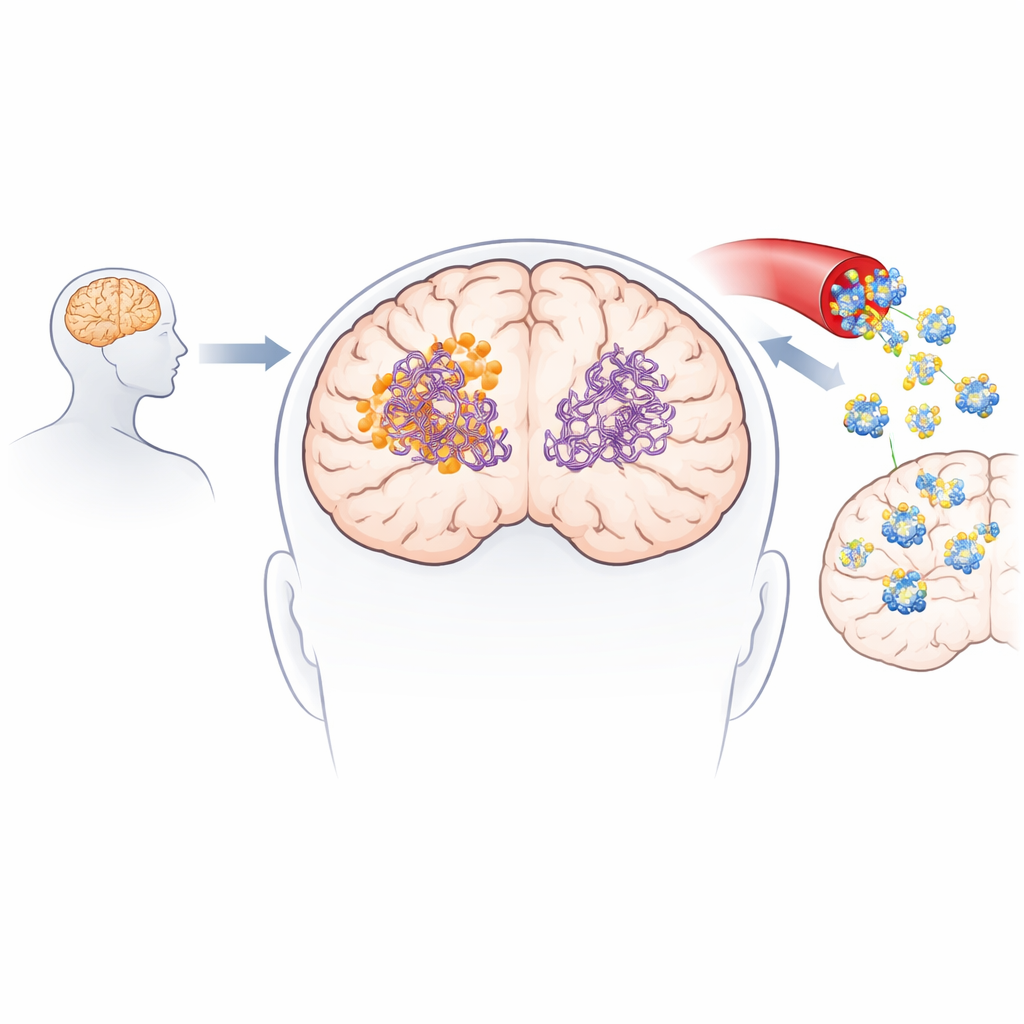
סימולציות חושפות כיצד היא נצמדת לסיבים רעילים
כדי להבין כיצד המולקולה החדשה עשויה לעבור אינטראקציה עם חלבונים גורמי מחלה, הצוות פנה לבינה מלאכותית ולסימולציות מולקולריות. הם השתמשו במודלים מתקדמים של דוקינג כדי לבחון אלפי דרכים שבהן התרכובת יכולה להיצמד לסיבי עמילואיד-בטא וטאו שכבר נוצרו. החישובים הראו בעקביות כי 3-דזוקסי־קולינוקטון B נקשרת בחוזק רב יותר לשני סוגי הסיבים מאשר קולינולקטון, נכנסת לכיסים הידרופוביים ויוצרת מגעים מייצבים כגון קשרי מימן וגשרים מלחיים. סימולציות דינמיקת מולקולות עקבו אחר הסיבים בזמן וגילו כי לאחר היקשרות, התרכובת מגדילה את הגמישות המקומית ומחלישה מגעים קריטיים בין הגדילים החלבוניים, וגורמת לדחיפה בכיוון של פירוק מבני.
מצד מבחנות אל מוחי עכבר
ניסויים במעבדה אישרו כי 3-דזוקסי־קולינוקטון B לא רק מאט את היווצרות סיבי עמילואיד-בטא וטאו חדשים, אלא גם מפרק באופן פעיל סיבים קיימים ואוליגומרים קטנים ורעילים במיוחד. בבדיקות ללא תאים, היא הקטינה באופן משמעותי סיבים ואוליגומרים של עמילואיד-בטא, והראתה אפקטים חזקים אף יותר על שברי טאו המרכזיים להיווצרות קשרים (tangles). המולקולה עברתה דגמי מחסום דם־מוח מלאכותיים וביולוגיים והייתה ניתנת לזיהוי במוחות עכברים לאחר מתן תוך־ורידי ובפעם orale. בשני דגמי עכבר דמויי אלצהיימר, טיפול קצר־טווח וארוך־טווח הוריד רמות של פלאקים עמילואידיים וסוגי עמילואיד מסיסים, הקטין סמנים של דלקת מוחית, השיב חלקית חלבוני סינפסה ושיפר ביצועים במבחני זיכרון ולמידה כגון מבוך בצורת Y וזיהוי עצם חדש. 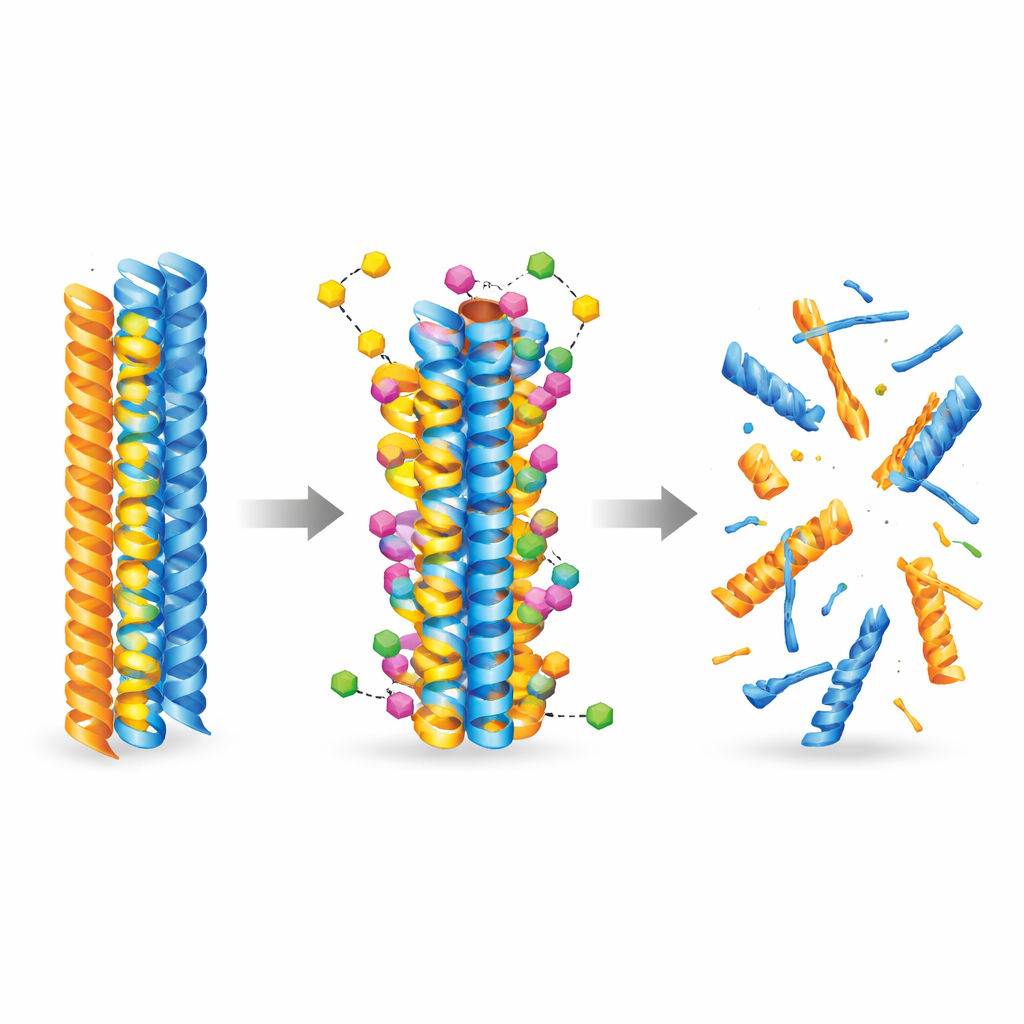
הבטחה ושלבים הבאים
בסך הכל, המחקר ממחיש כי 3-דזוקסי־קולינוקטון B היא מולקולה קטנה בעלת פעילות כפולה שיכולה להיכנס למוח, להיקשר בעוז לשני סוגי צברי עמילואיד-בטא וטאו, ולקדם את פירוקם, מה שמוביל לשיפורים קוגניטיביים מדידים בעכברים. עבור הקורא הרחב, המשמעות היא שהתרכובת פועלת קצת כמו ממס מולקולרי לשני סוגי הצברים הקשורים לאלצהיימר, במקום רק להסתיר תסמינים. בעוד שהמולקולה מופרשת יחסית במהירות מהגוף ותצטרך שיפורים על מנת להישאר לאורך זמן במחזור הדם, הסינתזה הניתנת להקנה שלה, החדירה למוח והפעילות הרחבה כנגד חלבונים מקופלים הופכים אותה לנקודת פתיחה מבטיחה לפיתוח טיפולים נגישים ויעילים יותר שיתקפו את שורש מחלת האלצהיימר.
ציטוט: Heo, S., Cha, M., Zhung, W. et al. Synthesis of 3-desoxycollinoketone B and its ability to reduce Alzheimer-associated misfolded proteins. Nat Commun 17, 3288 (2026). https://doi.org/10.1038/s41467-026-69662-z
מילות מפתח: מחלת האלצהיימר, עמילואיד-בטא, חלבון טאו, טיפול במולקולות קטנות, צברי חלבון