Clear Sky Science · es
Síntesis de 3-desoxicollinocetona B y su capacidad para reducir proteínas mal plegadas asociadas con el Alzheimer
Un nuevo enfoque sobre el Alzheimer
La enfermedad de Alzheimer está impulsada en parte por agrupaciones de proteínas mal plegadas que dañan el cerebro de forma progresiva, pero los tratamientos actuales hacen poco para eliminar estos depósitos nocivos. Este estudio presenta un análogo sintético de un compuesto natural raro que puede alcanzar el cerebro de forma más eficaz y atacar directamente dos proteínas problemáticas a la vez. Combinando química avanzada, inteligencia artificial y estudios en animales, los investigadores muestran cómo esta pequeña molécula descompone agregados proteicos tóxicos y mejora la memoria en modelos de ratón del Alzheimer.
Una molécula natural con limitaciones
Investigadores habían descubierto anteriormente un producto natural bacteriano llamado collinolactona que puede desmantelar los cúmulos proteicos formados por amiloide beta y tau—dos proteínas emblemáticas de la enfermedad de Alzheimer. Sin embargo, la collinolactona es difícil de extraer en cantidades útiles de su fuente microbiana y tiene un acceso limitado a ciertas regiones del cerebro, especialmente la corteza, donde ocurre gran parte del daño en el Alzheimer. Estas desventajas dificultan su desarrollo como fármaco práctico. El equipo se propuso diseñar y sintetizar una molécula relacionada que conservara la actividad beneficiosa de la collinolactona mejorando su estabilidad y su capacidad para atravesar al cerebro.
Construyendo una molécula más inteligente
Empleando síntesis orgánica moderna, los investigadores construyeron un nuevo compuesto llamado 3-desoxicollinocetona B. Montaron tres bloques químicos más simples y luego desencadenaron una rara reacción formadora de anillos que imita un paso que se cree ocurre en la naturaleza. Cálculos computacionales detallados explicaron por qué esta reacción favorece una forma de tres anillos específica que es más estable que otras estructuras alternativas. La molécula resultante es ligeramente más lipofílica que el producto natural original, una propiedad que se espera le ayude a atravesar la barrera hematoencefálica. De forma importante, la vía sintética es escalable, lo que significa que se pueden producir cantidades a nivel de gramos de manera fiable en el laboratorio para pruebas biológicas extensas y futura optimización. 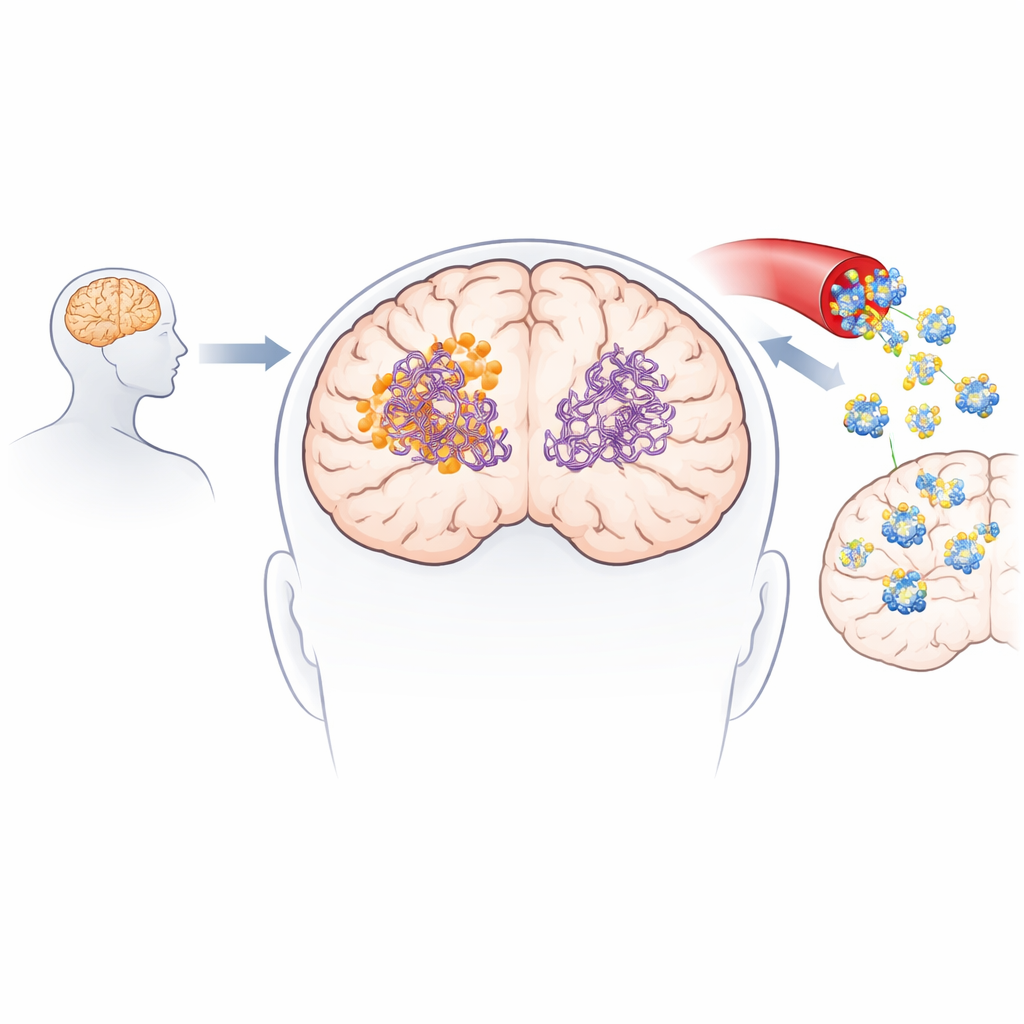
Simulaciones que revelan cómo se agarra a las fibras tóxicas
Para comprender cómo podría interactuar la nueva molécula con las proteínas causantes de la enfermedad, el equipo recurrió a la inteligencia artificial y a simulaciones moleculares. Usaron modelos de acoplamiento de última generación para explorar miles de formas en que el compuesto podría unirse a fibras preformadas de amiloide beta y tau. Los cálculos mostraron de forma consistente que la 3-desoxicollinocetona B se une con más fuerza a ambos tipos de fibras que la collinolactona, acomodándose en bolsillos hidrofóbicos (repelentes al agua) y formando contactos estabilizadores como enlaces de hidrógeno y puentes salinos. Simulaciones de dinámica molecular siguieron luego la evolución temporal de las fibras y revelaron que, una vez unida, la molécula aumenta la flexibilidad local y debilita contactos críticos entre las hebras proteicas, empujando a las fibras hacia la desintegración estructural.
De los tubos de ensayo al cerebro de los ratones
Experimentos de laboratorio confirmaron que la 3-desoxicollinocetona B no solo ralentiza la formación de nuevas fibras de amiloide beta y tau, sino que también fragmenta activamente fibras existentes y oligómeros pequeños y altamente tóxicos. En ensayos sin células, redujo fibras y oligómeros de amiloide beta en cantidades significativas, y mostró efectos aún más pronunciados sobre fragmentos de tau centrales en la formación de ovillos. La molécula atravesó modelos artificiales y biológicos de la barrera hematoencefálica y fue detectable en los cerebros de ratones tras dosis tanto intravenosas como orales. En dos modelos de ratón con rasgos similares al Alzheimer, tratamientos a corto y largo plazo disminuyeron los niveles de placas amiloides y de especies amiloides solubles, redujeron marcadores de inflamación cerebral, restauraron parcialmente proteínas sinápticas y mejoraron el rendimiento en pruebas de memoria y aprendizaje como el laberinto en Y y el reconocimiento de objetos nuevos. 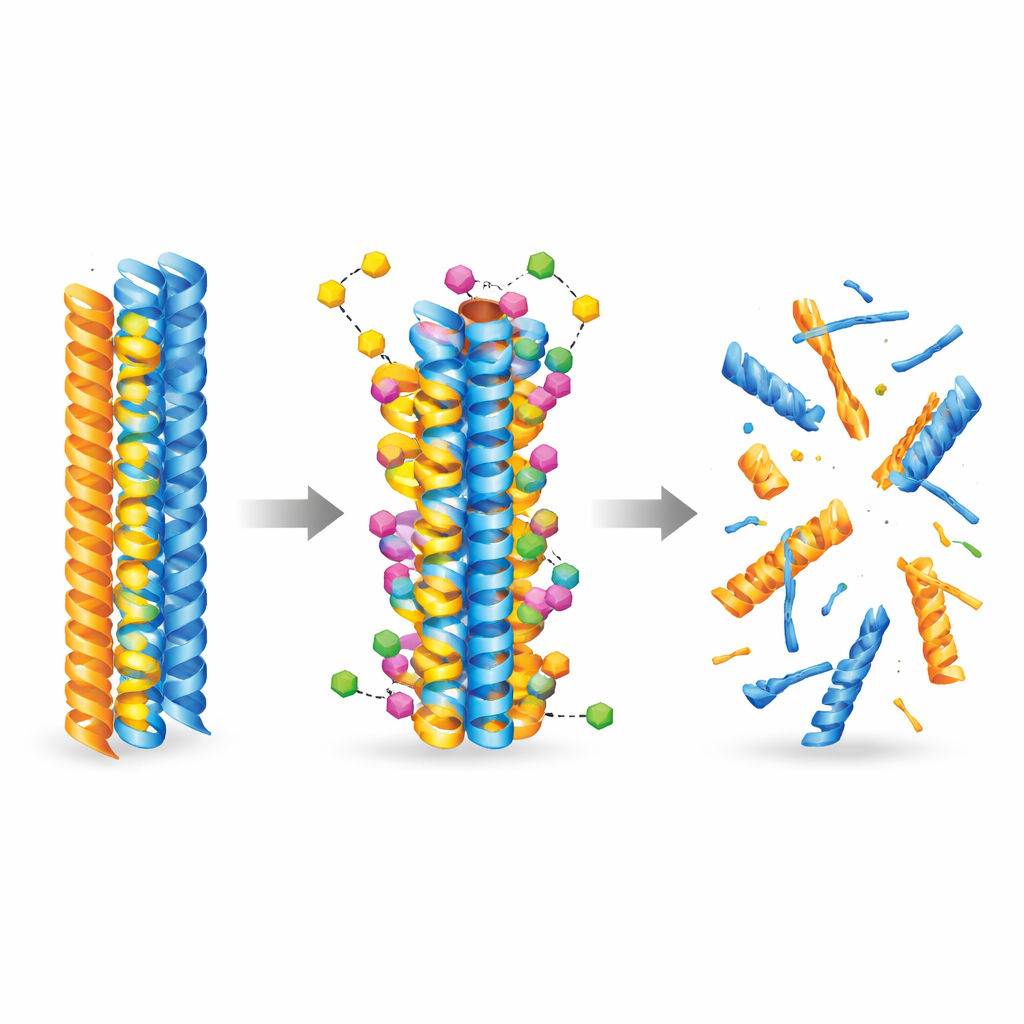
Promesa y próximos pasos
En conjunto, el estudio demuestra que la 3-desoxicollinocetona B es una pequeña molécula de acción dual que puede entrar en el cerebro, unirse fuertemente tanto a agregados de amiloide beta como de tau, y promover su descomposición, conduciendo a beneficios cognitivos medibles en ratones. Para un público no especializado, esto significa que el compuesto actúa un poco como un disolvente molecular para dos tipos clave de cúmulos proteicos relacionados con el Alzheimer, en lugar de limitarse a enmascarar los síntomas. Aunque la molécula se elimina relativamente rápido del organismo y requerirá ajustes adicionales para permanecer más tiempo en el torrente sanguíneo, su síntesis escalable, penetración cerebral y amplia actividad contra proteínas mal plegadas la convierten en un punto de partida prometedor para desarrollar tratamientos más accesibles y rentables que aborden el Alzheimer en su raíz.
Cita: Heo, S., Cha, M., Zhung, W. et al. Synthesis of 3-desoxycollinoketone B and its ability to reduce Alzheimer-associated misfolded proteins. Nat Commun 17, 3288 (2026). https://doi.org/10.1038/s41467-026-69662-z
Palabras clave: Enfermedad de Alzheimer, amiloide beta, proteína tau, terapia con pequeñas moléculas, agregados proteicos