Clear Sky Science · de
Synthese von 3-Desoxycollinoketon B und seine Fähigkeit, Alzheimer-assoziierte fehlgefaltete Proteine zu reduzieren
Ein neuer Blickwinkel auf Alzheimer
Die Alzheimer-Krankheit wird teilweise durch Aggregate fehlgefalteter Proteine vorangetrieben, die das Gehirn langsam schädigen. Die heutigen Therapien entfernen diese schädlichen Ablagerungen jedoch nur unzureichend. Diese Studie stellt einen im Labor hergestellten Verwandten einer seltenen Naturverbindung vor, der das Gehirn besser erreicht und gleichzeitig zwei wichtige Problemproteine direkt angreift. Durch die Kombination fortgeschrittener Chemie, künstlicher Intelligenz und Tierversuchen zeigen die Forschenden, wie dieses Kleinmolekül toxische Proteinaggregate auflöst und das Gedächtnis in Mausmodellen der Alzheimer-Krankheit verbessert.
Ein natürliches Molekül mit Einschränkungen
Wissenschaftler entdeckten zuvor ein bakterielles Naturprodukt namens Collinolacton, das Proteinaggregate aus Amyloid-beta und Tau – zwei Kennproteine der Alzheimer-Krankheit – auflösen kann. Collinolacton lässt sich jedoch nur schwer in nützlichen Mengen aus seinem mikrobiellen Ursprung gewinnen und gelangt schlecht in bestimmte Hirnregionen, insbesondere in den Kortex, wo ein Großteil der Alzheimer-Schädigung stattfindet. Diese Nachteile erschweren die Entwicklung zu einem praktikablen Medikament. Das Team machte sich daher daran, ein verwandtes Molekül zu entwerfen und zu synthetisieren, das die vorteilhafte Aktivität von Collinolacton beibehält, aber Stabilität und Gehirngängigkeit verbessert.
Ein intelligenteres Molekül aufbauen
Mithilfe moderner organischer Synthese konstruierten die Forschenden eine neue Verbindung namens 3-Desoxycollinoketon B. Sie setzten drei einfachere chemische Bausteine zusammen und lösten dann eine seltene ringbildende Reaktion aus, die einen Schritt imitiert, von dem man annimmt, dass er in der Natur abläuft. Detaillierte Rechnungen erklärten, warum diese Reaktion eine bestimmte drei-ringige Form begünstigt, die stabiler ist als alternative Strukturen. Das resultierende Molekül ist etwas lipophiler als das ursprüngliche Naturprodukt, eine Eigenschaft, die voraussichtlich hilft, die Blut–Hirn-Schranke zu passieren. Wichtig ist, dass die synthetische Route skalierbar ist, sodass Gramm-Mengen zuverlässig im Labor hergestellt werden können für umfangreiche biologische Tests und zukünftige Optimierungen. 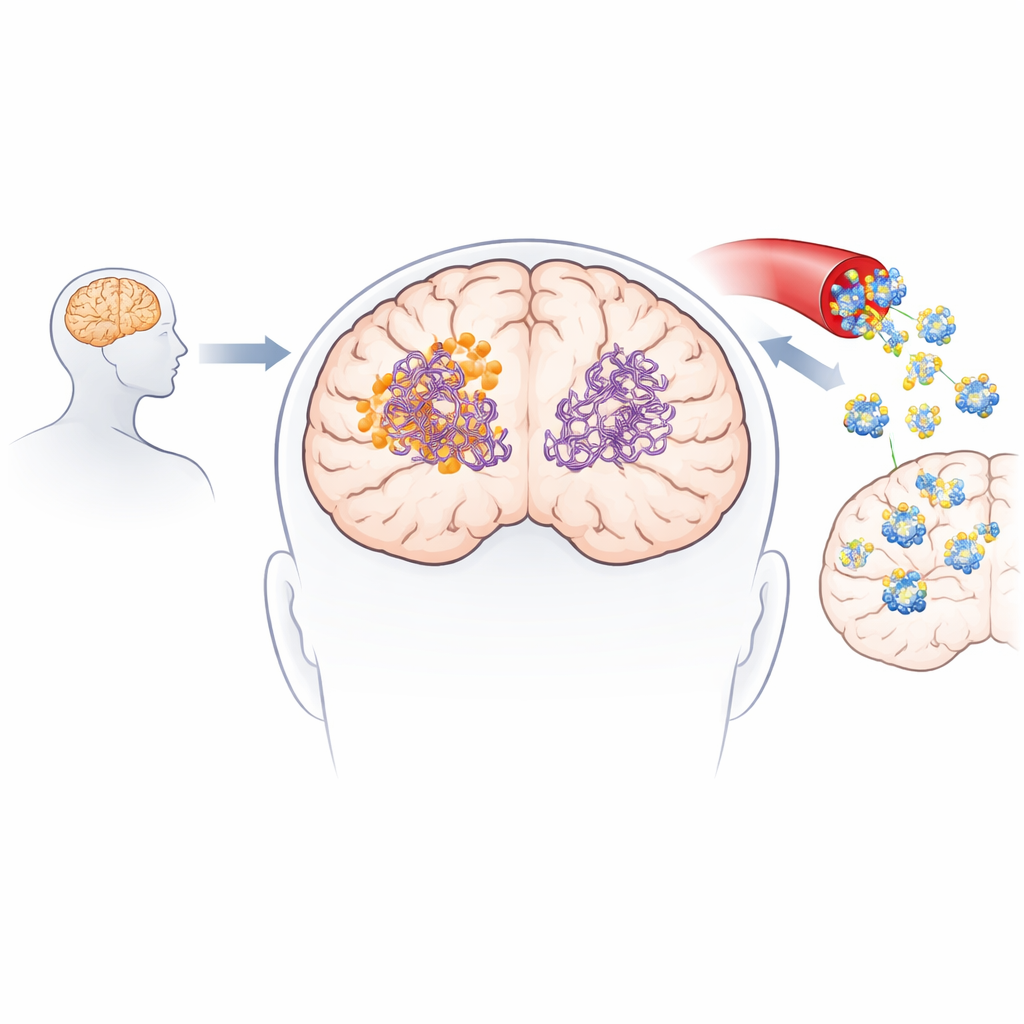
Simulationen zeigen, wie es toxische Fasern greift
Um zu verstehen, wie das neue Molekül mit krankheitsverursachenden Proteinen interagieren könnte, wandte sich das Team künstlicher Intelligenz und molekularer Simulationen zu. Sie nutzten aktuelle Docking-Modelle, um Tausende von möglichen Bindungsmodi zu vorgeformten Amyloid-beta- und Tau-Fasern zu untersuchen. Die Berechnungen zeigten konsistent, dass 3-Desoxycollinoketon B stärker an beide Fasertypen bindet als Collinolacton, indem es sich in hydrophobe (wasserabweisende) Taschen einlegt und stabilisierende Kontakte wie Wasserstoffbrücken und Salzbrücken bildet. Molekulardynamik-Simulationen verfolgten die Fasern über die Zeit und zeigten, dass das gebundene Molekül die lokale Flexibilität erhöht und kritische Kontakte zwischen Proteinsträngen schwächt, wodurch die Fasern in Richtung strukturellen Zerfalls gedrängt werden.
Vom Reagenzglas zum Mausgehirn
Laborexperimente bestätigten, dass 3-Desoxycollinoketon B nicht nur die Bildung neuer Amyloid-beta- und Tau-Fasern verlangsamt, sondern auch bestehende Fasern und kleinere, hochtoxische Oligomere aktiv aufspaltet. In zellfreien Tests reduzierte es Amyloid-beta-Fasern und Oligomere in erheblichem Maße und zeigte noch stärkere Effekte auf Tau-Fragmente, die für die Bildung von Tangles zentral sind. Das Molekül durchquerte künstliche und biologische Modelle der Blut–Hirn-Schranke und war nach intravenöser sowie oraler Verabreichung im Gehirn von Mäusen nachweisbar. In zwei verschiedenen Alzheimer-ähnlichen Mausmodellen senkte eine kurz- und längerfristige Behandlung die Mengen an Amyloidplaques und löslichen Amyloid-Spezies, verringerte Marker der Gehirnentzündung, stellte synaptische Proteine teilweise wieder her und verbesserte die Leistung in Gedächtnis- und Lernaufgaben wie Y-Maze und Novel-Object-Recognition. 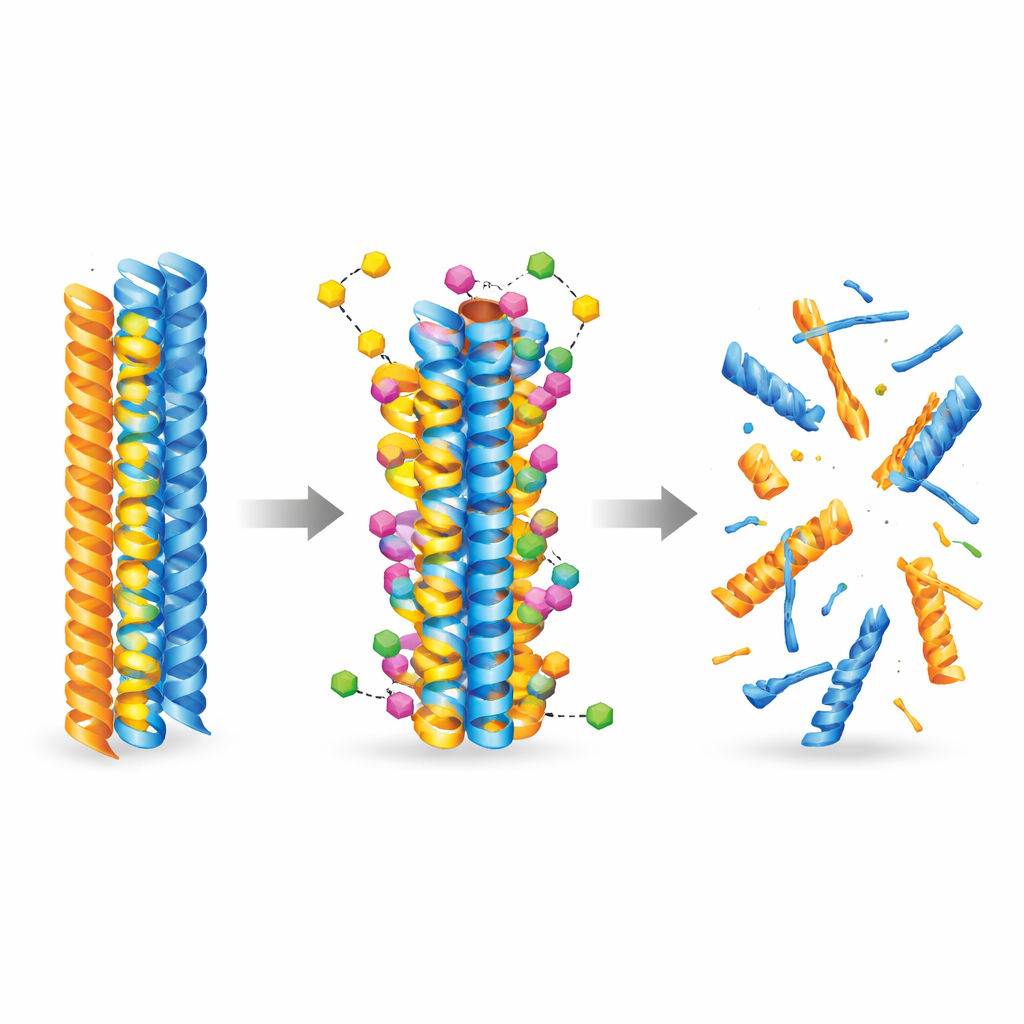
Versprechen und nächste Schritte
Insgesamt zeigt die Studie, dass 3-Desoxycollinoketon B ein dual wirkendes Kleinmolekül ist, das ins Gehirn eindringen, stark an sowohl Amyloid-beta- als auch Tau-Aggregate binden und deren Auflösung fördern kann, was zu messbaren kognitiven Vorteilen bei Mäusen führt. Für Laien bedeutet das, dass die Verbindung ein wenig wie ein molekularer Lösungsmittel für zwei Schlüsseltypen Alzheimer-assoziierter Proteinaggregate wirkt, anstatt lediglich Symptome zu überdecken. Zwar wird das Molekül relativ schnell aus dem Körper eliminiert und muss weiter modifiziert werden, um länger im Blut präsent zu bleiben, doch machen seine skalierbare Synthese, die Gehirngängigkeit und die breite Aktivität gegen fehlgefaltete Proteine es zu einem vielversprechenden Ausgangspunkt für die Entwicklung zugänglicherer und kostengünstigerer Behandlungen, die Alzheimer an der Wurzel packen.
Zitation: Heo, S., Cha, M., Zhung, W. et al. Synthesis of 3-desoxycollinoketone B and its ability to reduce Alzheimer-associated misfolded proteins. Nat Commun 17, 3288 (2026). https://doi.org/10.1038/s41467-026-69662-z
Schlüsselwörter: Alzheimer-Krankheit, Amyloid-beta, Tau-Protein, Kleinmolekulare Therapie, Proteinaggregate