Clear Sky Science · ar
تخليق 3-ديسوكسيكولينوكيتون ب وقدرته على تقليل البروتينات المشوهة المرتبطة بمرض الزهايمر
زاوية جديدة على الزهايمر
ينجم مرض الزهايمر جزئياً عن تكتلات من البروتينات المشوهة التي تضر الدماغ ببطء، لكن العلاجات الحالية تفعل القليل لإزالة هذه الترسبات الضارة. تقدم هذه الدراسة قريباً تصنّعه مختبرياً لمركب نادر طبيعي يمكنه الوصول إلى الدماغ بشكل أكثر فاعلية ومهاجمة بروتينين رئيسيين في آن واحد. من خلال دمج الكيمياء المتقدمة والذكاء الاصطناعي ودراسات على الحيوانات، يبين الباحثون كيف يكسر هذا الجزيء الصغير التراكمات البروتينية السامة ويحسن الذاكرة في نماذج الفئران المصابة بالزهايمر.
مركب طبيعي بحدود
اكتشف العلماء سابقاً منتجاً طبيعياً بكتيريّاً يُدعى كولينولاكتون يمكنه تفكيك تكتلات البروتين المُشكّلة من أميلويد-بيتا وتاو—وهما بروتينا العلامة المميزة لمرض الزهايمر. ومع ذلك، فمن الصعب استخلاص الكولينولاكتون بكميات مفيدة من مصدره الميكروبي كما أنه ضعيف في الوصول إلى بعض مناطق الدماغ، لا سيما القشرة حيث يحدث الكثير من التلف في الزهايمر. تجعل هذه العيوب تطويره كدواء عملي أمراً صعباً. سعى الفريق إلى تصميم وتخليق جزيء ذي صلة يحافظ على الفعالية المفيدة للكولينولاكتون مع تحسين استقراره وقدرته على اختراق الدماغ.
بناء جزيء أكثر ذكاءً
باستخدام التخليق العضوي الحديث، بنى الباحثون مركباً جديداً سماه 3-ديسوكسيكولينوكيتون ب. جمعوا ثلاثة لبِنات كيميائية أبسط ثم أطلقوا تفاعل تكوين حلقي نادر يحاكي خطوة يُعتقد أنها تحدث في الطبيعة. شرحت الحسابات الحاسوبية التفصيلية لماذا يفضّل هذا التفاعل شكلاً معيناً ذا ثلاث حلقات أكثر استقراراً من البنى البديلة. الجزيء الناتج أكثر محبة للدهون قليلاً من المنتج الطبيعي الأصلي، وهي خاصية من المتوقع أن تساعده على اجتياز الحاجز الدموي الدماغي. ومن المهم أن طريق التخليق هذا قابل للتوسع، ما يعني أنه يمكن إنتاج كميات على مستوى الغرام بشكل موثوق في المختبر لإجراء اختبارات بيولوجية واسعة وتحسينات مستقبلية. 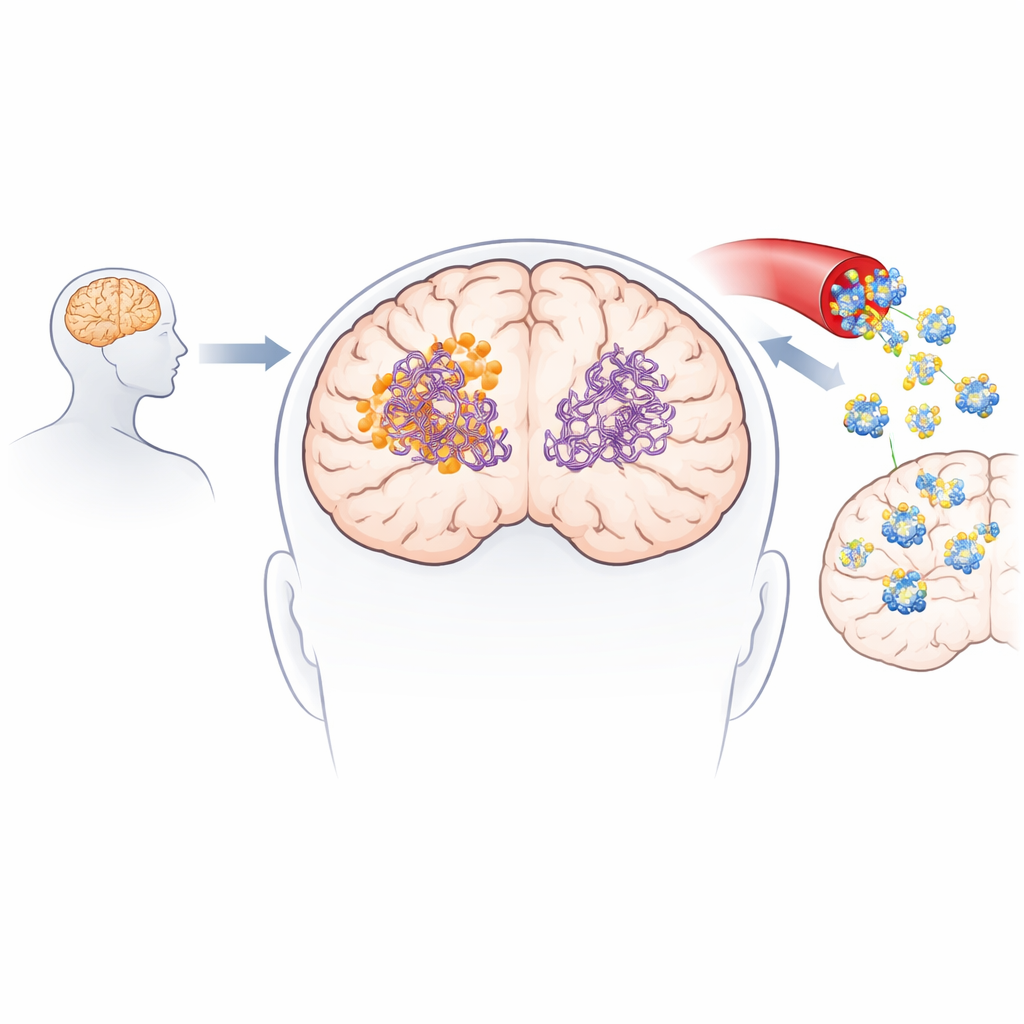
المحاكاة تكشف كيف يمسك بالألياف السامة
لفهم كيفية تفاعل الجزيء الجديد مع البروتينات المسببة للمرض، لجأ الفريق إلى الذكاء الاصطناعي والمحاكاة الجزيئية. استخدموا نماذج تركيب متقدمة لاستكشاف آلاف الطرق التي يمكن أن يرتبط بها المركب بالألياف المكوّنة مسبقاً من أميلويد-بيتا وتاو. أظهرت الحسابات باستمرار أن 3-ديسوكسيكولينوكيتون ب يرتبط بإحكام أكبر مع كلا النوعين من الألياف مقارنةً بالكولينولاكتون، متشعباً داخل جيوب كارهة للماء ويكوّن اتصالات مُثبِّتة مثل الروابط الهيدروجينية والجسور الملحية. ثم تابعت محاكاة الديناميكا الجزيئية الألياف مع مرور الزمن وكشفت أنه بمجرد الارتباط، يزيد المركب من المرونة المحلية ويضعف الاتصالات الحرجة بين شرائط البروتين، مما يدفع الألياف نحو الانهيار البنيوي.
من أنابيب الاختبار إلى أدمغة الفئران
أكدت التجارب المخبرية أن 3-ديسوكسيكولينوكيتون ب لا يبطئ فقط تكوّن ألياف أميلويد-بيتا وتاو الجديدة، بل يفكك أيضاً الألياف الموجودة والأوليغومرات الأصغر عالية السمية بنشاط. في تجارب خالية من الخلايا، خفّض المركب الألياف والأوليغومرات الخاصة بأميلويد-بيتا بنسب ملحوظة، وأظهر تأثيرات أقوى على شظايا تاو المركزية في تكوين التشابكات. عبر الجزيء نماذجاً اصطناعية وبيولوجية للحاجز الدموي الدماغي وكان قابلاً للكشف في أدمغة الفئران بعد إعطاء وريدياً وشفوياً. في نموذجين مختلفين شبيهيْن بالزهايمر لدى الفئران، خفضت المعالجات القصيرة والطويلة الأمد مستويات لويحات الأميلويد والأنواع القابلة للذوبان، قلّلت مؤشرات الالتهاب الدماغي، أعادت جزئياً بروتينات المشابك، وحسّنت الأداء في مهام الذاكرة والتعلّم مثل متاهةY والتعرف على جسم جديد. 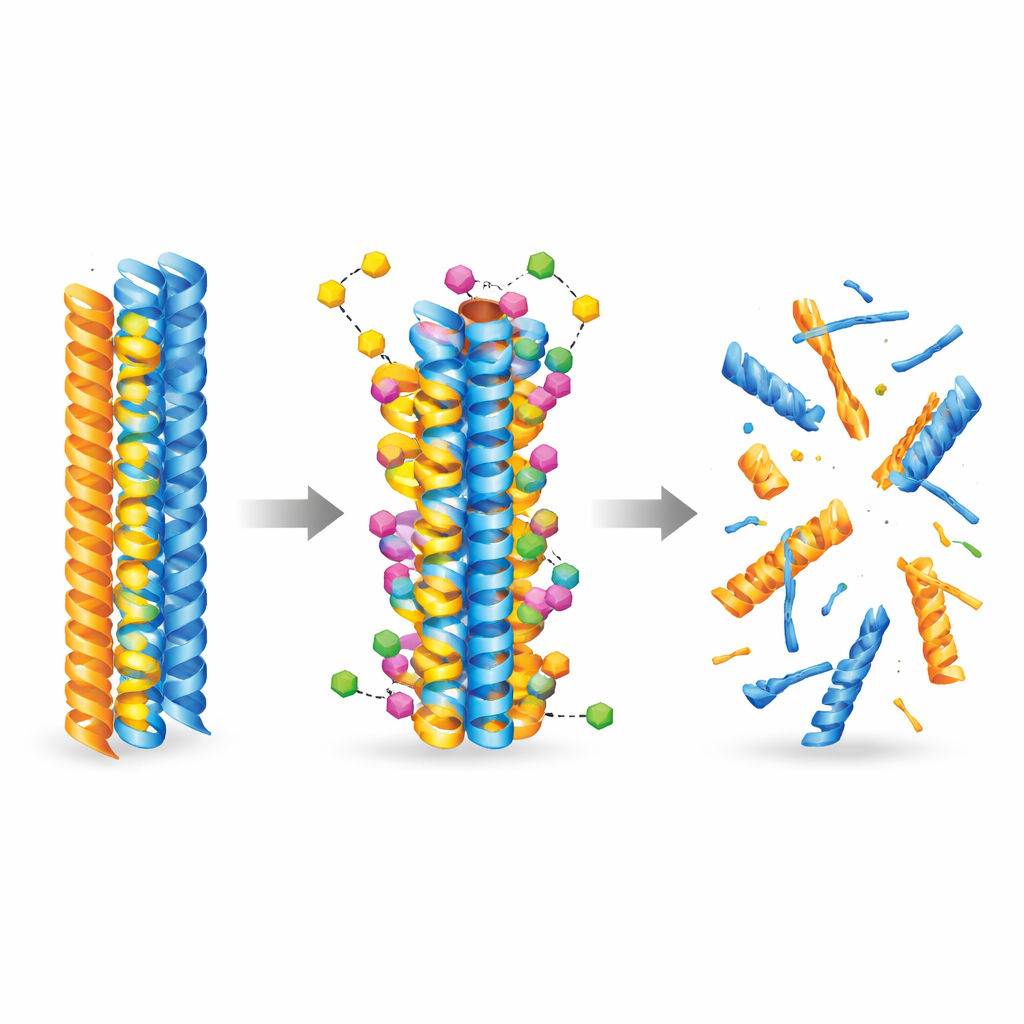
الوعد والخطوات التالية
بشكل عام، تُظهر الدراسة أن 3-ديسوكسيكولينوكيتون ب هو جزيء صغير ذو تأثير مزدوج يمكنه دخول الدماغ، والارتباط بإحكام بكل من تكتلات أميلويد-بيتا وتاو، وتعزيز تفككها، مما يؤدي إلى فوائد معرفية قابلة للقياس في الفئران. بالنسبة للقارئ العام، يعني ذلك أن المركب يعمل بمثابة مذيب جزيئي لنوعين رئيسيين من تكتلات البروتين المرتبطة بالزهايمر، بدلاً من مجرد إخفاء الأعراض. بينما يُطرد الجزيء من الجسم بسرعة نسبياً وسيحتاج إلى تعديل إضافي ليبقى فترة أطول في مجرى الدم، فإن قابليته للتخليق على نطاق، وقدرته على اختراق الدماغ ونطاق نشاطه الواسع ضد البروتينات المشوهة تجعله نقطة انطلاق واعدة لتطوير علاجات أكثر وصولاً وفعالية من حيث التكلفة تعالج مرض الزهايمر من جذوره.
الاستشهاد: Heo, S., Cha, M., Zhung, W. et al. Synthesis of 3-desoxycollinoketone B and its ability to reduce Alzheimer-associated misfolded proteins. Nat Commun 17, 3288 (2026). https://doi.org/10.1038/s41467-026-69662-z
الكلمات المفتاحية: مرض الزهايمر, أميلويد-بيتا, بروتين تاو, علاج بجزيئات صغيرة, تراكمات البروتين