Clear Sky Science · ja
3-デソキシコリノケトンBの合成とアルツハイマー関連の誤折りたたみタンパク質を低減する能力
アルツハイマーへの新たな視点
アルツハイマー病は、誤って折りたたまれたタンパク質の塊がゆっくりと脳を損傷することによって部分的に進行しますが、現行の治療法はこれら有害な沈着物を除去する効果がほとんどありません。本研究は、希少な天然化合物の人工的な類縁体を紹介し、それが脳へより効率的に到達し、二つの主要な問題タンパク質を同時に直接攻撃できることを示します。高度な化学、人工知能、動物実験を組み合わせることで、この低分子がどのように有毒なタンパク質凝集体を分解し、アルツハイマーのマウスモデルで記憶を改善するかを示しています。
制約のある天然分子
科学者たちは以前、アミロイドβとタウというアルツハイマー病の二つの特徴的タンパク質が形成する凝集体を分解できる細菌由来の天然物質コリノラクトンを発見しました。しかし、コリノラクトンは微生物由来から有用な量を抽出するのが難しく、特に皮質などアルツハイマーで大きな損傷が生じる脳領域への到達性が低いという欠点があります。これらの短所があるため、実用的な薬としての開発は困難でした。研究チームは、コリノラクトンの有益な活性を保持しつつ、安定性と脳内移行性を改善した関連分子を設計・合成することを目指しました。
より賢い分子の構築
現代の有機合成を用いて、研究者たちは3-デソキシコリノケトンBと呼ばれる新規化合物を合成しました。彼らは三つのより単純な化学ビルディングブロックを組み立て、その後、自然界で起こると考えられる段階を模倣する稀な環形成反応を誘起しました。詳細な計算化学は、この反応がなぜ特定の三環形状を優先するのかを説明し、それが他の構造よりも安定であることを示しました。得られた分子は元の天然物よりやや疎脂性が高く、これは血液脳関門を通過しやすくする性質と考えられます。重要な点として、合成経路はスケール可能であり、グラム単位の量を実験室で安定して生産できるため、広範な生物学的試験や今後の最適化に適しています。 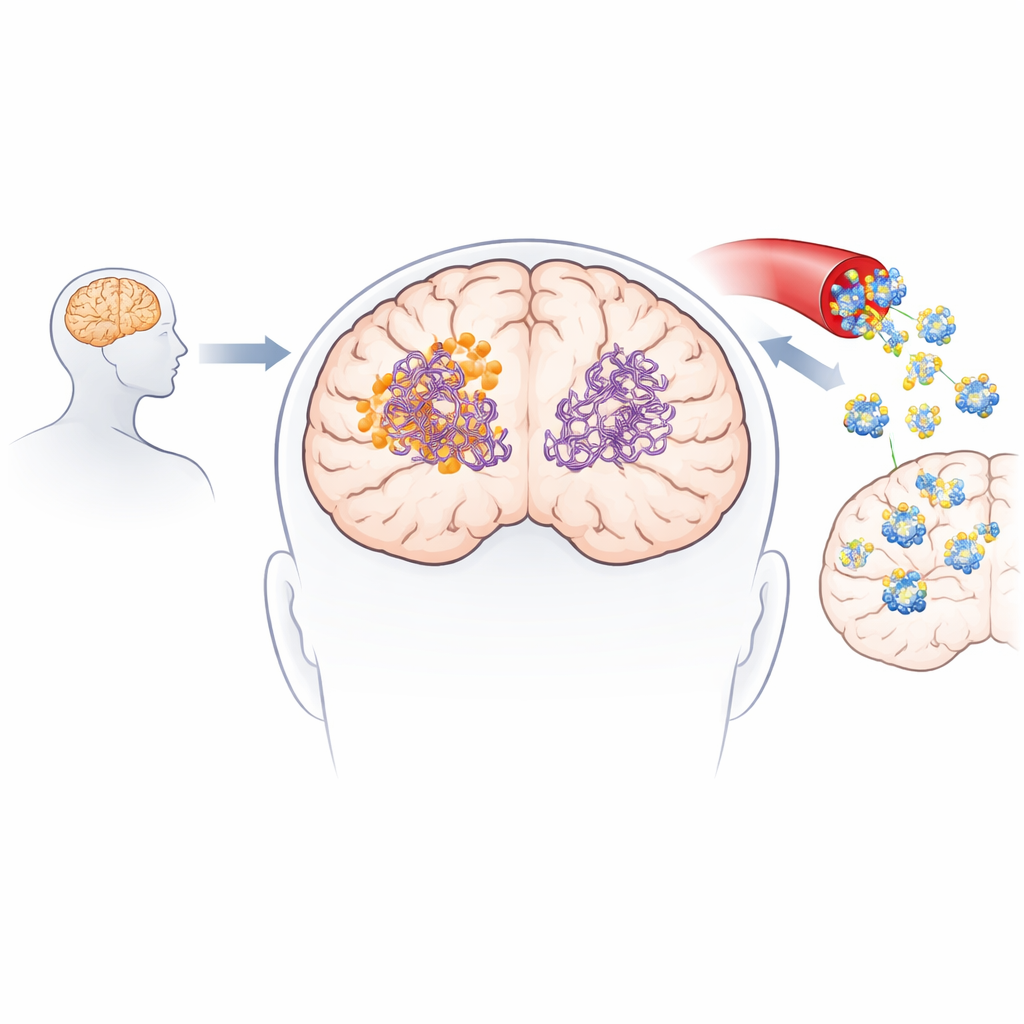
シミュレーションが示す毒性ファイバーへの握り方
新規分子が病原性タンパク質とどのように相互作用するかを理解するために、チームは人工知能と分子シミュレーションを活用しました。最先端のドッキングモデルを用いて、化合物が既に形成されたアミロイドβおよびタウの繊維に結合する何千通りもの可能性を探りました。計算結果は一貫して、3-デソキシコリノケトンBがコリノラクトンより両者の繊維により強く結合し、疎水性(親水を避ける)ポケットに収まり、水素結合や塩橋などの安定化接触を形成することを示しました。さらに分子動力学シミュレーションは時間経過で繊維を追跡し、結合後に局所的な柔軟性が増し、タンパク質鎖間の重要な接触が弱められて構造的崩壊へ向かうことを明らかにしました。
試験管からマウスの脳へ
実験室での試験により、3-デソキシコリノケトンBが新しいアミロイドβおよびタウ繊維の形成を遅らせるだけでなく、既存の繊維やより小さく高度に毒性を持つオリゴマーを能動的に分解することが確認されました。無細胞アッセイでは、アミロイドβの繊維とオリゴマーが有意に減少し、絡み合い形成の中心となるタウ断片に対してはさらに強い効果が示されました。該当分子は人工的および生体の血液脳関門モデルを通過し、静脈投与および経口投与のいずれの場合でもマウスの脳内で検出されました。二種類のアルツハイマー様マウスモデルにおいて、短期および長期の投与でアミロイド斑と可溶性アミロイド種のレベルが低下し、脳の炎症マーカーが減少し、シナプス蛋白の一部が回復し、Y迷路や新規物体認識といった記憶・学習課題での成績が改善しました。 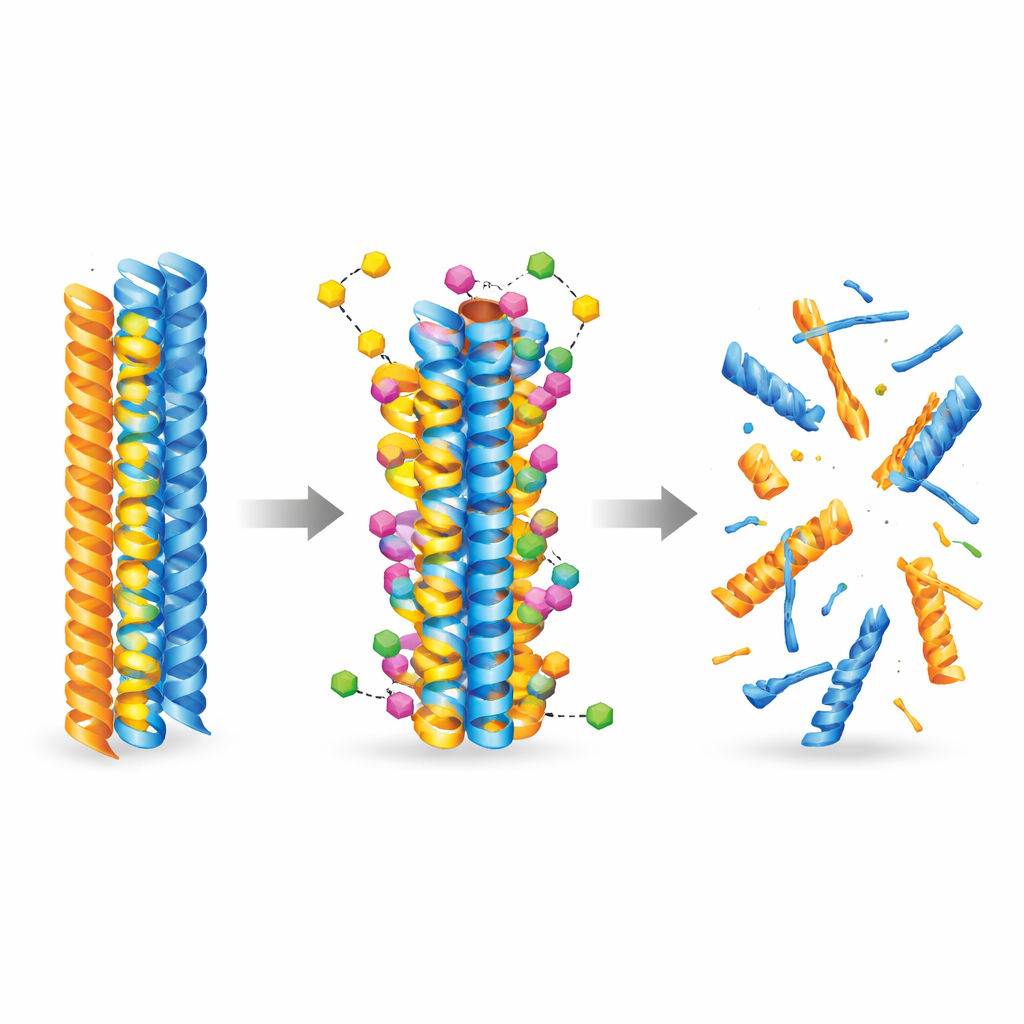
将来性と次の段階
総じて本研究は、3-デソキシコリノケトンBが脳へ到達し、アミロイドβとタウの両方の凝集体に強く結合してそれらの分解を促進し、マウスで計測可能な認知改善をもたらす二重作用の低分子であることを示しています。一般向けに言えば、この化合物は症状を単に覆い隠すのではなく、アルツハイマーに関連する二種類のタンパク質塊に対して分子レベルの“溶媒”のように作用すると考えられます。分子は体内から比較的速やかに消失するため血中滞留時間の延長などさらに調整が必要ですが、合成のスケール可能性、脳内浸透性、誤折りたたみタンパク質に対する広範な活性は、アルツハイマー病を根本から扱うよりアクセスしやすく費用効果の高い治療を開発するための有望な出発点となります。
引用: Heo, S., Cha, M., Zhung, W. et al. Synthesis of 3-desoxycollinoketone B and its ability to reduce Alzheimer-associated misfolded proteins. Nat Commun 17, 3288 (2026). https://doi.org/10.1038/s41467-026-69662-z
キーワード: アルツハイマー病, アミロイドβ, タウタンパク質, 低分子療法, タンパク質凝集体