Clear Sky Science · fr
Synthèse du 3-desoxycollinoketone B et capacité à réduire les protéines mal repliées associées à la maladie d’Alzheimer
Un nouvel angle sur la maladie d’Alzheimer
La maladie d’Alzheimer est en partie provoquée par des amas de protéines mal repliées qui détériorent progressivement le cerveau, mais les traitements actuels font peu pour éliminer ces dépôts nocifs. Cette étude présente un analogue synthétique d’un composé naturel rare qui peut atteindre le cerveau plus efficacement et s’attaquer directement à deux protéines problématiques majeures à la fois. En combinant chimie avancée, intelligence artificielle et études animales, les chercheurs montrent comment cette petite molécule dégrade les agrégats protéiques toxiques et améliore la mémoire dans des modèles murins de la maladie d’Alzheimer.
Une molécule naturelle avec des limites
Des scientifiques ont précédemment découvert un produit naturel bactérien appelé collinolactone capable de démanteler les amas protéiques formés par l’amyloïde-bêta et la tau — deux protéines emblématiques de la maladie d’Alzheimer. Cependant, la collinolactone est difficile à extraire en quantités utiles depuis sa source microbienne et a un accès limité à certaines régions du cerveau, en particulier le cortex, où se produisent une grande partie des dommages liés à Alzheimer. Ces inconvénients compliquent son développement comme médicament pratique. L’équipe s’est donc attelée à concevoir et synthétiser une molécule apparentée qui conserve l’activité bénéfique de la collinolactone tout en améliorant sa stabilité et sa capacité à traverser le cerveau.
Construire une molécule plus intelligente
Grâce à la synthèse organique moderne, les chercheurs ont construit un nouveau composé appelé 3-desoxycollinoketone B. Ils ont assemblé trois blocs de construction chimiques plus simples puis déclenché une réaction de fermeture de cycle rare qui imite une étape supposée se produire dans la nature. Des calculs informatiques détaillés expliquent pourquoi cette réaction favorise une conformation à trois anneaux spécifique, plus stable que les structures alternatives. La molécule résultante est légèrement plus lipophile que le produit naturel d’origine, une propriété susceptible de faciliter son passage à travers la barrière hémato-encéphalique. Fait important, la voie synthétique est extensible, ce qui signifie que des quantités au gramme peuvent être produites de manière fiable au laboratoire pour des tests biologiques approfondis et une optimisation future. 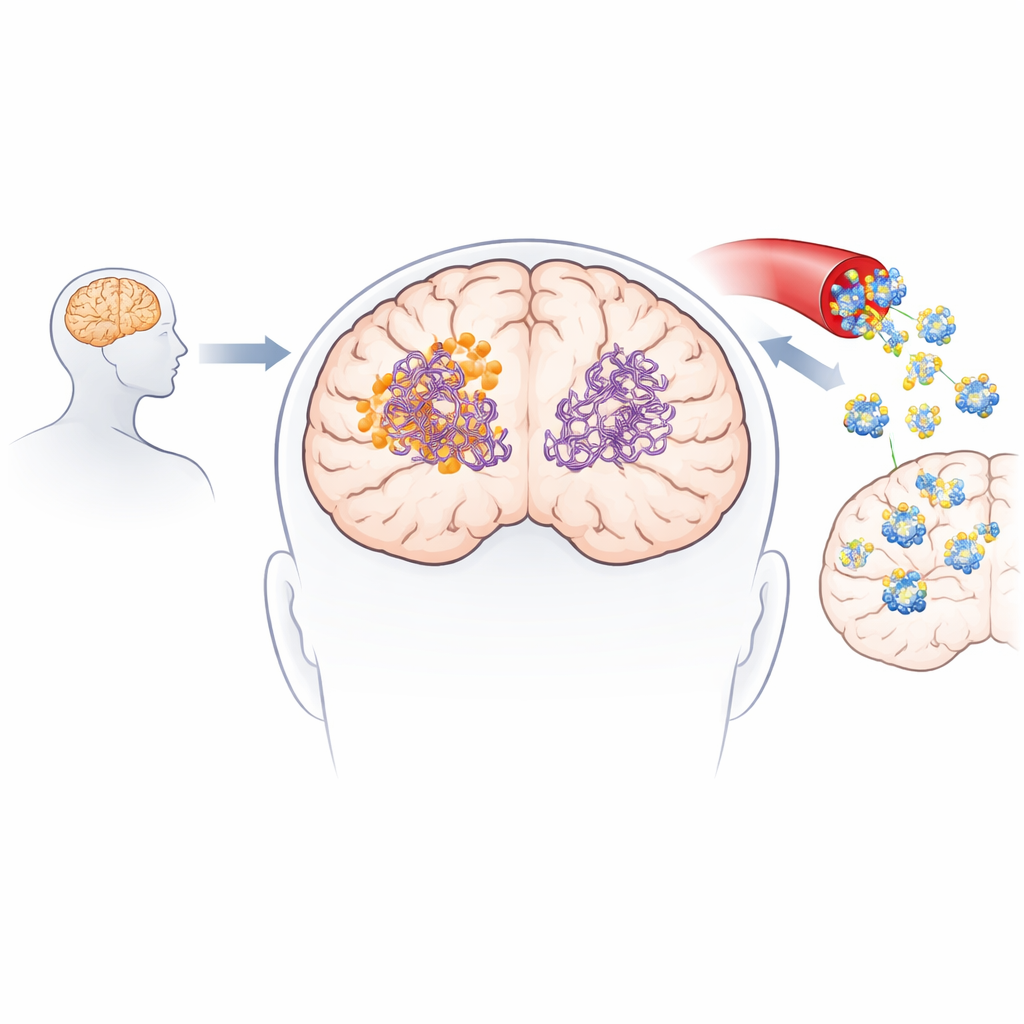
Des simulations révèlent comment elle agrippe les fibres toxiques
Pour comprendre comment la nouvelle molécule pourrait interagir avec les protéines responsables de la maladie, l’équipe s’est tournée vers l’intelligence artificielle et les simulations moléculaires. Ils ont utilisé des modèles de docking de pointe pour explorer des milliers de façons dont le composé pourrait se fixer aux fibres préformées d’amyloïde-bêta et de tau. Les calculs ont montré de façon cohérente que le 3-desoxycollinoketone B se lie plus fortement aux deux types de fibres que la collinolactone, s’insérant dans des poches hydrophobes (répulsives à l’eau) et formant des contacts stabilisants tels que des liaisons hydrogène et des ponts salins. Des simulations de dynamique moléculaire ont ensuite suivi l’évolution des fibres dans le temps et ont révélé qu’une fois lié, le composé augmente la flexibilité locale et affaiblit des contacts critiques entre les brins protéiques, poussant les fibres vers une dégradation structurelle.
Des éprouvettes aux cerveaux de souris
Des expériences en laboratoire ont confirmé que le 3-desoxycollinoketone B non seulement ralentit la formation de nouvelles fibres d’amyloïde-bêta et de tau, mais détruit aussi activement des fibres existantes et des oligomères plus petits et très toxiques. Dans des essais sans cellules, il a réduit de manière significative les fibres et oligomères d’amyloïde-bêta, et a montré des effets encore plus marqués sur des fragments de tau au cœur de la formation d’enchevêtrements. La molécule a traversé des modèles artificiels et biologiques de la barrière hémato-encéphalique et a été détectable dans le cerveau des souris après administration intraveineuse et orale. Dans deux modèles murins différents de type Alzheimer, des traitements de courte et de plus longue durée ont abaissé les niveaux de plaques amyloïdes et d’espèces amyloïdes solubles, réduit des marqueurs d’inflammation cérébrale, restauré partiellement des protéines synaptiques et amélioré les performances aux tâches de mémoire et d’apprentissage telles que le labyrinthe en Y et la reconnaissance d’un nouvel objet. 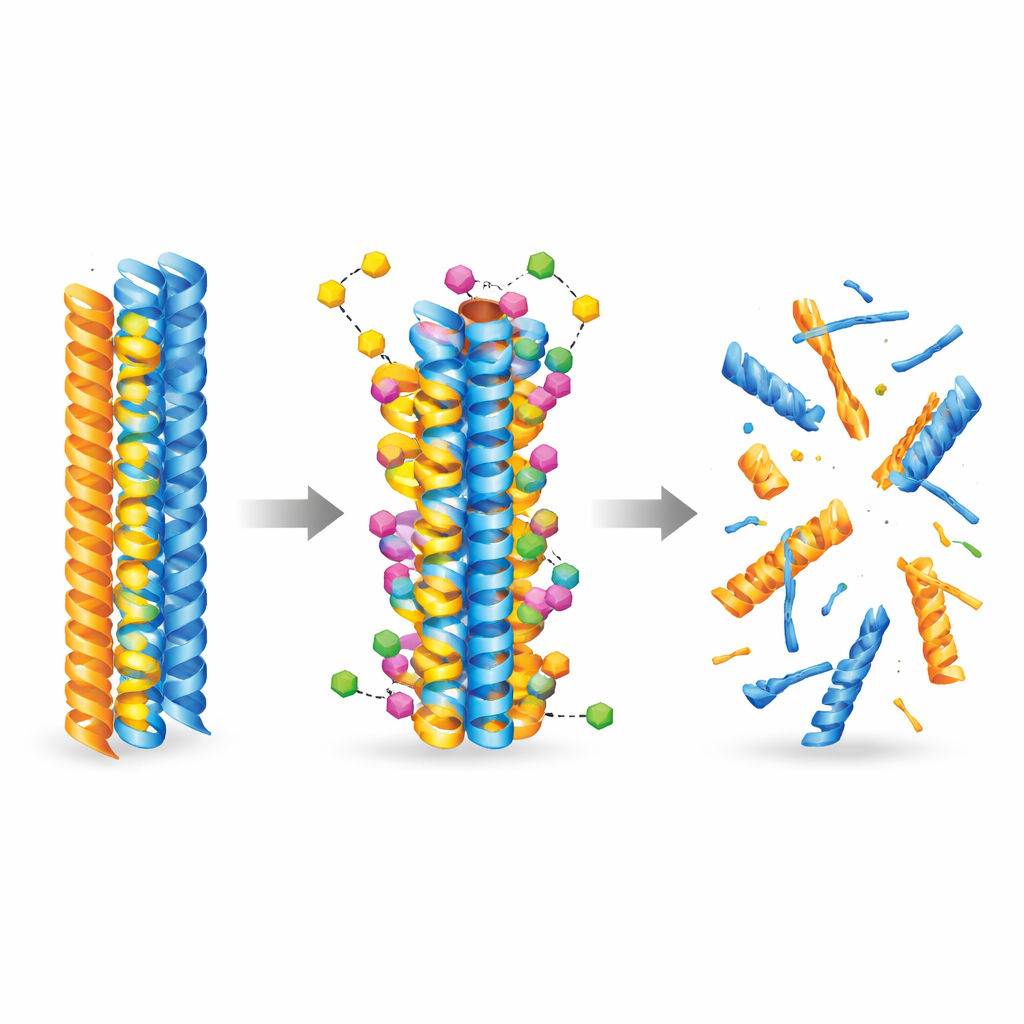
Promesses et étapes suivantes
Dans l’ensemble, l’étude démontre que le 3-desoxycollinoketone B est une petite molécule à double action capable de pénétrer le cerveau, de se lier fortement aux agrégats d’amyloïde-bêta et de tau, et de favoriser leur fragmentation, entraînant des bénéfices cognitifs mesurables chez la souris. Pour un non-spécialiste, cela signifie que le composé agit un peu comme un solvant moléculaire pour deux types clés d’amas protéiques liés à Alzheimer, plutôt que de simplement masquer les symptômes. Bien que la molécule soit éliminée relativement rapidement de l’organisme et nécessitera des ajustements pour durer plus longtemps dans la circulation sanguine, sa synthèse extensible, sa pénétration cérébrale et son activité large contre les protéines mal repliées en font un point de départ prometteur pour développer des traitements plus accessibles et économiques qui s’attaquent à la maladie d’Alzheimer à sa source.
Citation: Heo, S., Cha, M., Zhung, W. et al. Synthesis of 3-desoxycollinoketone B and its ability to reduce Alzheimer-associated misfolded proteins. Nat Commun 17, 3288 (2026). https://doi.org/10.1038/s41467-026-69662-z
Mots-clés: maladie d’Alzheimer, amyloïde-bêta, protéine tau, thérapie par petites molécules, agrégats protéiques