Clear Sky Science · it
Sintesi del 3-desossicollinoketone B e sua capacità di ridurre le proteine mal ripiegate associate all’Alzheimer
Un nuovo punto di vista sull’Alzheimer
La malattia di Alzheimer è in parte guidata da aggregati di proteine mal ripiegate che danneggiano lentamente il cervello, ma i trattamenti attuali rimuovono poco questi depositi nocivi. Questo studio presenta un parente sintetico di un raro composto naturale che può raggiungere il cervello in modo più efficace e attaccare direttamente due proteine problematiche contemporaneamente. Combinando chimica avanzata, intelligenza artificiale e studi su animali, i ricercatori mostrano come questa piccola molecola smantelli aggregati proteici tossici e migliori la memoria in modelli murini di Alzheimer.
Una molecola naturale con limiti
Studi precedenti hanno identificato un prodotto naturale batterico chiamato collinolattone in grado di smontare gli aggregati proteici formati da amiloide-beta e tau—due proteine distintive della malattia di Alzheimer. Tuttavia, il collinolattone è difficile da estrarre in quantità utili dalla sua fonte microbica e ha scarso accesso ad alcune regioni cerebrali, in particolare la corteccia, dove si verificano gran parte dei danni nell’Alzheimer. Questi svantaggi ne complicano lo sviluppo come farmaco pratico. Il team si è quindi posto l’obiettivo di progettare e sintetizzare una molecola correlata che conservi l’attività benefica del collinolattone migliorandone la stabilità e la capacità di penetrare nel cervello.
Costruire una molecola più intelligente
Servendosi della sintesi organica moderna, i ricercatori hanno costruito un nuovo composto chiamato 3-desossicollinoketone B. Hanno assemblato tre blocchi chimici più semplici e quindi innescato una rara reazione di formazione di anelli che imita un passaggio ritenuto avvenire in natura. Calcoli computazionali dettagliati hanno spiegato perché questa reazione favorisca una specifica conformazione a tre anelli, più stabile rispetto a strutture alternative. La molecola risultante è leggermente più lipofila rispetto al prodotto naturale originale, una caratteristica che dovrebbe aiutarla a permeare la barriera emato-encefalica. È importante che la via di sintesi sia scalabile, il che significa che è possibile produrre in modo affidabile quantità a livello grammo in laboratorio per ampi test biologici e per future ottimizzazioni. 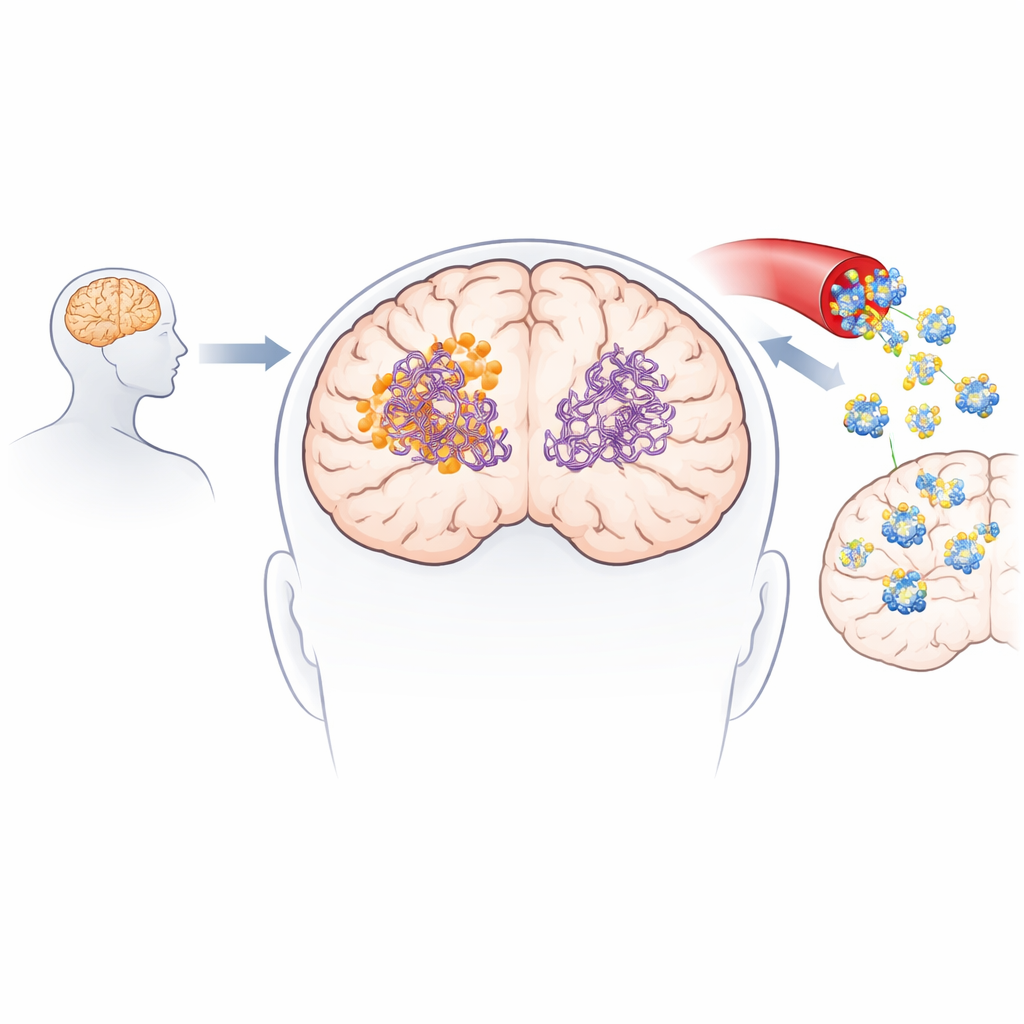
Simulazioni che rivelano come afferra le fibre tossiche
Per capire come la nuova molecola potesse interagire con le proteine responsabili della malattia, il gruppo si è rivolto all’intelligenza artificiale e alle simulazioni molecolari. Hanno utilizzato modelli di docking all’avanguardia per esplorare migliaia di modi in cui il composto potesse legarsi a fibre preformate di amiloide-beta e tau. I calcoli hanno mostrato in modo consistente che il 3-desossicollinoketone B si lega più saldamente a entrambi i tipi di fibre rispetto al collinolattone, posizionandosi in tasche idrofobiche (che respingono l’acqua) e formando contatti stabilizzanti come legami a idrogeno e ponti salini. Simulazioni di dinamica molecolare hanno poi seguito l’evoluzione delle fibre nel tempo e rivelato che, una volta legata, la molecola aumenta la flessibilità locale e indebolisce contatti critici tra le catene proteiche, spingendo le fibre verso il collasso strutturale.
Dalle provette ai cervelli dei topi
Gli esperimenti di laboratorio hanno confermato che il 3-desossicollinoketone B non solo rallenta la formazione di nuove fibre di amiloide-beta e tau, ma disgrega attivamente fibre già esistenti e oligomeri più piccoli e altamente tossici. In saggi cell-free ha ridotto in misura significativa fibre e oligomeri di amiloide-beta, mostrando effetti ancora più marcati sui frammenti di tau centrali nella formazione dei grovigli. La molecola ha attraversato modelli artificiali e biologici della barriera emato-encefalica ed è risultata rilevabile nei cervelli dei topi dopo somministrazione sia endovenosa sia orale. In due diversi modelli murini simili all’Alzheimer, trattamenti a breve e a lungo termine hanno abbassato i livelli di placche amiloidi e di specie amiloidi solubili, ridotto marcatori di infiammazione cerebrale, parzialmente ripristinato proteine sinaptiche e migliorato le prestazioni in compiti di memoria e apprendimento come il labirinto a Y e il riconoscimento di oggetti nuovi. 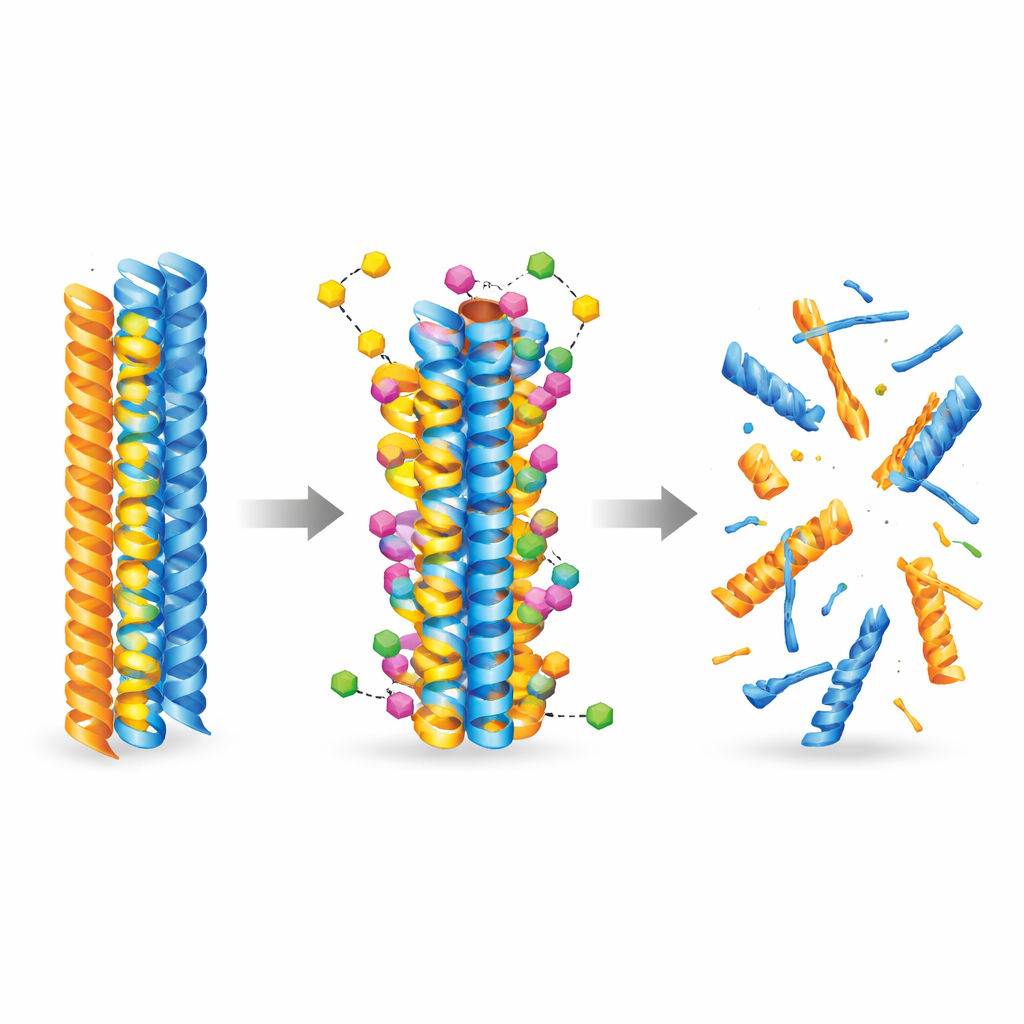
Promesse e prossimi passi
Nel complesso, lo studio dimostra che il 3-desossicollinoketone B è una piccola molecola ad azione duale in grado di entrare nel cervello, legarsi saldamente sia agli aggregati di amiloide-beta sia a quelli di tau e favorirne la disgregazione, con benefici cognitivi misurabili nei topi. Per il lettore non specialista, ciò significa che il composto agisce un po’ come un solvente molecolare per due tipi chiave di aggregati proteici legati all’Alzheimer, anziché limitarsi a mascherare i sintomi. Sebbene la molecola venga eliminata relativamente in fretta dall’organismo e necessiti di ulteriori modifiche per persistere più a lungo nel circolo ematico, la sua sintesi scalabile, la penetrazione cerebrale e l’ampia attività contro proteine mal ripiegate la rendono un punto di partenza promettente per sviluppare trattamenti più accessibili ed economici che affrontino la malattia di Alzheimer alla radice.
Citazione: Heo, S., Cha, M., Zhung, W. et al. Synthesis of 3-desoxycollinoketone B and its ability to reduce Alzheimer-associated misfolded proteins. Nat Commun 17, 3288 (2026). https://doi.org/10.1038/s41467-026-69662-z
Parole chiave: Malattia di Alzheimer, amiloide-beta, proteina tau, terapia con piccole molecole, aggregati proteici